JAMA:前瞻性临床试验表明:快速全基因组测序比靶向测序更容易诊断出婴儿遗传病
2023-08-02 测序中国 测序中国 发表于上海
研究团队对400个婴儿的血液分别进行了快速全基因组测序和靶向基因组测序分析。
近日,来自Women and Infants Hospital of Rhode Island等单位的研究团队在JAMA发表了题为“Rapid Whole-Genomic Sequencing and a Targeted Neonatal Gene Panel in Infants With a Suspected Genetic Disorder”的文章。研究团队对400个婴儿的血液分别进行了快速全基因组测序和靶向基因组测序分析。数据显示,快速全基因组测序获得结果的中位时间为6.1天,分子诊断率为49%,靶向基因组测序检测获得结果的中位时间为4.2天,分子诊断率为27%。在住院婴儿中,快速全基因组测序方法获得了更高的分子诊断率,但与靶向基因租测序相比,返回结果的时间更长。该研究中,76%的临床医生认为快速基因组检测在临床决策中有用或非常有用。

为了改善新生儿和婴儿的临床诊断,基因组测序必须提供及时和准确的分子诊断。当前,商业上可用的靶向测序检测可以嵌入有限数量的特定遗传病相关基因,这些靶向测序的Panel比全基因组测序更便宜,返回结果更快。但基因组测序和靶向新生儿基因测序之间的比较分析在之前的研究中并未涉及。
由美国国家卫生研究院支持的前瞻性、比较性、多中心研究“患病婴儿和新生儿基因组医学研究项目(The Genomic Medicine in Ill Infants and Newborns,GEMINI),在疑似患有遗传病的1岁以下住院婴儿中比较了基因组测序的诊断时间、分子诊断率和靶向新生儿基因检测的临床应用。
2021年,一项中期分析报告描述了首批113名GEMINI参与者的结果,共检测到51种新变异。此次JAMA发表的文章为GEMINI项目的最新成果。
主要研究内容
该研究共纳入400名疑似患有遗传病的住院婴儿、388名母亲和318名父亲,参与者为研究提供了血液进行了快速全基因组测序和靶向基因组测序分析。其中大多数婴儿在妊娠37周或更长时间后出生(63.0%),另有57.9%通过剖宫产分娩。
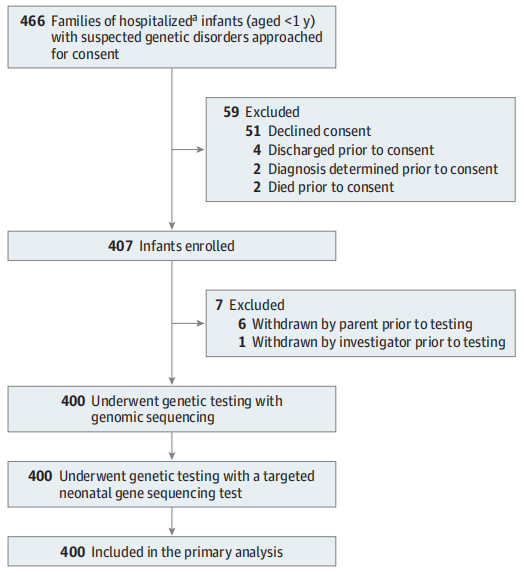
图1. 研究流程图
在400名婴儿中,最终204名(51%)婴儿鉴定了297个分子诊断变异,其中134个是新变异,这些婴儿至少携带1种基因变异被确定为致病或可能致病或意义不明的变异(VUS)。9名婴儿在非编码区域发现可疑的VUS,8名婴儿发现了大的结构变异。
结果显示,195名婴儿通过快速全基因组测序鉴定出遗传变异,109名婴儿通过靶向基因组测序鉴定出遗传变异。在鉴定出携带遗传变异的婴儿中,95名婴儿的诊断(164个遗传变异)是通过快速全基因组测序鉴定的,但无法通过靶向基因组测序检测到;9名婴儿的诊断(19个遗传变异)是通过靶向基因组测序检测的,但没有被基因组测序检测到。这一结果表明,与靶向基因组测序检测相比,快速全基因组测序的分子诊断几率增加了近10倍。
此外,在107例急诊婴儿病例中,研究团队利用快速全基因组测序诊断了59例,靶向基因组测序诊断了35例。对于紧急病例,快速基因组测序的周转时间为3.3天,靶向基因组测序的周转时间为4天。
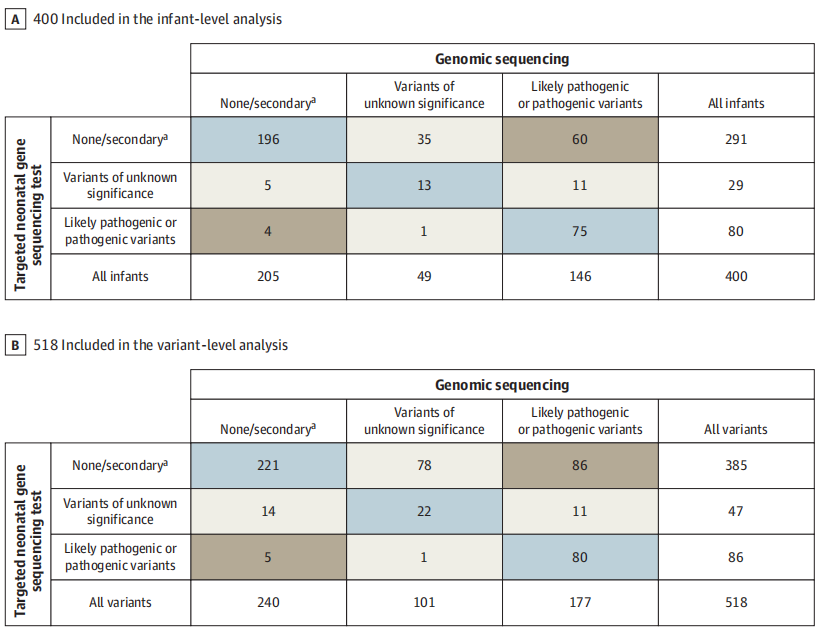
图2. 快速基因组测序与靶向基因组测序的比较分析
总体而言,297个分子诊断致病性或可能致病性基因变异或可疑VUS能够通过快速基因组测序、靶向基因组测序检测或同时检测,包括134种表型相关基因的新变异,以及73种被美国医学遗传学和基因组学学院归类为VUS的可疑致病变异。
在195个不一致变异中,靶向基因组测序检测无法检测到长度超过1kb的结构变异或不在预设Panel中的基因变异。当两种方法都能够检测到相同变异时,变异注释和分类在43%的情况下存在差异。研究团队认为,不一致的原因包括总体基因覆盖、计算过滤、嵌合体、线粒体基因变异和注释技术等。此外,通过提供至少一个亲本样本,87%的变异遗传可以通过快速基因组测序确定。
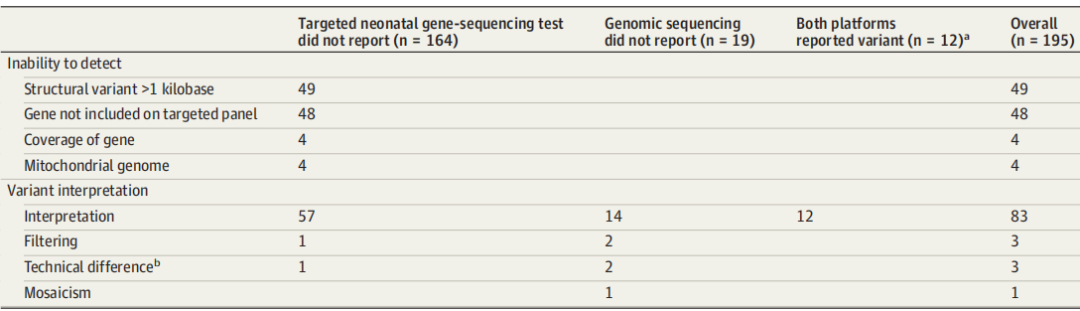
图3. 不一致变异结果的来源
该研究中,大多数医生 (398人中有302人) 认为快速全基因组测序是有用的或非常有用的,无论是否提供诊断信息。在符合接受继发性发现条件的374名婴儿中,鉴定出24种变异。12位母亲和15位父亲具有与先证者相同的常染色体显性致病或可能致病变异,三个母亲和一个父亲有与癌症风险增加相关的变异,并接受了遗传咨询。
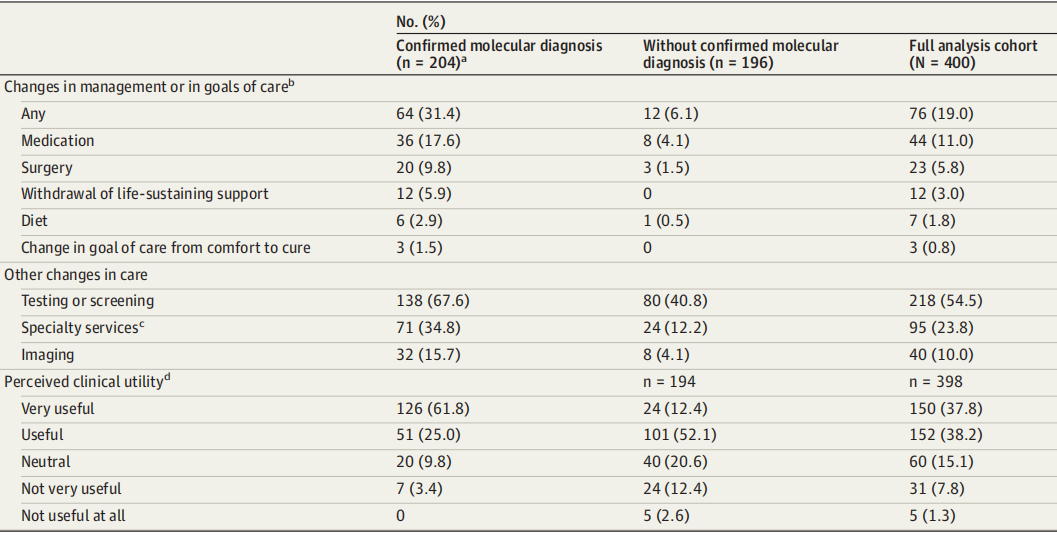
图4. 基因组检测的临床应用
结 语
该临床结果显示,快速全基因组测序的分子诊断率高于靶向基因组测序检测,但结果的返回时间相对较慢。此外,实验室间变异注释能力可能导致分子诊断率的差异,这可能对临床管理产生重要影响。
该文章通讯作者Jonathan Davis和第一作者Jill Maron教授表示:“这不仅是第一个对全基因组测序和靶向基因组测序的诊断率、临床实用性和诊断时间进行比较分析的研究,而且还包括在计算诊断率时检测可疑的VUS。”
Davis和Maron补充道:“可疑的VUS被定义为导致呈现表型的基因中发现的变异,并被报告给临床护理团队以通知医疗管理,这些变异的报告促使一些患者的护理得到改善。我们强烈支持医疗补助和商业保险公司覆盖全基因组测序,并且随着技术的进步,其成本也正在下降。此外,早期诊断也为成功治疗许多遗传病提供了巨大的机会,其中许多疾病目前是致命的。”
参考资料:
1. Maron JL, Kingsmore S, Gelb BD, et al. Rapid Whole-Genomic Sequencing and a Targeted Neonatal Gene Panel in Infants With a Suspected Genetic Disorder. JAMA. 2023.
https://jamanetwork.com/journals/jama/article-abstract/2807081?resultClick=1.
2.Infant Rapid Genome Sequencing Yields More Diagnoses Than Targeted Gene Panels, Study Finds
https://www.genomeweb.com/sequencing/infant-rapid-genome-sequencing-yields-more-diagnoses-targeted-gene-panels-study-finds
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言