STM:捷报!靶向编辑某一基因可逆转先天性肺部疾病
2019-04-24 Paris Echo 转化医学网
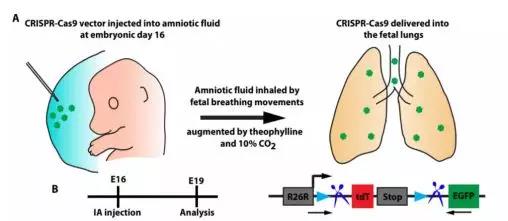
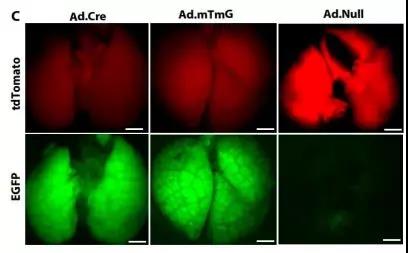
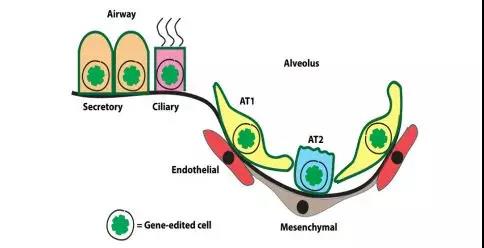
自20世纪初至今,短短百年之内,基因技术研究领域的高歌猛进,让人类与基因之间的关系发生了巨变。去年,首例基因编辑婴儿的问世引发了众多热议,但是抛开伦理问题,基因技术无疑在不断走向成熟。近日,宾夕法尼亚大学医学院和费城儿童医院在基因编辑领域再次取得突破,他们的研究团队成功修复了小鼠的一种致命基因突变,更让人赞叹的是,这种修复在小鼠出生之前便可以完成。这无疑是遗传性疾病治疗史上的一大里程碑事件。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#STM#
47
#先天性#
35
#肺部疾病#
41