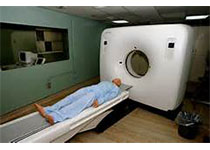
上海实施医疗器械优先审批流程 为医技创新开辟绿色通道
上海9月1日起实施《第二类医疗器械优先审批程序》,那些临床急需以及列入国家、上海科技重大专项或重点研发计划的医疗器械将在审批过程中单独排序,优先审评,确保能够在安全的情况下以最快的速度上市,为病人解忧。
中国医疗科技网 - 上海,医疗,器械 - 2017-09-03
CFDA改名“医疗产品监管局” 数字医疗产品审评思路浮出水面
导读:国家药监局英文简称定为“NMPA”,其中“medical products”的表述引发对药监局将来审评内容的猜测。我国数字医疗产品的审评政策与标准目前还不明确,但健康点昨日独家获悉药监局医疗器械审评中心专家对此类产品的审评思路,初步考虑将作为医疗器械报批的医疗AI软件区分为中低风险、高风险两个审评通道。
健康点healthpoint - CFDA - 2018-09-01
药监局发布进口医疗器械产品在中国境内企业生产相关公告
日前,国家药监局发布了关于进口医疗器械产品在中国境内企业生产有关事项的公告,适用范围为,进口医疗器械注册人通过其在境内设立的外商投资企业在境内生产第二类、第三类已获进口医疗器械注册证产品的有关事项。
药监局 - 医疗器械,中国境内,相关公告 - 2020-10-02
6大医疗文件被清理!简政放权又进一步
年第1号公告,公告公布了现行有效部门规章91项目录,将继续执行;决定不再作为部门规章纳入规范性文件管理的文件目录6项,包括《医疗机构设置规划指导原则》、《医用氧舱临床使用安全技术要求》、《妇幼保健机构评审实施规范》、《乡(镇)卫生院评审标准》、《医院乡(镇)卫生院评审结论判定标准》、《医疗事故分级标准(试行)》六项,实际上就是废除这6项规章。
“看医界”微信号 - 卫计委,医疗文件,公告 - 2018-01-22
国家卫计委取消三级医院评审结果复核与评价 加强事中事后监管
12月1日,国家卫计委网站发出关于取消三级医院评审结果复核与评价行政许可事项有关工作的通知,明确三级医院评审结论改为备案管理。各省级卫生计生行政部门将三级医院评审结论在辖区内公布后,将评审医院名单、医疗机构设置规划、评审标准、评审组织方式、结果及认定程序等向国家卫生计生委备案。2009年,根据新医改要求印发了《医院评审暂行办法》、《三级综合医院评审标准2011年版》等一系列评审工作文件,各地以医疗
国家卫计委 - 三级医院,国家卫计委 - 2017-12-01
国家卫计委:废除六项医疗规章 深化“放管服”改革
公告公布了现行有效部门规章91项目录,这91项将继续执行;决定不再作为部门规章纳入规范性文件管理的文件目录6项(截止2017年12月31日),包括《医疗机构设置规划指导原则》、《医用氧舱临床使用安全技术要求》、《妇幼保健机构评审实施规范》、《乡(镇)卫生院评审标准》、《医院乡(镇)卫生院评审结论判定标准》、《医疗事故分级标准(试行)》,实际上就是废除
健康界 - 医疗规章,放管服 - 2018-01-24
CFDA发布公告修订《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》
一、《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》修订的总体思路和原则是什么? 依据《条例》设定的原则和要求对《办法》进行修订。修订的总体思路与《条例》修订的总体思路保持一致,以分类管理为基础,以风险高低为依据,确定医疗器械注册与备案的具体要求。医疗器械注册是一项行政许可制度,是食品药品监督管理部门根据医疗器械注册申请人的申请,依照法定程序,对其拟上市医疗器械的安全性、有效性研究及其
CFDA - CFDA - 2015-02-09
详解:药械监管审批拉开巨变大幕
2020年12月22日,国务院常务会议上通过了《医疗器械监督管理条例》。时隔两年,当年的修订草案终于转正落地。虽然最终落地的政策终版尚未发布,但是医疗器械行业的监管剧变几乎已经在所难免。
动脉网 - 国内医疗市场,一蹴而就,崭新的开始 - 2021-01-04
《药品专利纠纷早期解决机制实施办法(试行)》公开征求意见
9月11日,国家药监局综合司、国家知识产权局办公室发布《药品专利纠纷早期解决机制实施办法(试行)(征求意见稿)》。规定化学仿制药申请人提交药品上市许可申请时,应当对照已在中国上市药品专利信息登记平台载
医谷网 - 意见,药品专利,仿制药品 - 2020-09-14
中国唯一的“医疗特区”博鳌乐城再出发
11月初,海南省琼海市天气微凉。从博鳌亚洲论坛国际会议中心出发,一路都是茂密的树林,大概开了13公里后出现了一大片空地,周围林立着博鳌超级医院、博鳌恒大国际医院、海南启研干细胞抗衰老医院等9家已在运营的医院。
八点健闻(HealthInsight) - 博鳌乐城先行区,医疗特区 - 2019-11-27
食药监总局:临床试验中弄虚作假、捏造数据将被严处
10月8日,中共中央办公厅、国务院办公厅发布了《关于深化审评审批制度改革鼓励药品医疗器械
中新网 - 食药监总局,临床试验,弄虚作假 - 2017-10-09
实访博鳌:海南“临床急需”用药通道与全国进口药上市的赛跑
6月15日,国家药品监督管理局批复了我国首款肿瘤免疫治疗(Immuno-Oncology Therapy,简称I-O治疗)药物。紧随其后,其他几款I-O治疗药物的批复箭在弦上,国家可能“逼平”海南省在I-O治疗等进口药方面的先试先行政策。作为国内首个省级自由贸易区,海南正寻求更大的政策突破。据海南省政府相关人士透露,国家药品监督管理局正在联合海南省政府向中央报批,申请由全国人大常委会授权,允
健康点healthpoint - 海南,临床急需,用药 - 2018-06-27
年均增长近23% 高端医疗器械这把火会烧多久
虽然眼下正值料峭寒冬,但国产高端医疗器械的春天即将到来。调研显示,目前我国医疗器械市场已近4000亿元规模,年均增长率约23%,到2020年国内销售总额将超7000亿元,未来10年年均增速达10%以上,远高于全球5%增长均值,可见国产医疗器械产业已加足马力,驶入快车道。行业散乱差 研发投入少虽然春天已不远,但棘手难题如冻冰三尺,还未消融。首先医疗器械行业整体处于“散、乱、差”的局面。华盖资本董
贝壳社 - 高端,医疗器械,增长 - 2018-01-04
医疗科技成果:要“开花”更要“结果”
“投资人都喜欢那种很快就能上市的产品。但我们只做出了原理样机,距离拿到产品注册证,最少还得再花一千万到两千万。”前不久,首都医科大学附属北京同仁医院眼科中心主任、北京市眼科研究所所长王宁利在带领团队研发眼压计原理样机的过程中,遇到了这样令人头疼的问题。研发本是为了惠及老百姓的健康,但产品孵化期该由谁来培育的问题,成了横亘在成果转化进程中的障碍。
医学科学报 - 医疗科技,成果转化,政策 - 2018-04-09
食品药品监管总局关于实施《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》有关事项的通知
食品药品监管总局关于实施《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》有关事项的通知 食药监械管〔2014〕144号 2014年08月01日 发布 各省、自治区、直辖市食品药品监督管理局:
CFDA - 医疗器械注册管理,食品药品监管总局 - 2014-08-06
为您找到相关结果约236个