多维度多准则中成药综合评价技术指导原则解读
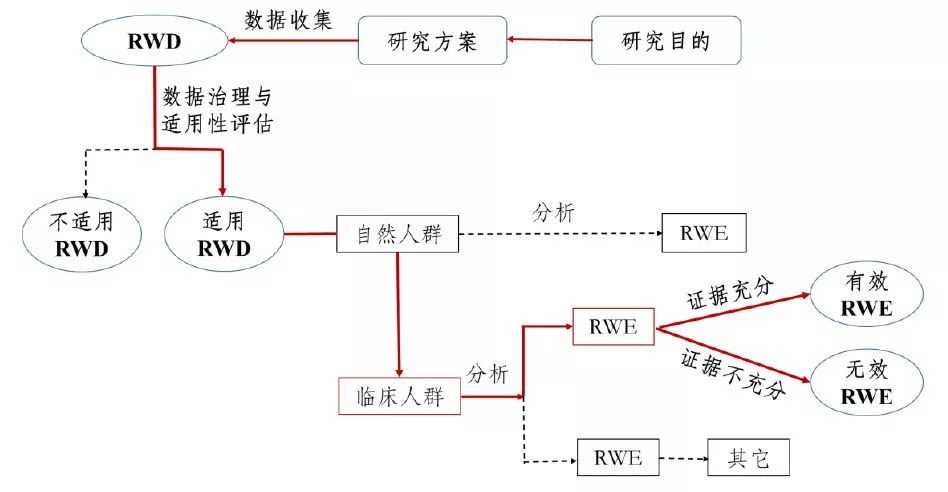
多维度、多准则中成药综合评价技术指导原则已经发布,提出了从安全、有效、经济、应用、科学、标准六大方面对中成药综合价值进行评价的技术指标体系(第一版
中国循证医学杂志 - 中成药 - 2022-07-31
总局发布质子碳离子治疗系统临床评价技术审查指导原则
1月8日,食品药品监管总局发布通告称,为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家食品药品监督管理总局组织制定了质子碳离子治疗系统临床评价技术审查指导原则(见附件),现予发布。
新浪医药新闻 - CFDA,质子碳离子治疗,质子碳离子治疗 - 2018-01-09
42种新型抗肿瘤药物临床应用指导原则进入“普法期”
近年来,抗癌新药在我国上市的脚步日益加快,且随着17种抗癌药纳入国家医保等惠民新政落地,患者对药物的可及性也越来越高。规范新抗癌药的应用,纳入国家监管部门的视野。
文汇报 - 新型抗肿瘤药物,临床应用 - 2019-04-16
妊娠期和哺乳期患者用药错误防范指导原则
本指导原则适用于医院机构在涉及妊娠期和哺乳期患者药物治疗的所有医务人员,旨在为防范妊娠期和哺乳期患者发生用药错误提供技术指导,确保妊娠期和哺乳期患者用药安全。
药物不良反应杂志.2017,19(3): - 妊娠期,哺乳期,用药错误 - 2017-09-10
【特别分享】呼吸机同品种临床评价注册审查指导原则
为进一步规范呼吸机医疗器械的管理,国家药监局器审中心组织制定了《呼吸机同品种临床评价注册审查指导原则》,现予发布。点击立即下载查看。
网络 - 呼吸机 - 2024-02-04
【今日分享解读】高流量呼吸治疗设备注册审查指导原则
为规范部分有源产品的注册申报和技术审评,国家药监局器审中心组织制定了《高流量呼吸治疗设备注册审查指导原则》等4项指导原则,现予发布。点击立即下载查看!
网络 - 2024-02-01
罕见疾病药物临床研发技术指导原则(征求意见稿)
罕见疾病是发病率极低的一组疾病的统称,由于中国拥有庞大的人口基数,罕见疾病患者的绝对患病人数并不少,对社会、经济、医疗等多方面均存在不容忽视的影响,是严重的公共健康问题之一。当前大部分罕见疾病尚缺乏有
CDE - 罕见病 - 2021-10-15
抗肿瘤药物临床试验技术指导原则(第二稿)
二○○七年三月 一、概述: 肿瘤疾病是严重威胁人类生命的一类疾病,尽管现有治疗手段取得了一定疗效,但多数肿瘤患者生存时间有限,缺乏有效的可以治愈的药物,亟需开发新的药物来满足患者需要。为达到延长生存的目标,患者往往愿意承担比其他药物更大的安全性风险,这使得对肿瘤药物的风险效益权衡不同于其他药物,也使得肿瘤药物的临床研究完全遵循一
MedSci原创 - 肿瘤,试验 - 2013-04-17
FDA指导原则:癌症临床试验中核心患者报告结局(草案)
本指南为申办者提供了在癌症临床试验中收集一组核心患者报告临床结果的建议,以及仪器选择和试验设计的相关考虑因素。虽然本指南侧重于患者报告的结果 (PRO) 措施,但其中一些建议可能与癌症临床试验中的其他
FDA - 患者报告结局 - 2021-10-22
抗菌药物临床应用指导原则(征求意见稿)(2014版)
目录第一部分 抗菌药物临床应用的基本原则抗菌药物治疗性应用的基本原则抗菌药物预防性应用的基本原则抗菌药物在特殊病理、生理状况患者中应用的基本原则附录1抗菌药物在预防某些细菌性感染中的应用附录2抗菌药物在预防手术部位感染中的应用附录
2014-01-01
FDA指导原则:临床试验中种族和民族数据的收集
本指南的目的是提供 FDA 对在美国和国外进行的 FDA 监管医疗产品临床试验提交中使用标准化方法收集和报告种族和民族数据的期望和建议。使用年龄、性别、性别、种族和民族的标准术语有助于确保一致地收集亚
FDA - 临床试验 - 2021-10-22
古代经典名方中药复方制剂说明书撰写指导原则(试行)
为加快构建中医药理论、人用经验和临床试验相结合的中药注册审评证据体系,规范中医药理论申报资料和古代经典名方中药复方制剂说明书相关内容的撰写,在国家药品监督管理局的部署下,药审中心组织制定了《中药新药复
CDE - 经典名方 - 2021-10-15
为您找到相关结果约500个