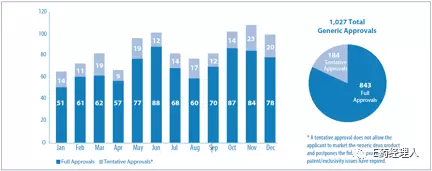
一年批准1027个仿制药
相较于其他年份,2017年美国批准仿制药数量更多,以1027件仿制药和暂时性批准创下历史之最;而在获批药品种类以及外部合作上也作出了更多新鲜的尝试。
E药经理人 - 仿制药,OGD,FDA - 2018-02-13
苏格兰医药协会批准两款NSCLC新药
近日,苏格兰医药协会(SMC)批准了百时美的PD-1抑制剂Opdivo (nivolumab)和辉瑞的靶向药Xalkori (crizotinib)用于治疗非小细胞肺癌。
生物谷 - 百时美,辉瑞 - 2016-07-18
诺华眼科药物Jetrea获加拿大卫生部批准
比利时生物技术公司Thrombogenics 8月16日宣布,眼科药物Jetrea已获加拿大卫生部批准,这是该药在欧美之外地区获得的首个监管批准。
生物谷 - 新药,FDA - 2013-08-21
梯瓦(Teva)抗过敏喷鼻剂Qnasl获FDA批准
2012年3月26日,梯瓦(Teva)公司周一宣布,FDA批准其药物Qnasl用于鼻过敏症(nasal allergy symptoms)的治疗。Qnasl是处方药,将于4月份上市,该药已被批准用于12岁及以上患有季节性过敏或常年过敏患者。 梯瓦(Teva)公司的股票价格在今晨早盘交易中上涨50美分
生物谷 - 新药,FDA - 2012-04-16
ACADIA制药宣布FDA批准NUPLAZID(Pimavanserin)的新剂量和配方
ACADIA制药公司于2018年6月29日宣布FDA批准了NUPLAZID(pimavanserin)的新剂量和配方,以帮助治疗患有幻觉和与帕金森病精神病相关的妄想症患者
MedSci原创 - Pimavanserin,帕金森,ACADIA - 2018-06-30
FDA批准全球首例数字药物 可追踪病人是否服药
据华尔街日报报道,美国有关部门批准了世界上首例数字药物,这种治疗精神疾病的药丸进入人体消化道后会向智能手机发出信号,以便医生追踪病人是否服药。美国食品和药物管理局(Food and Drug Administration, 简称FDA)周二批准该药物意味着日本的大冢制药(Otsuka Pharmaceutical Co.)可以在阿立哌唑(Abilify
凤凰网财经 - FDA,全球,数字药物 - 2017-11-14
基金委与BMGF大挑战合作研究项目批准通知
2016年度国家自然科学基金委员会(NSFC)与美国比尔及梅琳达•盖茨基金会(BMGF)大挑战合作研究项目批准通知 2016年度国家自然科学基金委员会(NSFC)与美国比尔及梅琳达•盖茨基金会(BMGF)大挑战合作研究项目共计受理有效全文申请书9项,经双方各自评审和共同协商,以下4个项目获得批准,项目执行期为4年(2017年1月1日—2020年12月31日)。
国家自然科学基金委员会 - BMGF,基金委 - 2016-09-20
EMA建议批准Vitrakvi治疗NTRK基因融合的实体瘤患者
拜耳公司近日宣布,欧洲药品管理局(EMA)的人用药品委员会(CHMP)建议批准Vitrakvi(larotrectinib)治疗NTRK基因融合的实体瘤患者(包括成人和儿童)。
MedSci原创 - Vitrakvi,NTRK基因融合,实体瘤 - 2019-07-28
FDA批准抗CTLA-4抗体ONC-392的IDN
OncoImmune制药公司近日宣布,其新一代抗CTLA-4抗体ONC-392的研究性新药申请(IND)已获得美国FDA批准。
MedSci原创 - CTLA-4抗体,ONC-392,FDA - 2019-12-31
FDA批准的用于实体瘤治疗的单抗类药物盘点
全球范围内癌症已成为导致人类死亡的最主要病因,并且随着人口的增长及老龄化的出现,发病率日益升高。在所有的治疗措施中,标准治疗方案主要为手术、化疗及放疗。尽管化疗方案效果显著,但该措施缺乏对于肿瘤细胞的选择性,因而容易导致对机体的系统性毒性,以及抗药性的产生。随着人类对于肿瘤细胞分子机理的深入了解,靶向治疗应运而生。绝大多数靶向治疗为容易进入肿瘤细胞的小分子化合物类药物以及特异性结合在靶标蛋白表面的
药智网 - FDA,实体瘤,单抗类药物 - 2017-08-11
美批准确定癌症患者KRAS突变的新检测法
资料图 2012年7月6日,美国食品与药物管理局(FDA)批准了首个帮助一些结直肠癌(CRC)患者确定爱必妥(西妥昔单抗)治疗是否有效的基因检测法。 FDA同时批准了西妥昔单抗新的适应证,即联合5—氟尿嘧啶、亚叶酸和伊立替康(
医学论坛网 - KRAS突变,结直肠癌,西妥昔单抗 - 2012-07-09
阿斯利康甲状腺癌新药Caprelsa获欧盟EMEA批准上市
近日,阿斯利康的治疗甲状腺髓样癌的新药Caprelsa获得欧洲委员会的批准,这种新药是一种口服的激酶抑制剂,是第一个获批的治疗甲状腺髓样癌(medullary thyroid cancer,MTC)的有效的药物
MedSci原创 - 阿斯利康,甲状腺癌,Caprelsa - 2012-02-25
Gabapentin口服液仿制药新药申请获得美FDA批准
Acella医药公司Gabapentin口服液仿制药申请(ANDA)获得美国食品药监局(FDA)批准。 FDA发现Acella仿制药申请的生物等效性上和治疗效果,和推荐药的是一样的。
中国医药123网 - 新药,FDA,Gabapentin - 2012-05-06
FDA批准Esbriet用于治疗特发性肺间质纤维化
10月15日,美国FDA批准了Esbriet(吡非尼酮)用于治疗特发性肺间质纤维化(IPF)。
医学论坛网 - Esbriet,特发性肺间质纤维化 - 2014-10-28
为您找到相关结果约500个