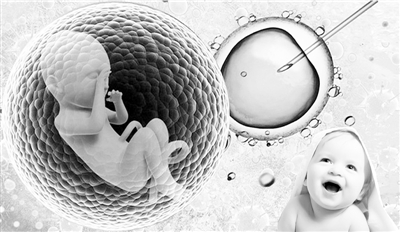
英国“三父母”婴儿技术首获临床试验许可
伦敦当地时间12月15日,英国做出了谨慎而重要的决定——允许“三父母”婴儿出生,成为世界上第一个明确允许开展“线粒体置换疗法”的国家! 英国人工授精与胚胎学管理局(HFEA)在声明中说,经过审慎的评估,该局已认可在一些特定的治疗方案中使用“三父母”技术,那些希望为病人提供这类治疗方案的诊所可以向该局申请许可。不过,它们还要经过一系列非常严格的审批过
科技日报 - 三父母,英国,线粒体 - 2016-12-17
新冠病毒中和抗体临床试验在上海启动
日前,上海君实生物医药科技股份有限公司与中国科学院微生物研究所等单位共同开发的重组全人源抗新冠病毒单克隆抗体注射液(以下简称“JS016”)获得国家药监局批准,进入Ⅰ期临床试验
周琳、仇逸 - 抗体,上海,新冠 - 2020-06-13
药华医药将于ASH年会发表治疗PV新药Proud-PV三期临床试验结果
真性红细胞增生症(PV)是骨髓中造血细胞的一种癌症,主要是红血球细胞和血小板的慢性增加。这种情况可能引发循环系统疾病,如血栓形成和栓塞,甚至恶性转化为骨髓纤维化或白血病。
药华医药股份有限公司 - 白血病,美通社 - 2016-11-29
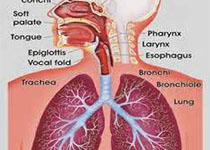
慢性阻塞性肺疾病药物临床试验规范
本规范旨在为慢阻肺治疗药物的临床研究设计、实施和评价提供方法学指导,主要适用于治疗慢阻肺的创新药物临床研究,也可为已上市药品再评价或开发新适应证的药物临床试验所参考。
中华医学杂志.2018.98(4):24 - 慢性阻塞性肺疾病,药物临床试验 - 2018-01-28
总局发布创新药(化学药)Ⅲ期临床试验药学研究信息指南的通告(2018年第48号)
关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号),鼓励研究和创制新药,加快创新药药学研发和审评技术指南标准体系的建立,提高研发和审评质量及效率,国家食品药品监督管理总局组织制定了《创新药(化学药)Ⅲ期临床试验药学研究信息指南
CFDA - 创新药,临床试验 - 2018-03-19
OncoImmune的CD24Fc治疗新冠病毒住院患者的III期临床试验,获得FDA批准
"除了抗病毒治疗外,治疗COVID-19患者的策略还应包括针对组织损伤引起炎症的非抗病毒治疗方法。"
MedSci原创 - III期临床试验,新冠COVID-19,CD24Fc融合蛋白 - 2020-04-09
总局发布医疗器械临床试验设计指导原则
关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号),加强医疗器械产品注册工作的管理,进一步提高注册审查质量,鼓励医疗器械研发创新,国家食品药品监督管理总局组织制定了医疗器械临床试验设计指导原则
新浪医药新闻 - 医疗器械,CFDA,指导原则 - 2018-01-09
FDA送大复方中药连花清瘟的圣诞礼物,在美国开展II期临床试验
12月19日,田院长与孙鹤博士到美国clinical research solutions临床管理中心洽谈Ⅱ期临床事宜 很自信“这是天上掉馅饼吗?明明就是砸了一个砖头!”很多人在得知连花清瘟获IND的消息时“吓了一跳”,认为FDA根本不可能同意13味大复方中药做临床,为这项“不可能的任务”顿感压力巨大。
同写意 - 连花清瘟,FDA - 2015-12-24
助力临床试验公益事业,期待您的加入
近期大家可能经常看到关于梅斯临床试验公益平台的消息呢?大家是不是期待它的上线呢?我们不会让大家期待很久的!1!2!3!梅斯临床试验平台正式上线了!临床试验怎么做公益临床试验患者招募对多数医生来说是陌生又熟悉的,对于一、二城市的三甲医院的医生来说,可能曾经或正在参与某些药企的临床试验,但是对于更对的三、四线的医院医生朋友几乎很少接
MedSci原创 - 2017-07-21
最新临床试验公益事业,期待您的加入!
近期大家可能经常看到关于梅斯临床试验公益平台的消息呢?大家是不是期待它的上线呢?我们不会让大家期待很久的!1!2!3!梅斯临床试验平台正式上线了!临床试验怎么做公益临床试验患者招募对多数医生来说是陌生又熟悉的,对于一、二城市的三甲医院的医生来说,可能曾经或正在参与某些药企的临床试验,但是对于更对的三、四线的医院医生朋友几乎很少接
MedSci原创 - 2017-07-21
Nature:临床试验错误解读 是欺骗还是不懂?
Scott Harkonen 曾经一位制药经理人,也是社会精英,但是目前,他处于软禁状态,且面临着专业除名。其罪行为:歪曲科学数据。但是 Harkonen 本人却对美国最高法院反驳说他自己并没有歪曲任何数据。 前美国药物公司首席官呼吁对结果分析实施欺骗行为进行定罪。 Scott Harkonen 曾经一位制药经理人,也是社会精英,但是目前,他处于软禁状态,且面临着专业除名。其
MedSci原创 - 临床试验 - 2013-12-20
抗肿瘤新药首次人体临床试验申请临床相关资料准备建议
优化临床试验审评审批制度是当前改革重点之一,临床试验方案将成为临床审评重点,内容结构完整的、高质量、可评价的临床试验方案是高效完成审评的保障。抗肿瘤新药是全球创新药研发热点,在当前创新药临床试验申请中大约占40%。然而,现阶段抗肿瘤药物首次
NMPA - 抗肿瘤,新药 - 2018-12-12
确证性临床试验中数据缺失的处理指南
1 前言 确 证性临床试验是在探索性临床试验基础上,通过开展多中心临床试验,进一步确证药物临床疗效,为获得上市许可获得充足证据。该阶段试验通常要求纳入较多的样 本例数,设计随机双盲对照试验,并在此基础上进行数据统计以客观评价新药疗效。然而,受各种因素影响,在确证性临床试验中出现数据缺失是不可避免的,例 如:患者拒绝继续研究、治疗失败/成功或出现不良事件导致退出试验、患者移居,以及观测指标
中国新药杂志 - 临床试验,数据缺失 - 2014-08-09
为您找到相关结果约500个