1. 什么是生物标志物?
生物标志物(Biomarker)是指可以标记系统、器官、组织、细胞及亚细胞结构或功能的改变或可能发生的改变的生化指标。人体内存在多种不同的生物标志物,并且随着分子生物学技术的不断进展,生物标志物包括的种类也越来越多,包括基本身体状况、影像资料(例如乳房X光照片)、特定的分子(例如前列腺特异性抗原PSA)、基因突变(例如BRCA突变)、细胞标记(例如循环肿瘤细胞)以及蛋白质或代谢物等生物分子的生物标志物。
2. Biomarker的研究手段有哪些?
基因组学位于遗传组学上游,能告诉我们机体可能发生哪些变化,但是由于突变、转录调控、基因沉默等,很多遗传信息并不能完全传递到蛋白水平;蛋白质作为生命活动的体现者,更接近生命表征,更能反应机体状态,蛋白质组学位于遗传组学最下游,可以帮助我们了解遗传相关的信息;代谢组学处于微观组学的末端,是基因组学和蛋白质组学的延伸和终端,有助于加深对疾病发生发展机制的理解。因此,在生物标志物研究中,基因组学、蛋白质组学和代谢组学的研究都是非常有意义的。
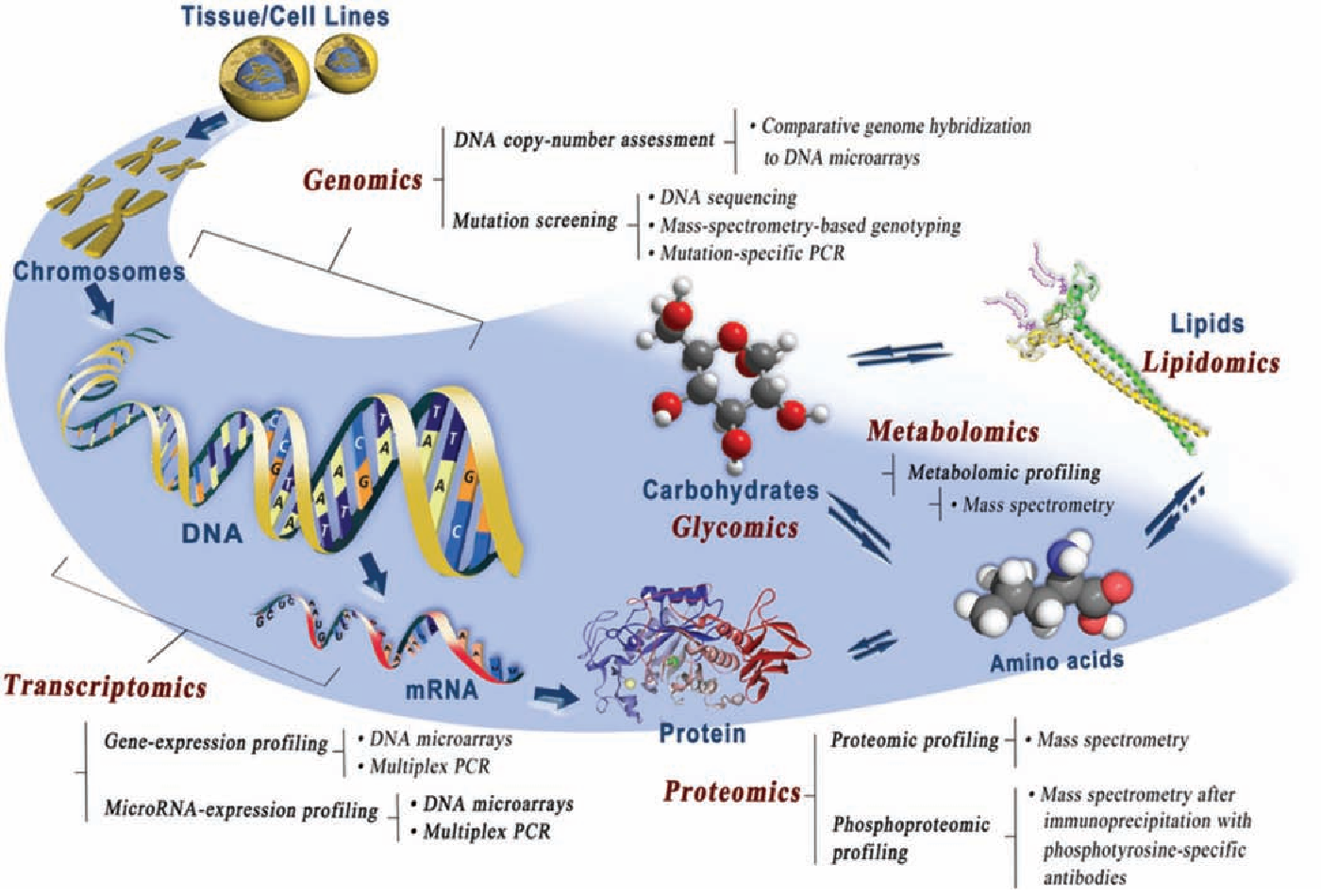
图1 多组学研究手段[1]
3. Biomarker的研究思路是怎样的?
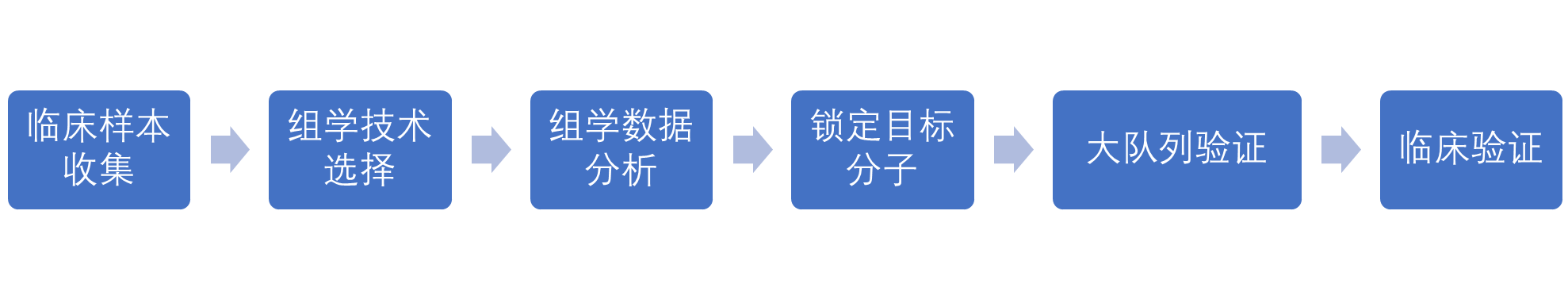
图2 Biomarker研究思路图
(1)临床样本收集
Ø 样本类型的选取:组织和血液为主,以肿瘤为例,建议发现队列选择癌组织样本,疾病特征反映明显;验证队列选择无创、微创的体液样本,如:血清、血浆、尿液等;
Ø 患者信息收集:包括性别、年龄、临床分期、临床病理信息等;
Ø 队列选择:尽量做到多中心、随机采样,进行临床指标的采集与筛选,若有条件可进行随访数据的收集,便于进行预后分析。
Ø 样本数量:发现集建议每组50例以上,验证集则越多越好。
(2)组学技术选择
蛋白质和代谢物都是常见的生物标志物,且两者近年来备受欢迎,CNS级文章屡见不鲜,建议蛋白组学与代谢组学联合研究,筛选更多潜在的生物分子。其中,发现队列应尽可能多的鉴定蛋白/代谢分子,且样本数基本在100例左右,建议选择DIA蛋白质组(蛋白)和非靶向代谢组/脂质组(代谢)。
表1 组学技术及其特征
|
组学技术 |
技术特征 |
|
iTRAQ/TMT蛋白质组 |
重复性好,系统误差小;TMT标记方法最大可以实现16个样本的同时分析,显著提高了分析通量 |
|
Label-free蛋白质组 |
搭配多馏分、长梯度,尽可能多的检测蛋白个数和修饰位点个数,实现常规细胞、组织等样本的蛋白质组学和修饰组学的高深度研究 |
|
DIA蛋白质组 |
适用于各类型生物样本;不依赖信号强度进行母离子的挑选;重复性好,蛋白质覆盖率高,定量准确性高,适用于大样本 |
|
非靶向代谢组/脂质组 |
无偏向性,高通量,检测更多的代谢物,样本无需特殊处理且一次进样分析 |
|
类靶向代谢组 |
综合非靶向代谢组学高通量优点与靶向代谢组学高准确度、高灵敏度优点的一种新型代谢组检测技术 |
(3)组学数据分析
Ø 标准分析:主要包括质控分析、注释分析、定量分析、差异分析等
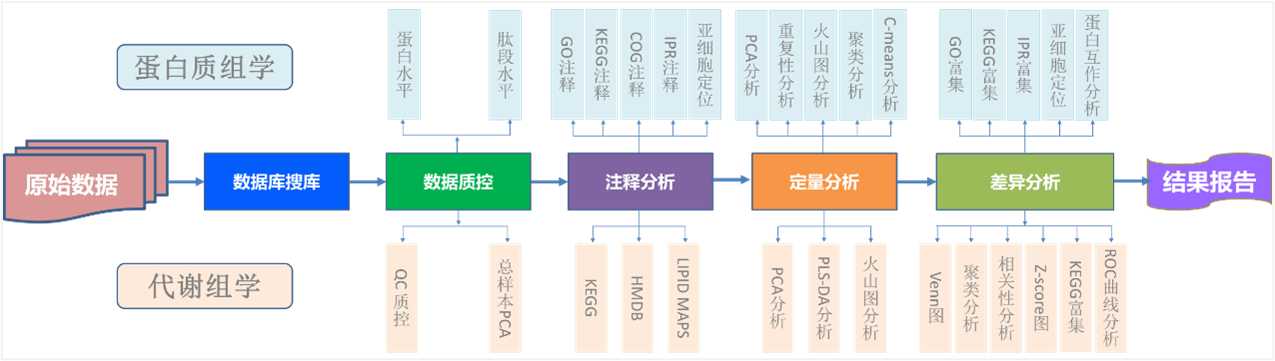
图3 组学数据标准分析流程
(4)锁定目标分子
Ø 高级分析:个性化挖掘深层次的分子机理,锁定关键蛋白质/代谢物分子,是提升文章层次,揭示新机制,锁定目标分子的必备技能。
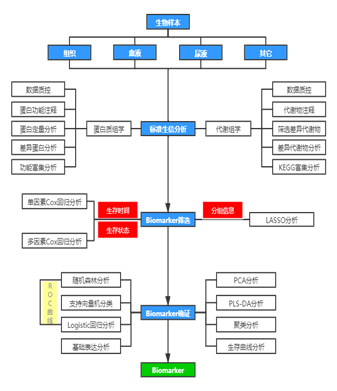
图4 组学数据高级分析流程
(5)大队列验证
Ø 表达水平验证:为确定锁定的目标分子的真实性和可靠性,可在细胞水平、动物水平进行表达水平验证,常见的技术方法包括:RT-PCR、Western Blot、ELISA和靶向质谱(PRM)等;
Ø 队列验证:训练集直接参与了模型调参的过程,显然不能用来反映模型真实的能力,所以需要测试集来考察模型真正的能力。通过发现队列锁定目标分子后,需要重新募集队列验证发现队列筛选到的biomarker是否准确可靠。
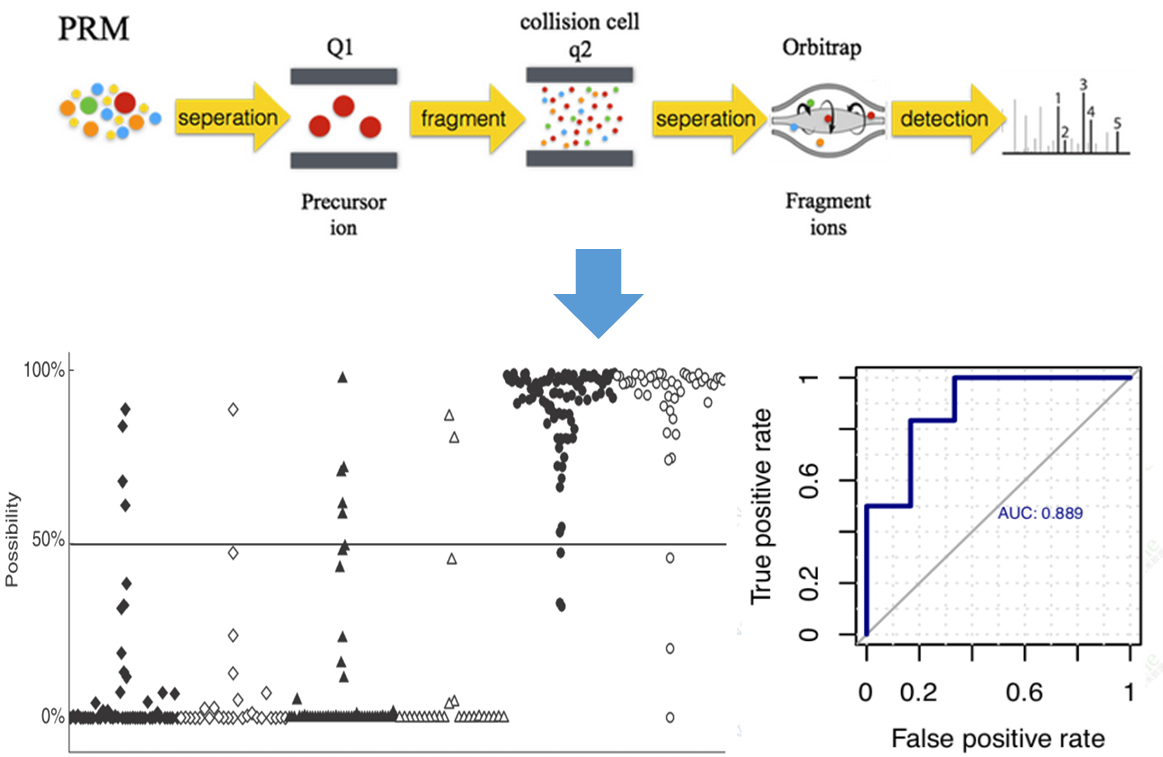
图5 PRM验证及其结果展示
(6)临床验证
指导临床是生物标志物筛选的最终目标,因此需要进行临床诊断、药效评价、新药/新疗法在目标人群的安全性及有效性评估等一系列验证。
4. 有哪些Biomarker研究的案例?
案例1:非小细胞肺癌治疗效果的潜在生物标志物[2]

2021年2月,北京大学肿瘤医院王子平主任团队和方健主任团队于肺癌转化领域知名期刊Translational Lung Cancer Research在线发表题为Identification of serum biomarkers to predict pemetrexed/platinum chemotherapy efficacy for advanced lung adenocarcinoma patients by data-independent acquisition (DIA) mass spectrometry analysis with parallel reaction monitoring (PRM) verification的文章。通过DIA定量蛋白质组学技术分析了接受培美曲塞/铂类化疗的晚期肺腺癌患者的20份血清样本,共鉴定出23种显著差异的蛋白质;接着利用PRM靶向蛋白质组学技术在一个新队列中进行验证,获得了10种潜在的预后生物标志物,这些潜在的生物标志物可能对预测培美曲塞/铂类化疗疗效具有重要意义。该研究的DIA+PRM蛋白质组学服务由诺禾致源提供。

图6 案例1研究思路图
案例2:慢加急性肝衰竭精准诊断蛋白标志物[3]

2019年1月,浙江大学医学院附属第一医院李兰娟院士团队于 Theranostics 在线发表文章 Circulating proteomic panels for diagnosis and risk stratification of acute-on-chronic liver failure in patients with viral hepatitis B,该文章通过定量蛋白质组学技术从血浆样本中广筛到了部分 ACLF 相关差异蛋白,作为候选生物标志物;随后,联用PRM靶向蛋白质组学 在更大规模样本上进行了验证;最后成功建立了两个模型,分别用于 ACLF 的临床诊断和预后分析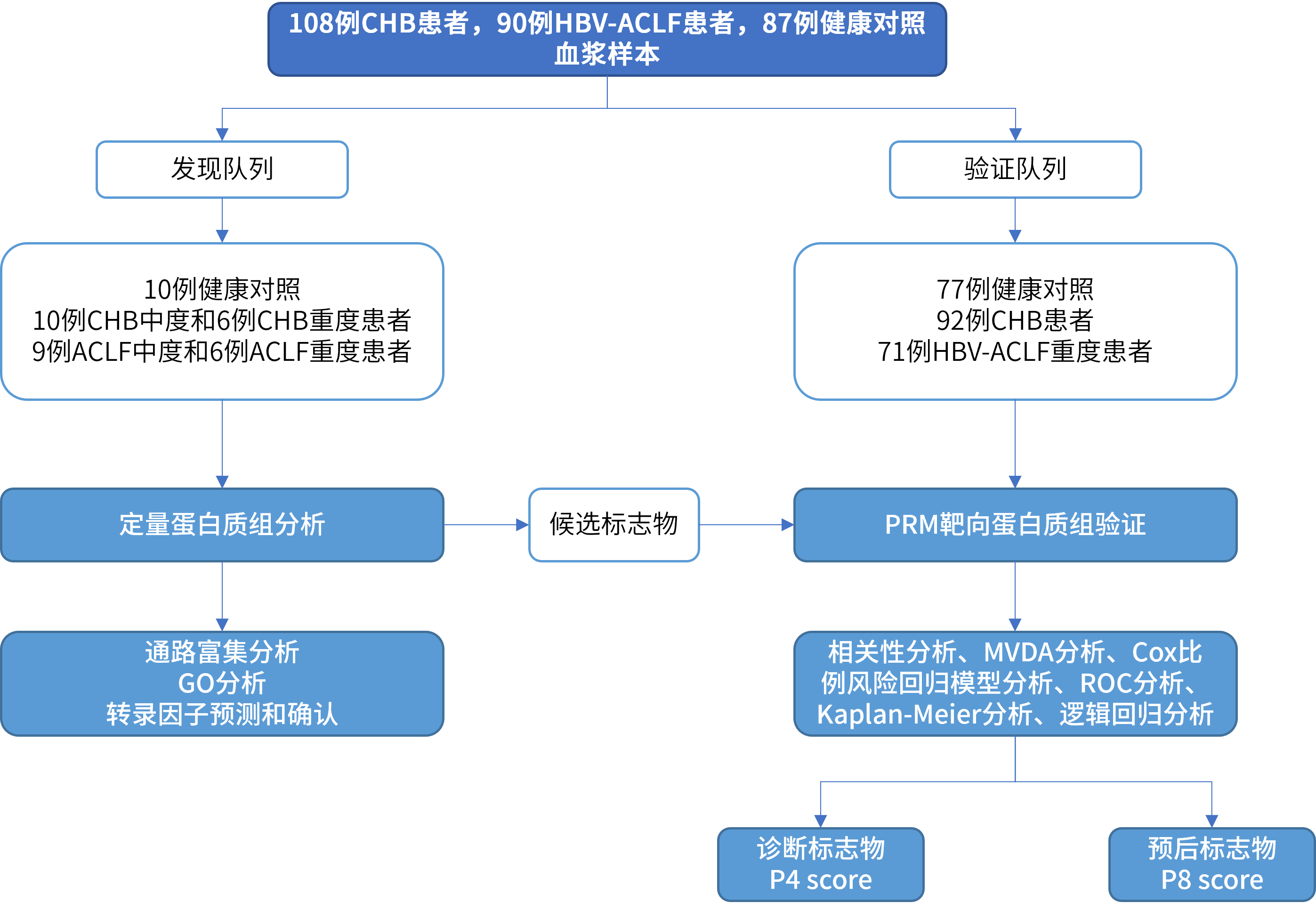
图7 案例2研究思路图
5. 诺禾致源的Biomarker解决方案
采用QTRAP® 6500+、Q Exactive™ HF-X、Obitrap Exploris™480及timsTOF Pro2等技术平台,获取可靠的组学数据;拥有强大的生信分析团队,深度挖掘数据,助力biomarker筛选与验证,为医疗工作者提供一站式解决方案。

图8 (a) QTRAP® 6500+ ;(b) Q Exactive™ HF-X ;
(c) Obitrap Exploris™480;(d)timsTOF Pro2
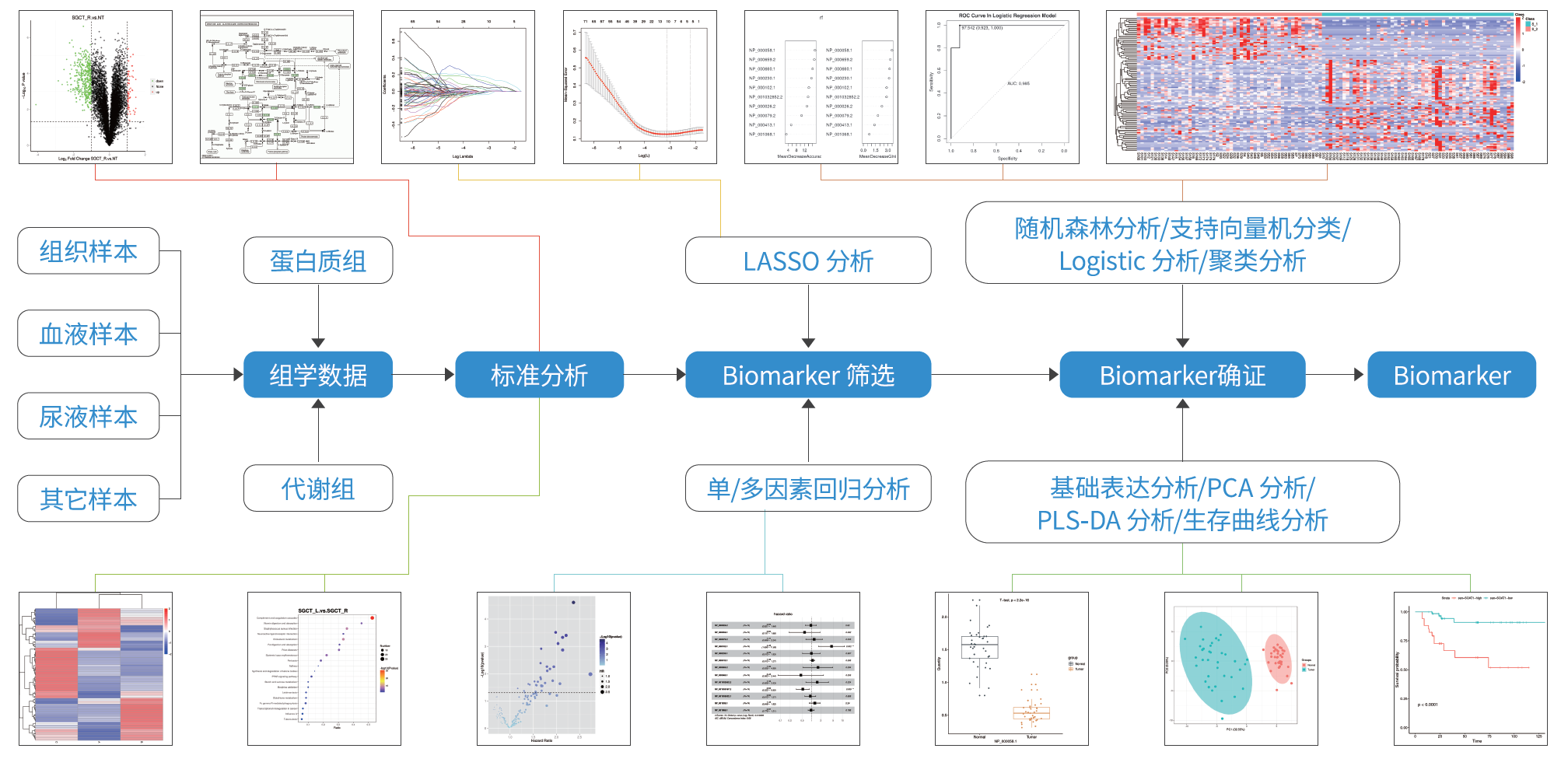
图9 诺禾致源生物标志物分析流程
更多实用内容请关注“诺禾致源质谱”微信公众号

参考文献:
[1] Wu R Q , Zhao X F , Wang Z Y , et al. Novel molecular events in oral carcinogenesis via integrative approaches.[J]. Journal of Dental Research, 2011, 90(5):561.
[2] Jia B, Zhao X, Wu D, et al. Identification of serum biomarkers to predict pemetrexed/platinum chemotherapy efficacy for advanced lung adenocarcinoma patients by data-independent acquisition (DIA) mass spectrometry analysis with parallel reaction monitoring (PRM) verification.[J]. Translational Lung Cancer Research, 2021(2).
[3] Zeyu, Sun, Xiaoli, et al. Circulating proteomic panels for diagnosis and risk stratification of acute-on-chronic liver failure in patients with viral hepatitis B.[J]. Theranostics, 2019.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#标志物#
47
#生物标志物#
73
#生物标志#
51
#生物标志#
44
基础研究推动临床
55