Nature Cancer:世界首次,通过实体瘤癌症患者来源的类器官,筛选到临床候选药物
2022-05-23 王聪 “生物世界”公众号
近年来,类器官领域研究成果不断,许多新型类器官和更复杂的类器官不断涌现,为新药研发、精准治疗、再生医学等领域带来了更强大的工具。由癌症患者样本培养而来的类器官,有助于在临床治疗中为患者提供最佳治疗策略
2009年,Hans Clevers 等人使用来自小鼠肠道的成体干细胞培育出首个肠道类器官,开创了类器官研究的时代。2013年,类器官被 Science 评为年度十大科学技术,Hans Clevers 也因类器官领域的开创性研究获得了2013年科学突破奖(Breakthrough Prize)。
近年来,类器官领域研究成果不断,许多新型类器官和更复杂的类器官不断涌现,为新药研发、精准治疗、再生医学等领域带来了更强大的工具。由癌症患者样本培养而来的类器官,有助于在临床治疗中为患者提供最佳治疗策略。
2022年4月25日,冠科生物、Merus公司和巴塞罗那科学技术研究院的研究人员合作,在 Nature 子刊 Nature Cancer 发表了题为:Functional patient-derived organoid screenings identify MCLA-158 as a therapeutic EGFR × LGR5 bispecific antibody with efficacy in epithelial tumors 的研究论文。
该研究首次使用来自癌症患者的类器官库对500多个双特异性抗体进行筛选,从中发现了名为 MCLA-158 的 EGFR × LGR5 双特性抗体,能够有效抑制结直肠癌类器官的生长,并防治转移的发生。该研究为医药公司使用类器官进行药物发现奠定了基础。

2021年10月,Merus 公司报告了其开发的名为 MCLA-158 的 EGFR × LGR5 双特性抗体治疗晚期头颈部鳞状细胞癌(HNSCC)的中期临床试验的安全性、耐受性和抗肿瘤活性,7名患者中3名出现了部分缓解,其中1名实现了完全缓解,7名患者均观察到肿瘤缩小。
MCLA-158(Petosemtamab),是一种双特异性抗体,可识别癌症干细胞表面的两种蛋白——EGFR 和 LGR5,EGFR 促进细胞不受控生长,而 LGR5 则是负责癌症扩散的肿瘤干细胞表面的标志物。
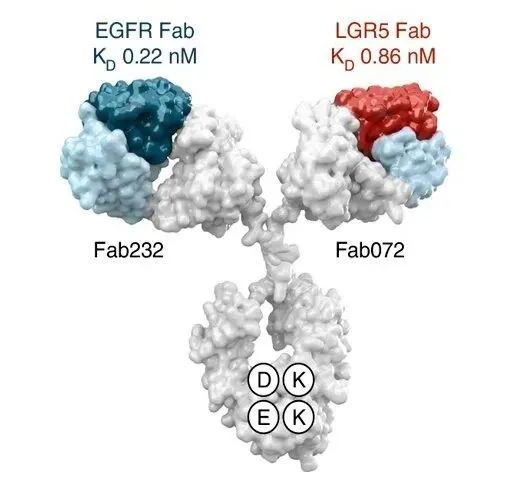
MCLA-158 能够抑制具有 LGR5 标志物的癌症干细胞中的 EGFR 蛋白,从而阻断引起癌症扩散的肿瘤干细胞的生长和存活。而且这种双特异性抗体不会影响健康干细胞的功能。
之前的研究显示,MCLA-158 能够抑制头颈部肿瘤、食道肿瘤和胃肿瘤的临床前肿瘤模型的生产,还能抑制结直肠癌类器官的生长和转移。
为了进一步开发和表征该双特异性抗体,HUB Organoids(由类器官的开创者Hans Clevers创建)的研究人员建立了一个大型类器官库,包括来自结直肠癌患者的类器官、来自结直肠癌转移到肝脏的类器官以及来自正常非癌组织的类器官。OcellO 公司(被冠科生物收购)的科学家对这一类器官库进行了高通量筛选。
在药物开发的早期阶段,使用来自患者肿瘤组织类器官,有助于识别对患者有效的,甚至是对携带特定突变肿瘤有效的治疗性药物。而使用来自健康组织的类器官,可以识别对器官产生不良作用的药物,评估药物的有害影响,从而在研究初期撤回毒性作用更大的药物。
在这项研究中,研究团队在结直肠癌患者来源的类器官和健康结肠粘膜来源的类器官进行高通量筛选,从500多种双特异性抗体中发现了 MCLA-158。MCLA-158 能够特异性触发 LGR5 阳性癌症干细胞中的 EGFR 蛋白降解,而对 LGR5 阳性健康结肠干细胞的毒性很小。
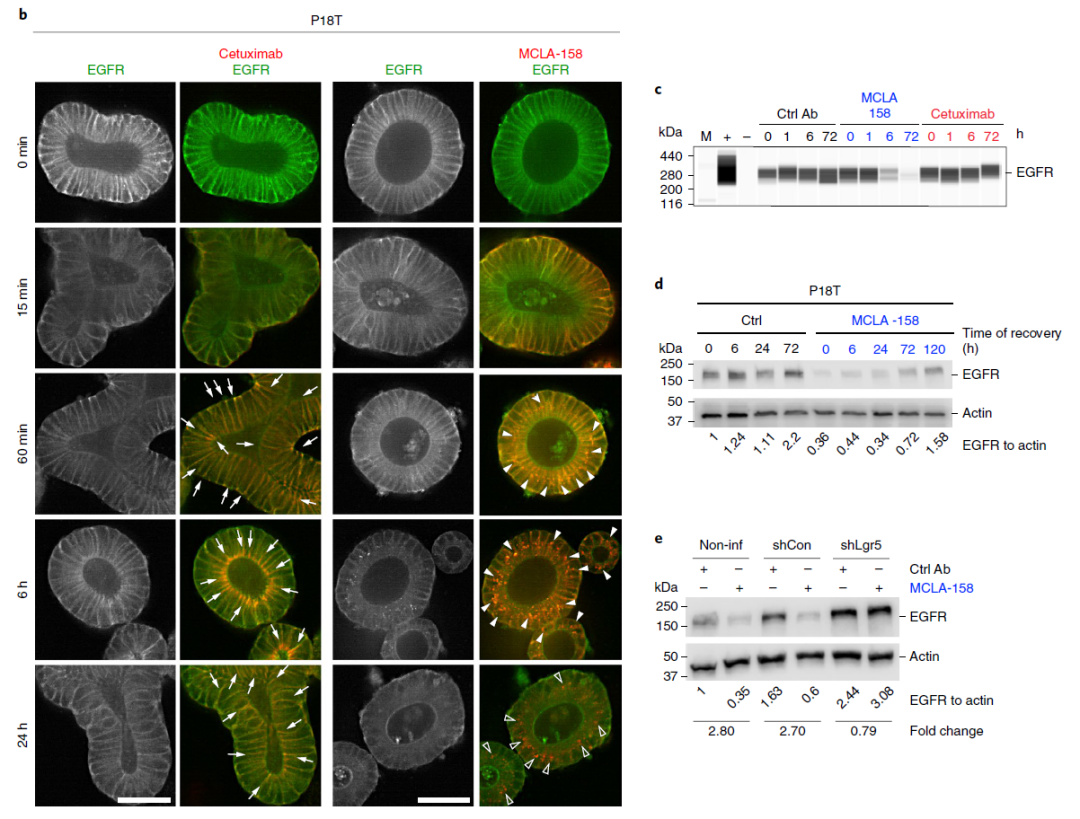
MCLA-158 在几种上皮癌类型的临床前模型中表现出治疗特性,例如 KRAS 突变型结直肠癌的生长抑制、转移起始的阻断和肿瘤生长的抑制。
这也是首次在实体瘤类器官中筛选到临床候选药物,为基于类器官的药物发现奠定了基础。
原始出处:
Goto, N., Yilmaz,et al. Bispecific antibodies seek out colon cancer stem cells. Nat Cancer 3, 379–380 (2022). https://doi.org/10.1038/s43018-022-00368-z.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#候选药物#
57
#Nat#
42
#癌症患者#
46
#筛选#
47
#类器官##胃癌#
117