聚焦2022WCLC,带你从奥希耐药进展中窥探靶向治疗行业前沿发展
2022-08-14 找药宝典 找药宝典
病理类型转化是奥希替尼耐药的原因之一。而对于此类人群,治疗方案上需联合EP这样的小细胞肺癌化疗方案,患者群中碰到过多次这样的患者,对症用药后效果不错。
“耐药”这件事就像是悬在所有患者头顶的一柄达摩克利斯之剑,是一柄高悬头顶的危险利刃,不知何时会落下。如果一直不耐药,那疗效固然好,患者得到的缓解就可以长期地维持下去,甚至生活如常人;而一旦耐药,病灶就会再次开始迅速地生长,癌症卷土重来。
2022年IASLC世界肺癌大会(WCLC)于近日在奥地利首都维也纳展览会议中心盛大举行。关于如何克服患者EGFR-TKI耐药,此次WCLC大会也给出了最新进展报道~小编特汇,希望对您能有所帮助。

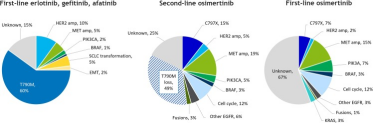
既往研究发现,不同线数下使用奥希替尼,耐药的机制虽然整体相似,但二线耐药相对更复杂。
一线和二线都有相似的主要耐药机制,即MET扩增和C797S。
一线奥希替尼耐药后不会出现T790M的继发突变。
二线奥希替尼耐药的继发基因改变,无论是EGFR原位的或其他基因的旁路激活,类型都更复杂一些,甚至多种同时存在。
二线奥希替尼耐药后可能会出现向小细胞肺癌和肺鳞癌转化的可能,发生率在4%左右。
01
进展一:EGFR C797X突变揭秘耐药机制
酪氨酸激酶抑制剂 (TKI) 是表皮生长因子受体 ( EGFR ) 突变的非小细胞肺癌 (NSCLC) 患者的标准治疗方案) 基因,一线治疗通常是第三代 EGFR TKI 奥希替尼。因此奥希替尼耐药问题不可避免,EGFR C797X突变是主要机制之一。研究人员利用Guardant INFORM真实世界临床基因组数据库评估EGFR C797X和其他耐药驱动因子在EGFR突变NSCLC中的真实世界检出率和生物标志物共存情况。
在71,430例NSCLC患者中,9,306例有EGFR外显子19缺失或L858R,其中1337例和713例分别接受奥希替尼一线和二线治疗。开始奥希替尼一线治疗后5年,MET和CCNE1扩增与EGFR C797X突变的累积发生率为6.4%、7.9%、8.0%,38个月后EGFR C797X突变累积发生率超过MET和CCNE1扩增。开始奥希替尼二线治疗后5年,MET和CCNE1扩增与EGFR C797X突变的累积发生率分别为7.2%、10.3%和17.5%,19个月后EGFR C797X突变累积发生率超过MET和CCNE1扩增。在对G360后一个月内停用奥希替尼的患者(代表疾病进展)进行的亚组分析中,C797X的累积发生率较高。
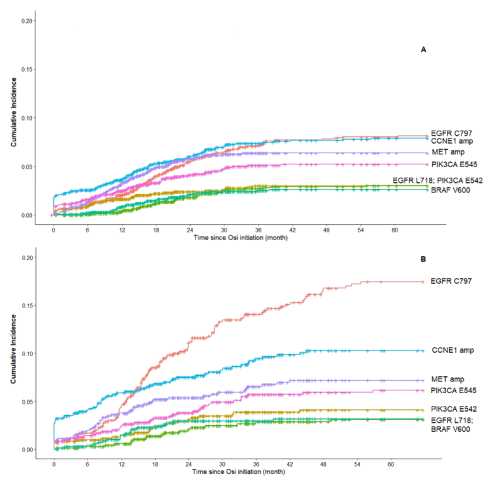
Osimertinib治疗开始后常见获得性耐药突变的累积发生率:(A)一线(n=1337)和(B) 二线(n=713)
研究表明:EGFR C797X是一线和二线奥希替尼治疗后最常见的获得性靶内或脱靶耐药突变,分别为8.0%和17.5%,超过了奥希替尼使用第一年后MET和CCNE1的早期脱靶扩增。研究结果表明,需继续开发下一代EGFR-TKI以应对EGFR突变NSCLC患者C797X驱动的耐药性。
02
进展二:Amivantamab+拉泽替尼/铂类化疗,ORR可观!
铂类化疗是目前Osimertinib(奥希替尼)治疗后疾病进展的非小细胞肺癌 (NSCLC) 患者的标准治疗。然而,奥希替尼复发性疾病可能仍然对EGFR和/或MET抑制敏感,铂类化疗与Amivantamab和拉泽替尼靶向抑制EGFR/MET信号传导作用相结合,会改善EGFR酪氨酸激酶抑制剂(TKI)复发性/难治性疾病,产生较高的总缓解率!
CHRYSALIS-2研究入组了EGFR TKI作为末线治疗(最多三线既往治疗)期间或治疗后疾病进展的EGFR突变NSCLC患者。患者接受1400mg(体重≥80kg时为1750mg)静脉给药,前4次每周一次(21天为1个周期)给药(首次给药分次进行),直至第2周期第1天,此后接受1750mg(体重≥80kg时为2100mg)静脉给药,每3周一次,联合240mg口服拉泽替尼每日一次,和500mg/m2培美曲塞加卡铂(AUC5),4个周期后停止卡铂治疗。
结果显示:在随访3个月时,最佳缓解包括10例确认部分缓解的患者、7例疾病稳定的患者和3例疾病进展的患者。最常见治疗中出现的不良事件为输液反应(73.3%)、中性粒细胞减少症(66.7%)、皮疹(46.7%)、血小板减少症(40.0%)、疲乏和恶心(各33.3%)。在中止治疗的5例受试者中,2例因化疗相关严重不良事件,3例因疾病进展。
03
进展三:奥希替尼联合HER2/EGFR抑制剂,初显疗效!
在一线厄洛替尼或吉非替尼后进展的肿瘤中,约有 10% 观察到 HER2 扩增;在 osimertinib 耐药之后,情况就不那么好了。此外,HER2突变是 NSCLC 中的致癌驱动因素。因此,HER2-扩增和/或-突变被靶向治疗EGFR-TKI耐药的EGFRm NSCLC。
该项单组、多中心、开放性Ib/II期研究,旨在探索奥希替尼、耐昔妥珠单抗和曲妥珠单抗(ONT)联合用药在经组织学证实奥希替尼治疗后进展的携带激活和致敏EGFR突变的转移性成人NSCLC患者的II期试验推荐剂量(RP2D)、安全性、耐受性和初步疗效。
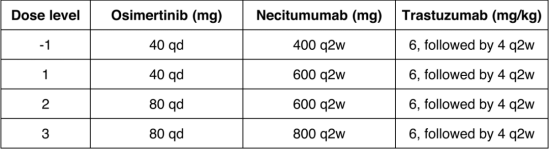
根据RECIST 1.1标准通过客观缓解率(ORR)评估疗效。分析包括接受至少一剂研究治疗的所有患者。
结果显示:在所有受试者中,在任何剂量下观察到的最常见不良事件(不考虑因果关系和级别)包括痤疮样皮疹(73%)、头痛(55%)、恶心(45%)、皮肤干燥(36%)、腹泻(27%)、疲乏(27%)、口腔黏膜炎(27%)和呕吐(27%)。3级治疗相关毒性为痤疮样皮疹 (36%)、腹泻 (9%) 和高血压(9%)。未发生4级或5级不良事件或治疗相关死亡。达到部分缓解或疾病稳定的可评价受试者比例为62.5%(5/8)。1例EGFR p.L861Q突变受试者达到部分缓解(肿瘤缩小56%,持续5.5个月)。
目前,EGFR+最新的药物就是三代“明星”靶向药奥希替尼,虽然让很多肺癌患者成功“续命”,但是也难逃“耐药”的宿命。这时候,四代EGFR抑制剂就成了“众望所归”。
04
进展四:JIN-A02 第四代高效EGFR-TKI,靶向NSCLC三重突变
JIN-A02 是一种靶向 C7JIN-A02 97S 突变的新型、可口服、第四代 EGFR 酪氨酸激酶抑制剂 (TKI),并在双突变或三突变EGFR(ex19del / T790M或ex19del / T790M / C797S)的临床前模型中表现出强效的抗肿瘤活性。
JIN-A02 在 PDC 模型中表现出显著疗效。在携带 EGFR ex19del / T790M / C797S 突变的 PDC YU-1097 细胞中,JIN-A02对 EGFR ex19del / T790M / C797S 的抑制作用强于奥希替尼,而在 EGFR WT A549 细胞中,EGFR WT活性在很大程度上保持不变,在 YU-1097 PDC 异种移植模型中,肿瘤显著消退,而用奥希替尼(25 mg/kg,每日一次)处理的小鼠的肿瘤生长未受影响 (TGI = 51.7%)。在 10 mg/kg 和 50 mg/kg 剂量下观察到抗肿瘤疗效,且呈剂量依赖性。在所有给药组中均未观察到显著毒性。
这些临床前研究证明,JIN-A02是第四代 EGFR TKI 中具有高效和选择性的潜在最佳药物。JIN-A02 对 EGFR C797S 突变(包括单突变和双突变)表现出强大的活性。它对 L718Q 也有效,目前尚无替代治疗。JIN-A02 有望为既往 EGFR TKI 治疗后进展的患者提供治疗机会,未来计划进行首次人体试验,检测临床疗效和安全性。
05
进展五:BBT-176,首次人体数据公布
在一项开放标签1/2期试验 (NCT04820023) 中,研究人员正在研究 BBT-176 在接受 EGFR 酪氨酸激酶抑制剂治疗后进展的晚期或转移性 IIIB/IV 期 NSCLC 患者中的疗效、耐受性和安全性。根据此前公布的初步报告,使用160毫克剂量的BBT-176进行治疗,一名患者达到了临床缓解,肿瘤缩小了51%;在310剂量下,一名患者肿瘤缩小了30%。当前的安全性试验结果提示,BBT-176治疗的不良事件均在1~3级,安全性良好。
在本次大会中:此项实验有了最新进展,截至2022年03月10日,共有18例患者接受了 BBT-176 治疗。在5例患者的血液中检测到三重突变 EGFR 基因(外显子 19 del / T790M / C797S 或L858R / T790M / C797S)。2例携带外显子 19缺失 / T790M / C797S 三重突变的患者显示靶病灶和非靶病变中均表现出放射学改善。
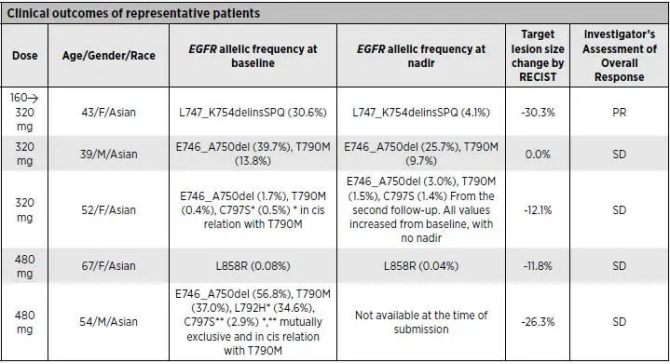
以上结果表明BBT-176连续每日给药的耐受性良好,毒性可管理。通过对患者进行分子选择和液体活检的动态监测,BBT-176的有效性可能进一步增强。
EGFR四代药带给无数患者新的曙光,但是目前为止,FDA 尚未批准任何一款新的靶向药针对奥西替尼耐药患者,从临床研究到药物的正式获批还需要漫长的等待。那么已经奥希替尼耐药的患者首先可根据疾病进展的状态,进行针对性的处理。
一、缓慢进展,可以继续用奥希替尼,配合局部治疗
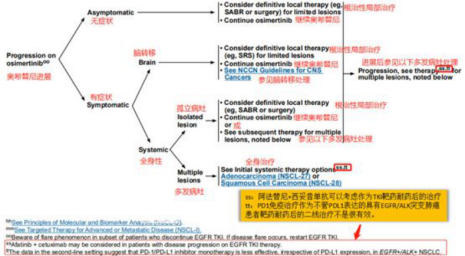
研究显示,奥希替尼初次耐药患者大多数为孤立性进展,这些患者继续服用9291,配合上局部治疗,还能获益。因此,对于无症状、影像学进展缓慢的耐药患者,可以先不着急换药。NCCN指南推荐以下三种情况患者可以考虑根治性局部治疗(如立体定向放疗或手术),同时继续使用奥希替尼:①无症状进展;
②有症状的脑转移(配合脑转移处理,如全脑放疗、培美曲赛、替莫唑胺、鞘内注射等);③有症状的全身性(颅外)孤立性病灶(转移灶<3-5个)。
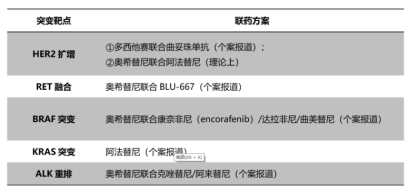
二、基因检测,找出耐药突变,针对性给予靶向联合治疗
如果奥希替尼使用后,机体出现快速进展的情况,请迅速进行基因检测,根据突变情况进行针对性的靶向治疗。
1. C797S单发突变,使用一代EGFR靶向药物一线使用奥希替尼,耐药后一般不会出现T790M的突变,但会发现C797S的单发突变,因为奥希替尼尽早使用是能够抑制T790M突变产生的,也会避开T790M与其他突变的共存。这一位点的突变对一代吉非替尼或厄洛替尼都比较敏感,临床处理相对容易。
2.C797S与T790M的顺式突变,目前仍在研
3.C797S与T790M的反式突变,1代+3代EGFR靶向药物
4. 继发MET扩增,EGFR抑制剂+MET抑制剂
5. 其他靶点的继发性突变
6. 继发EGFR点突变:可用回1/2代EGFR靶向药
三、基因检测后,无可针对的耐药靶点出现,可选用新联合方案或安罗替尼
1. 先转归化疗,灵活用药,可穿插或尝试再挑战奥希替尼
2. 安罗替尼
3. 免疫治疗不做常规推荐,可联合化疗或筛选适用人群
4. 阿法替尼+西妥昔单抗
NCCN指南推荐,阿法替尼联合西妥昔单抗可以作为EGFR耐药的处理方案。
5. 奥希替尼加量:
一般从80mg/天→160mg/天适用于无可针对新靶点,通过增加体内药物浓度杀伤肿瘤,特别是脑软膜转移的患者。BLOOM试验纳入了21例EGFR19/21突变的软脑膜转移患者(既往中位治疗线数=3,都用过EGFR靶药),使用奥希替尼160mg/天治疗。其中T790M突变共8例。结果显示,经确认的软脑膜ORR为33.33%,DCR达到76.19%。这里举一个案例。下图A及B为奥希替尼增量(80mg→160mg)前后脑软膜的病灶变化,加大剂量后病灶疗效达到部分缓解PR。
6.“脉冲式”特罗凯:
短时间内大剂量给药,临床无统一的给药剂量方案。NCCN指南推荐“脉冲式”特罗凯治疗EGFR脑软膜转移患者
四、新靶点药
1.U3-1402(HER3靶向药)
一项I期临床研究,评估晚期EGFR突变NSCLC患者在EGFR-TKIs奥希替尼治疗和铂类化疗失败后使用HER3抑制剂U3-1402(patritumab-deruxtecan,5.6 mg/kg)治疗的安全性和有效性。中位治疗时间为3.5个月,中位随访时间为5个月,55%的患者仍然在继续治疗,疗效图瀑布图如下所示:一例患者达到CR,13例患者确认为PR,3例PR患者待确认。
五、靶向药轮换(民间做法,不做强推荐)
在奥希替尼耐药后,民间还有多个靶向药之间的切换使用方法,通过对不同耐药机制细胞群的轮替杀伤,达到压制肿瘤进展的作用。然而,这种方案未得到临床试验的数据支持,故不做推荐。
六、转化小细胞肺癌的治疗:除转归化疗,案例用奥希替尼轮换治疗亦见效
病理类型转化是奥希替尼耐药的原因之一。而对于此类人群,治疗方案上需联合EP这样的小细胞肺癌化疗方案,患者群中碰到过多次这样的患者,对症用药后效果不错。
声明:本资料中涉及的信息仅供参考,请遵从医生或其他医疗卫生专业人士的意见或指导。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#WCLC#
53