Cell:揭示细菌抑制宿主细胞干扰素反应机制
2022-05-23 生物谷 生物谷
许多病毒---包括SARS-CoV2---已经进化出抑制正常干扰素功能的蛋白来感染我们并在人群中传播,但是细菌病原体是否逃避干扰素反应仍不清楚。
细菌感染,如志贺氏菌引起的痢疾,每年造成数百万人死亡,但是这些细菌是否也能干扰身体对抗感染的能力,以前并不清楚。
在一项新的研究中,来自伦敦国王学院的研究人员阐明了细菌阻止宿主细胞识别即将发生的感染的分子过程。相关研究结果于2022年5月13日在线发表在Cell期刊上,论文标题为“A family of conserved bacterial virulence factors dampens interferon responses by blocking calcium signaling”。

在感染期间,构成我们身体第一道防线的细胞会释放“干扰素”。干扰素诱导一种抗菌状态,保护组织免受感染。干扰素提醒邻近的细胞,使它们准备好抵御即将到来的感染。许多病毒---包括SARS-CoV2---已经进化出抑制正常干扰素功能的蛋白来感染我们并在人群中传播,但是细菌病原体是否逃避干扰素反应仍不清楚。
这些作者证明了志贺氏菌III型分泌效应物OspC蛋白家族阻断干扰素信号传导,并且与它的细胞死亡抑制活性无关。相反,干扰素抑制是通过志贺氏菌OspC1和OspC3与钙离子传感蛋白钙调蛋白(calmodulin, CaM)的结合进而阻断CaM激酶II和下游的JAK/STAT信号传导来实现的。缺乏OspC1和OspC3的志贺氏菌在上皮细胞和小鼠感染模型中的生长减弱了。在这两种情形下,这种表型可通过剔除干扰素受体而得到拯救。在其他病原体中保守的OspC同源物不仅结合CaM,而且还抑制干扰素,这表明是一种广泛的毒力策略。这些发现揭示了一种保守的但以前未描述的干扰素抑制的分子机制,并证实了钙离子和干扰素靶向在细菌致病机制中起着关键作用。
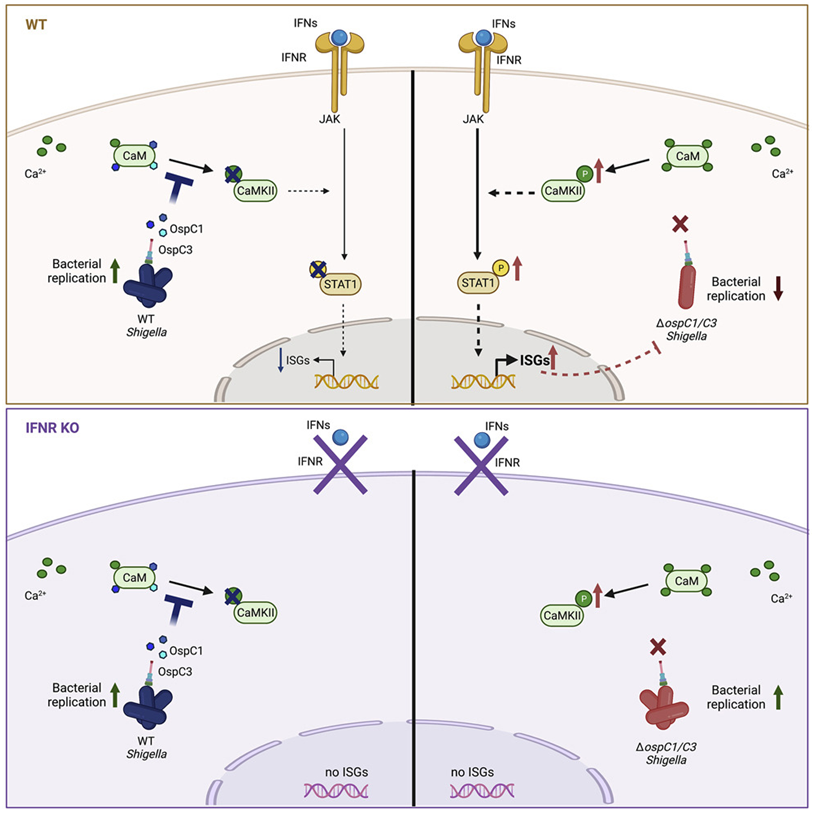
图片来自Cell, 2022, doi:10.1016/j.cell.2022.04.028
这是一种新发现的策略,通过破解宿主的钙离子信号来欺骗我们的免疫系统,阻止我们对这种细菌感染产生有效的免疫反应。
论文通讯作者、伦敦国王学院的Charlotte Odendall博士说,“这项新的研究是另一个完美的例子,说明研究病原体不仅可以更好地了解感染过程,而且还可以揭示宿主对感染反应的复杂性。”
这些作者认为,这些观察结果可能为开发针对细菌感染的新疗法打开大门。
参考资料:
1. Noémie Alphonse et al. A family of conserved bacterial virulence factors dampens interferon responses by blocking calcium signaling. Cell, 2022, doi:10.1016/j.cell.2022.04.028.
2. Bacteria that cause dysentery also actively block body's ability to fight the infection.
https://medicalxpress.com/news/2022-05-bacteria-dysentery-block-body-ability.html.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#CEL#
33
#Cell#
45
#干扰素#
51
#宿主#
46