Lancet:NALIRIFOX联合白蛋白结合紫杉醇和吉西他滨治疗初治转移性胰腺导管腺癌(NAPOLI3):一项随机、开放标签的3期临床试验
2023-10-07 daikun MedSci原创 发表于上海
该研究旨在评估NALIRIFOX联合白蛋白结合紫杉醇和吉西他滨治疗初治转移性胰腺导管腺癌(NAPOLI3)的疗效和安全性,研究结果支持使用NALIRIFOX方案作为mPDAC一线治疗的可能参考方案。
胰腺导管腺癌仍然是最致命的恶性肿瘤之一,对于诊断为转移性疾病的患者,估计5年生存率仅为3%。在过去的十年中,两种联合化疗方案,氟尿嘧啶,亚叶酸钙,伊立替康和奥沙利铂(FOLFIRINOX)的四联体以及nab-紫杉醇和吉西他滨的双重方案已成为一线标准治疗方案。然而,这些方案从未被直接比较过,因此对最佳治疗方案存在不确定性。除了微卫星不稳定性高的胰腺癌外,免疫检查点抑制剂仅显示出部分益处,尽管人们对使用基因组分析来改善预后非常感兴趣,但相对较少的患者有资格接受分子靶向药物。大多数患者预后不良,治疗选择数量少,这突出表明需要进一步研究,以比较有效和可耐受的新治疗方法,并最大限度地发挥细胞毒性化疗方案的益处。NAPOLI3研究旨在比较NALIRIFOX与白蛋白结合的紫杉醇和吉西他滨作为转移性胰腺导管腺癌(mPDAC)一线治疗的疗效和安全性。
伊立替康是一种拓扑异构酶I抑制剂,主要通过其活性代谢物SN-38起作用。脂质体伊立替康是一种脂质体制剂,将伊立替康包封在脂质双层囊泡中。包封使伊立替康在转化为SN-38之前比未包封(游离)伊立替康保持循环的时间更长。因此,在同等剂量下,相对于游离伊立替康,脂质体伊立替康显示出更高且持续的伊立替康和SN-38肿瘤内水平。来自难治性晚期实体瘤患者(n=13)脂质体伊立替康的初步研究数据显示,给药后72小时,肿瘤活检样本中SN-38水平比血浆中SN-38水平高5倍,表明伊立替康对SN-38的局部代谢激活。

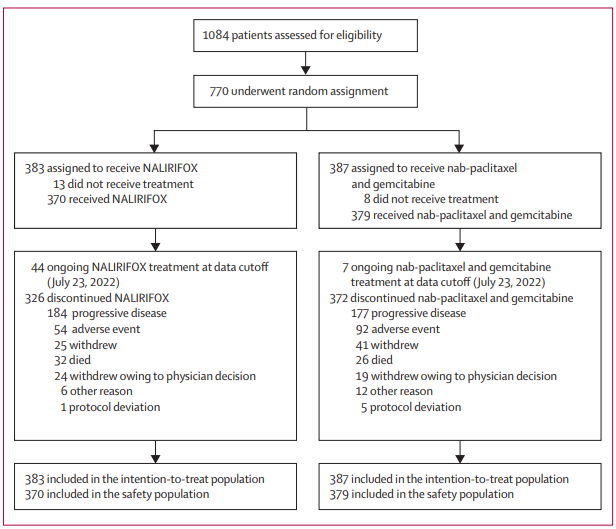
方法:NAPOLI3是一项在欧洲、南北美洲、亚洲和澳大利亚187个国家的18个社区和学术机构进行的随机、开放标签的3期研究。mPDAC和东部肿瘤协作组的表现状态评分为0或1的患者被随机(1:1)接受NALIRIFOX(脂质体伊立替康50 mg/m²,奥沙利铂60 mg/m²,亚叶酸400 mg/m²和氟尿嘧啶2400 mg/m²,连续静脉输注46小时)或nab-紫杉醇125 mg/m²和吉西他滨1000 mg/m²,在28天周期的第1,8和15天静脉内给药。主要终点是意向治疗人群的总生存率,当两个治疗组中至少观察到543个事件时进行评估。所有接受至少一剂研究治疗的患者均进行了安全性评估。
研究结果:在2020年2月19日至2021年8月17日期间,770名患者被随机分配(NALIRIFOX,383;nab-紫杉醇-吉西他滨,387;中位随访16.1个月[IQR 13.4-19.1])。NALIRIFOX组的中位总生存期为11.1个月(95%CI 10.0-12.1),而nab-紫杉醇-吉西他滨组为9.2个月(8.3-10.6)(风险比0.83;95%CI 0.70-0.99;p=0.036)。
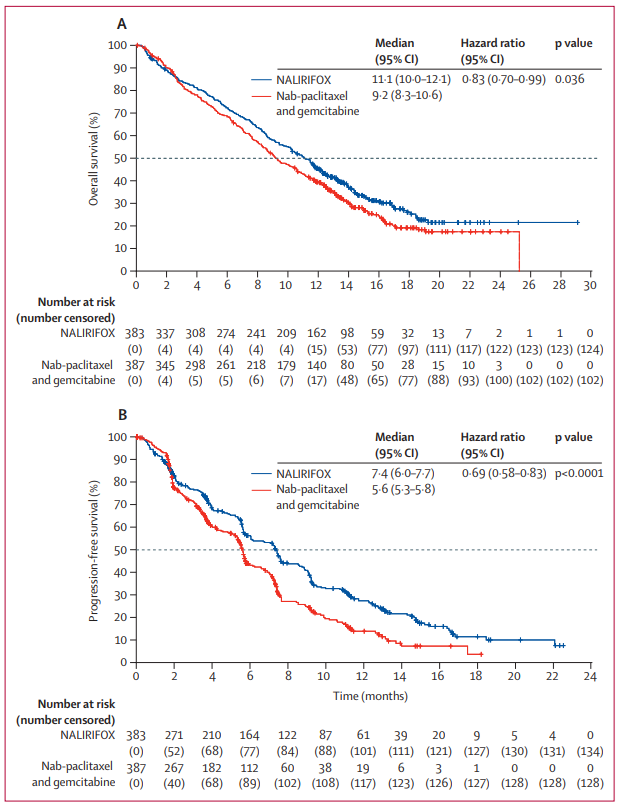
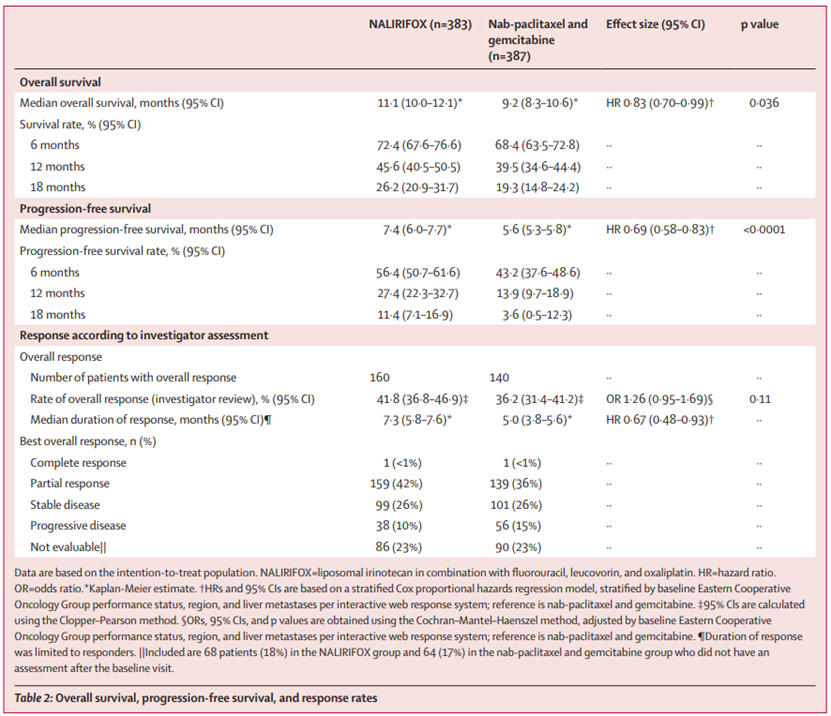
安全性分析:370例接受NALIRIFOX治疗的患者中有322例(87%)发生3级或更高级别的治疗紧急不良事件,379例接受nab-紫杉醇-吉西他滨治疗的患者中有326例(86%)发生3级或更高级别的治疗紧急不良事件;NALIRIFOX组有6名(2%)患者和nab-紫杉醇-吉西他滨组有8名(2%)患者发生了与治疗相关的死亡。

结论:该研究结果支持使用NALIRIFOX方案作为转移性胰腺导管腺癌(mPDAC)一线治疗的可能参考方案。
原始出处:
Wainberg ZA, et al. 2023. NALIRIFOX versus nab-paclitaxel and gemcitabine in treatment-naive patients with metastatic pancreatic ductal adenocarcinoma (NAPOLI 3): a randomised, open-label, phase 3 trial. The Lancet. DOI: 10.1016/s0140-6736(23)01366-1.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言