放射诱发性肉瘤,这些知识点需要掌握!
2023-10-24 大乘医学资讯 大乘医学资讯 发表于上海
随着放射治疗学的发展,癌症患者的生存期延长,故RIS的发生率也随之日益增高,且对其治疗来说是一种挑战。
放射诱发性肉瘤(Radiation-Induced Sarcomas, RIS)为少见的临床类型,是由于既往癌症或接受大剂量放射治疗(RT)其它疾病所致的照射后发生的医源性肿瘤。随着放射治疗学的发展,癌症患者的生存期延长,故RIS的发生率也随之日益增高,且对其治疗来说是一种挑战。在放射治疗后10年时RIS的发生率为0.03-0.2%,15年时累积RIS发生率为3.2/1000。RIS占所有肉瘤确诊的3%-6%。
RIS表现为侵袭性肿瘤亚型和行为,绝大多数为中高级别肿瘤。PFS和OS分别为15个月和21个月。RIS的定义还尚未被明确定义,通常采用Cahan所提议及修改的标准:
1.在放射治疗时没有新肿瘤的依据
2.肉瘤出现在辐照区域
3.肉瘤发病前潜伏期较长
4.组织学证实的肉瘤
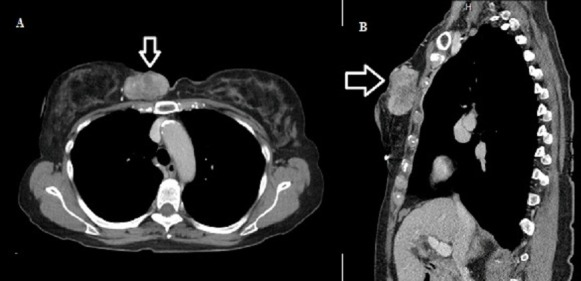
在评估和发现放疗诱发的肿瘤(RIS)以及原发肿瘤蔓延距离时,核磁共振成像(MRI)与计算机断层成像(CT)是较好的成像的设备(上图)。RIS的影像特点缺乏特异性,仅依靠影像学很难鉴别其与原发肿瘤,因此单纯通过影像学不能确诊RIS。
一项回顾性研究统计了1979-2013年34年间确诊的肉瘤2845例,其中64例(2%)为RIS。与原发肿瘤的中位间隔时间为11年,整个队列的5年生存率为32%。
法国居里研究所的一项回顾性研究显示,在总计13472例接受放射治疗的患者,中位剂量为50-55Gy,有35位患者患上了肉瘤,潜伏期为3-20.3年,其中13例为血管肉瘤,5年生存率为36%。
已经明确的RIS危险因子有:治疗时年龄较小,以及治疗相关的因素包括高放射剂量、放疗同时给予含有烷化剂的化疗方案。RIS的发生还与Brca1基因突变,遗传性疾病(如Gardner综合征和Li-Fraumeni综合征有关)。放疗剂量大于50Gy可导致细胞死亡,而低剂量(<30 Gy)导致基因不稳定(DNA修复基因的缺失导致DNA变异的增加)并且损害细胞修复机制。基因组不稳定被认为是放射诱导性肉瘤的原因之一。
非转移性RIS唯一可治愈性的方式是宽切缘的根治性切除。外科手术包括广泛切除,保肢治疗或离断术。二次放射治疗在局部晚期RIS中的作用尚不清楚。由于放射性肉瘤位于放疗野内,通常对放疗不再敏感。如果需要考虑二次放疗,质子/重离子放疗可以考虑,因为粒子射线的高相对生物学效应、低氧增强比、布拉格峰集中释放能量等特点可杀灭光子不敏感的肿瘤细胞,特别是针对头颈部的RIS。
对于转移性肿瘤患者,姑息化疗使用单药阿霉素仍然是治疗大多数RIS的首选。
总体而言,放疗诱发的肉瘤预后差,相比于其他常见机制诱发的肉瘤恶性程度更高,存活率低于散发性软组织肉瘤。在单变量分析中,发生在乳房和上肢的RIS与较低的死亡风险相关。中位OS在接受治愈性治疗和未接受治愈性治疗的患者存在差异,分别为37个月vs13个月。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







