Cell Death Differ:间充质干细胞移植技术揭示外泌体miR-21或可成为视网膜变性的潜在治疗靶标
2020-11-06 xiaozeng MedSci原创
感光细胞凋亡作为感光细胞死亡的主要形式之一,被认为是视网膜变性相关疾病的一种关键发病机制,其拮抗作用或可成为一种潜在的保护视觉功能的方法。
感光细胞凋亡作为感光细胞死亡的主要形式之一,被认为是视网膜变性相关疾病的一种关键发病机制,其拮抗作用或可成为一种潜在的保护视觉功能的方法。
既往研究显示,间充质干细胞移植(MSCT)在眼疾的治疗上具有巨大潜力,其中细胞外囊泡(EVs),特别是外泌体已成为有效的眼科治疗手段。然而,目前仍不清楚MSCT是否以及如何保护感光细胞免受细胞凋亡。因此,阐明相关的潜在作用和机制或可为视网膜变性相关疾病提供潜在的新疗法。
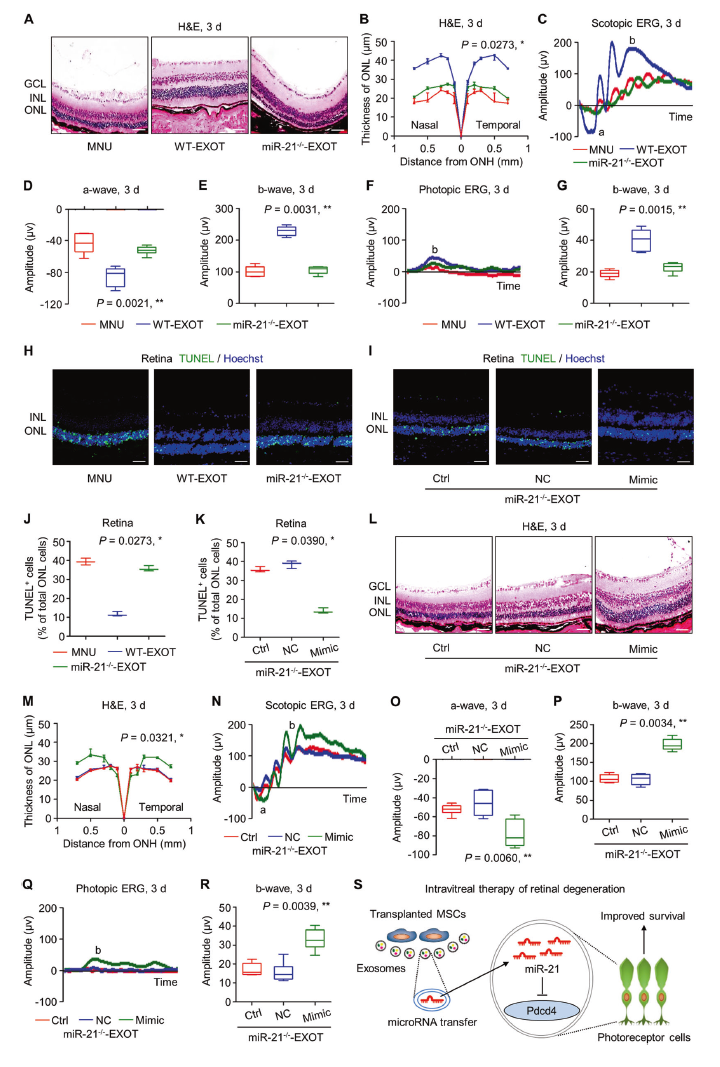
在该研究中,研究人员发现,在MNU(N-甲基-N-亚硝基脲)诱导感光细胞损伤的小鼠模型中,玻璃体内MSCT能够抵消光感受器的凋亡并减轻视网膜形态和功能上的退化。有趣的是,GW4869预处理能够通过阻断外泌体的生成抑制MSCT的作用。此外,MSC衍生的外泌体移植(EXOT)能够有效的抑制MNU诱发的感光细胞损伤。
玻璃体内MSCT能够抵消光感受器的凋亡并减轻视网膜病变
值得注意的是,MSCT和EXOT对MNU诱导的视网膜变性的治疗效果是持续性的,即使注射后1-2个月也能够检测到对感光细胞的保存和视网膜维持作用。更重要的是,Pde6bmut(Pde6b基因无义突变)引起的自然发生的视网膜变性模型中,研究人员证实,MSCT和EXOT可以防止感光细胞的丢失并长期保护视网膜的功能。
进一步的机制研究显示,miR-21能够通过靶向Pdcd4来维持抗MNU损伤的感光细胞的活性,并通过MSC衍生的外泌体进行转移以行使其功能调节作用。此外,缺乏miR-21会加重MNU诱发的视网膜损伤,这一作用受到EXOT的抑制。研究人员进一步证实,miR-21能够调节EXOT对MNU诱导的感光细胞凋亡和视网膜功能障碍的治疗作用。
外泌体miR-21能够抵消MNU诱导的感光细胞凋亡和视网膜变性
综上,该研究结果揭示了基于间充质干细胞移植(MSCT)的感光细胞保护机制,表明外泌体miR-21或可成为视网膜变性的一个潜在治疗靶标。
原始出处:
Deng, C., Hu, C., Ling, S. et al. Photoreceptor protection by mesenchymal stem cell transplantation identifies exosomal MiR-21 as a therapeutic for retinal degeneration. Cell Death Differ (20 October 2020).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#间充质干细#
35
#miR#
23
#miR-21#
38
#视网膜变性#
29
#Cell#
29
#细胞移植#
21
#Differ#
24
#治疗靶标#
39
揭示了基于间充质干细胞移植(MSCT)的感光细胞保护机制,表明外泌体miR-21或可成为视网膜变性的一个潜在治疗靶标。
69
#CEL#
29