Trends in Cancer:弥漫性中线胶质瘤的CAR-T细胞疗法综述
2024-03-01 儿童肿瘤前沿 儿童肿瘤前沿 发表于上海
本文概括了最近以来用于DMG上的几种CAR T疗法。
弥漫性中线胶质瘤(Diffuse midline glioma, DMG)是一种致命的儿童和青少年中枢神经系统(CNS)癌症, 由少数突胶质细胞前体类细胞变异而来,在脑桥、丘脑、中脑和脊髓中都有发现, DMG 占所有儿科高级别胶质瘤(HGG)的 50%,是所有癌症中死亡率最高的(占所有儿科癌症相关死亡的 20-25%), 中位总生存期低于 1年。
由于DMG 的位置和浸润性,很难干净地手术清除肿瘤,加上血脑屏障,导致药物递送至肿瘤部位受到很大的限制,姑息性放疗的效益也很有限,而且肿瘤免疫微环境(TME)非常复杂和免疫抑制性,一直以来缺少有效的治疗方法,但近年发展迅速的CAR T疗法在DMG上展示了希望。
近日,澳大利亚纽卡斯尔大学,健康、医学和保健学院的 Matthew D. Dun 等作者在 Trends in Cancer 上发表了一篇题为 CAR T Cell Therapies for Diffuse Midline Glioma 的综述,概括了最近以来用于DMG上的几种CAR T疗法。

近年来CAR T细胞疗法在治疗血液恶性肿瘤上有了重大突破, 为CAR T细胞疗法在实体瘤临床使用中铺平了道路, 图1列出了已上临床试验的几款CAR T细胞疗法, 下面一一介绍这几款CAR T细胞疗法。

图1- 临床试验的几款CAR T细胞疗法
ERBB2 受体酪氨酸激酶 (HER2) 已被研究作为儿童和成人进展期非脑桥中枢神经系统肿瘤的治疗靶点,已有两例临床试验(NCT03500991和NCT02442297), 证明了其耐受性和安全性。虽然还不十分清楚颅内 CAR T 细胞持久性与肿瘤位置、CAR T 设计或过去治疗史的关系,但治疗后的中位总生存期有所延长,分别为 11.1 个月和24.5 个月。
表皮生长因子受体 (EGFR)是一个与肿瘤生长有关的广泛运用治疗靶点, 并且在一些 DMG 中过度表达。在一项针对患有 HGG 的成人的 二期试验 (NCT01454596) 中,在十名患者中通过 qPCR 和流式细胞方法均可检测到 CAR T 细胞,虽然在治疗后1个月后的外循环血液中没检测到CAR T细胞,但患者没有发现脱靶毒性,并表现出治疗后抗原密度的降低、免疫抑制调节性 T 细胞的浸润,以及激活了肿瘤抑制因子。
B7-同源物 3 蛋白 (B7-homolog 3 protein,B7-H3), 也是一个潜在的好靶点,它在多种癌症中, 包括DMG中过度表达。CAR T 细胞以重复、脑室内、每隔一周的给药方案进行输送,在对血清和脑脊液中细胞因子的评估中表明,局部输注后免疫细胞参与增加,有局部免疫激活的迹象,而且治疗后患者的脑脊液中可检测到循环的CAR T 细胞,这表明CAR T 细胞在中枢神经系统室中的持续性。
双唾液酸神经节苷脂 (Disialoganglioside,GD2)在多种实体瘤和中枢神经系统肿瘤中高表达,而在健康的组织中几乎不表达,一期临床试验 (NCT04196413),开始评估静脉 (IV) 输注自体 GD2 CAR T 细胞,然后可选择重复脑室内 (ICV) 给药,受试的四例患者有三例显示了肿瘤明显减小和神经系统改善。除了表上列的临床试验,还有两项 一期临床试验NCT04099797、ACTRN12622000675729, 目前也在招募 DMG和 DIPG患者以及其他 CNS 肿瘤患者。
白细胞介素 13 受体亚基 α2 (IL-13Rα2) 在DMG和多种中枢神经肿瘤中高度表达,针对 IL-13Rα2 阳性脑肿瘤儿童患者的一期临床试验 NCT04510051目前正在招募中,初步数据显示IL-13Rα2 在胶质母细胞瘤中的可行性和耐受性,并有可能扩展到 DMG 作为组合靶点, 联合单克隆抗体 (mAb) 疗法 nivolumab (PD1) 和 ipilimumab (CTLA-4), 使用 IL-13Rα2 CAR T 的第二项一期临床试验 (NCT04003649) 目前也正在进行中。
“四驾车”(针对B7-H3、EGFR806、HER2 和 IL-13Rα2四个靶点), 为解决DMG肿瘤高异质性,世界首例针对这四个靶点的一期CAR T试验 (BrainChild-04; NCT05768880) 最近向儿童和年轻人(1-26 岁)开放,参与这项研究的患者将收到由不同CAR T 细胞群汇集的载体生成的细胞产品。
治疗相关毒性 谈到CAR T疗法,其治疗毒性不得不谈。特别是针对中枢神经系统肿瘤的治疗,文章详细地列出了“在靶点上但没击中肿瘤”(on-target/off-tumor)毒性;细胞因子释放综合征;免疫效应细胞相关神经毒性综合征;肿瘤炎症相关的神经毒性, 详情请参考原文。
尚未解决的问题和将来发展的方向
尽管CAR T 疗法在治疗DMG 上很有希望,但用来筛选肿瘤相关抗原表型分析和治疗分层的活体肿瘤样本很有限,这是优化新CAR T疗法所面临的挑战。此外,考虑到高昂的研发和生产成本,针对每个患者生产带有接头 (adapter) 的多“驾车”,也将是巨大的经济挑战。更重要的是,许多关于肿瘤免疫微环境和独特的 DMG GAM 群体对 CAR T 细胞功效影响的多个问题仍未得到清晰的答案。例如,由于脑-血屏障和治疗中枢神经系统的肿瘤,颅内输送CAR T细胞和重复分次给药的效果怎样?CAR T 细胞的持久性达到什么程度?可能引起儿童的持续反应有哪些?当我们以治愈为目标时,孩子们的生活质量如何?CAR T疗法可以扩大到患有中枢神经系统肿瘤(包括 DMG)的年轻患者中?儿童患者和成人相比,有哪些因素影响 CAR T细胞的选择和反应?由于DMG的高特异性,有什么办法更有效地识别用于 CAR T 细胞开发的新型肿瘤相关的抗原?除了肿瘤免疫微环境外还有哪些局部因素影响治疗效果?
今后的发展可从三大方向上考虑:
1、局部给药和克服肿瘤免疫微环境,有效的T 细胞运输依赖于足够的天然信号网络(CCL3、CCL3、IL-1A、IL-6)来将具有杀伤力的CD8+ T 细胞募集到肿瘤部位,这在 DMG 免疫活性上不是个问题。局部给药可以有效地将 CAR T 细胞直接输送到肿瘤部位,进而引发能够促进免疫细胞浸润,引起局部炎症而攻击肿瘤细胞。
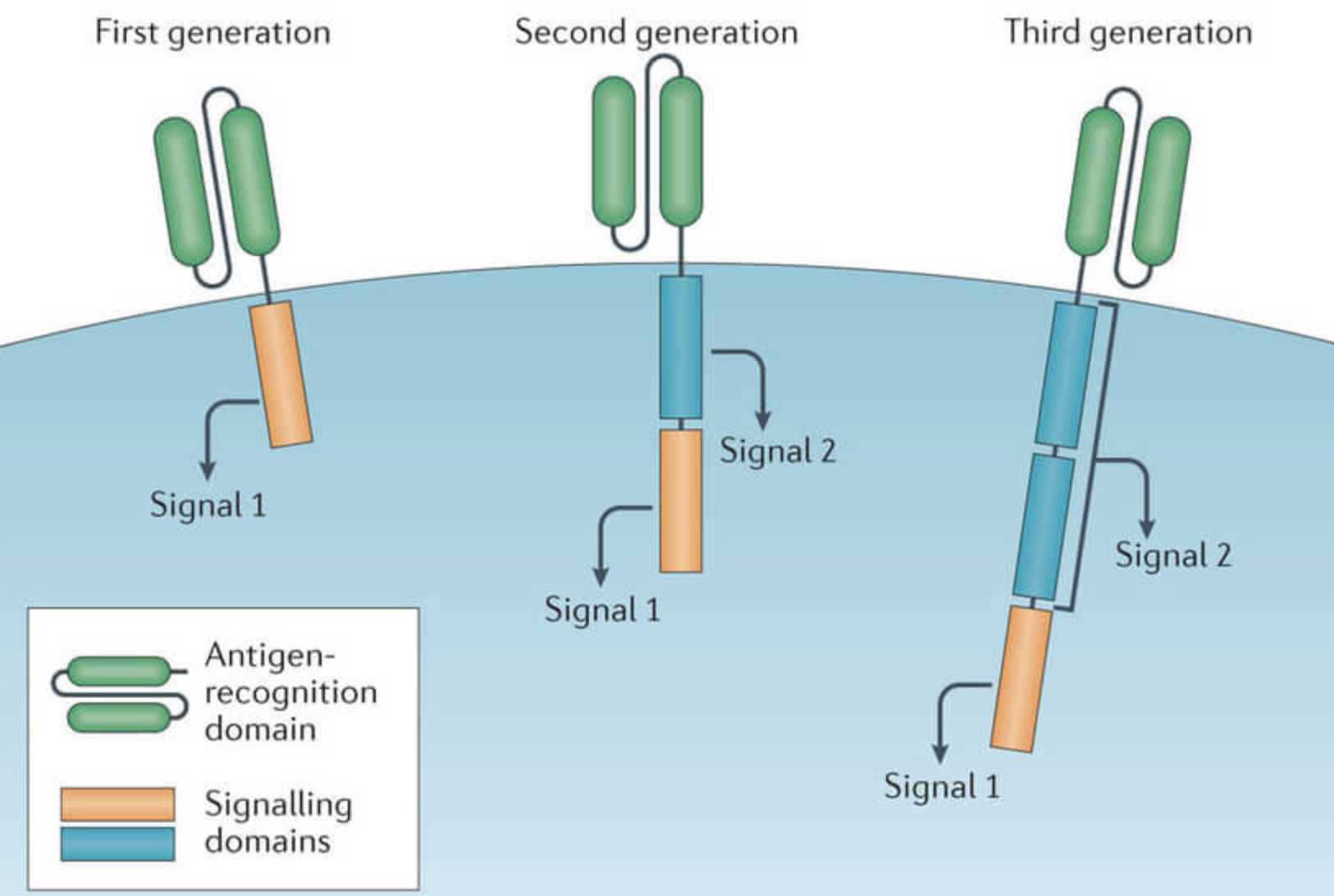
2、新的CAR T 工程设计,CAR T 细胞持久性的变化可能源于多种因素,包括 CAR T 细胞设计、制造程序、T 细胞亚群以及肿瘤免疫微环境,治疗效果高度依赖于 T细胞的适应性,其特征是耗竭标记物(exhaustion markers)的表达,如 PD-1、TIM-3、CTLA-4、TIGIT 和 LAG-3。在 DMG 背景下,肿瘤负荷、抗原密度和 scFv 亲和力是 CAR T 细胞设计中需要考虑的重要因素,因为它们会影响 CAR T 细胞激活值,从而影响耗竭标记物的表达。此外,随着多次给药策略的使用,有一个问题值得考虑,在这些情况下,CAR T细胞需要什么水平的持久性?最近“装甲车”(armored CAR)的设计,是通过增加共表达的免疫调节域来增强 CAR T 细胞的功能,以提高细胞持久性、降低细胞毒性和/或积极影响肿瘤免疫微环境,这些包括增加分泌性细胞因子以创造更有利的免疫微环境;增加趋化因子(chemokine) 受体以实现更好的引导T细胞到达肿瘤部位;增加配体的共表达,例如,与第三代 CAR T 细胞相比,共表达 IL-15 的第二代 GD2 CAR T 细胞在患有胶质母细胞瘤和 DMG 的小鼠中表现出优异的植入和抗肿瘤控制能力;此外,用于治疗胶质母细胞瘤的 CAR T 细胞中共表达 IL-15 表现出更强的抗肿瘤反应,并增加了其他免疫实体(包括 CD8+、NK 和 B 细胞)的参与,还有表达IL-15Rα的骨髓细胞同时被CAR T细胞杀死,从而阻断了它们的免疫抑制信号的传导。
3、靶点选择和DMG肿瘤异质性,评估几乎所有癌症类型的 CAR T 细胞的研究表明,由于肿瘤内异质性引起的抗原逃逸或治疗耐药群体,CAR T 细胞丧失部分有效性(图 2A-传统CAR T技术中肿瘤细胞的逃逸)。多靶点的CAR T开发正是为了解决这个问题(图 2B-不同靶点的CAR T 细胞共同输入患者),例如在患有 R/R 疾病的儿童 B-ALL 患者中,CD19 和 CD22 定向 CAR T 细胞的共同给药,这一组合提高了完全缓解率并降低了复发率 。上面所提到的四靶点 CAR T 细胞疗法的临床试验,目的是挑战多靶点CAR T 的工程极限。接头(adapter) CAR 技术是一种新兴的治疗策略,在 DMG 和许多其他癌症方面显示了治疗潜力(图 2C-接头小分子和CAR T共同作用于肿瘤细胞),它通过多个接头分子来提高 CAR T靶向的灵活性,这些接头分子靶向异质群体,同时也充当介导急性毒性事件的激活/抑制调节剂的功能,接头分子通常和IgG 分子大小差不多,因此具有脑血屏障渗透性,可以减少DMG 和其他 CNS 肿瘤对CAR T疗法的阻碍。
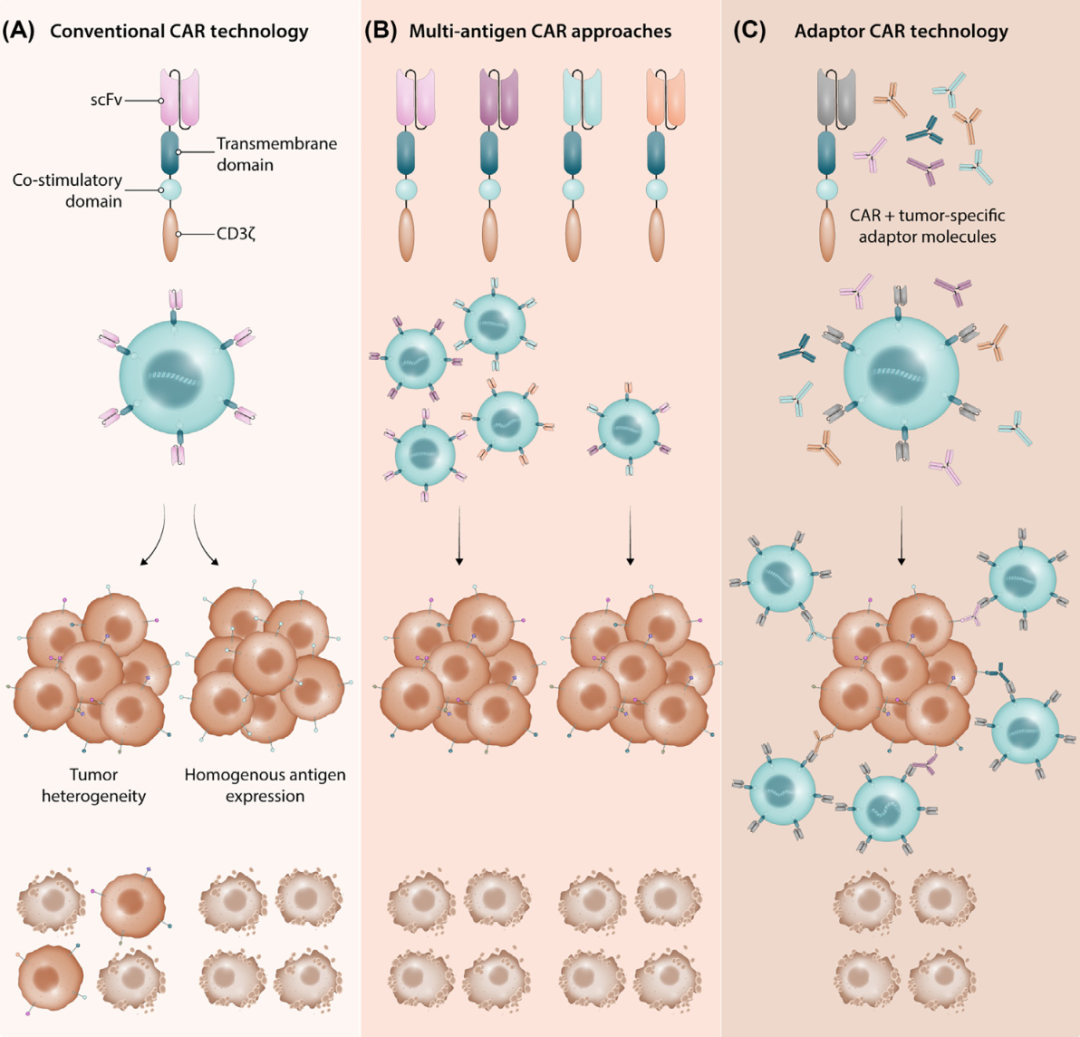
图 2 解决肿瘤异质性的 CAR T 细胞设计和治疗策略
总之,由于免疫惰性和复杂的微环境使DMG的治疗更具挑战,我们期待新颖的CAR T 技术在治疗DMG上的突破。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#Car-T细胞疗法# #弥漫性中线胶质瘤#
19