细胞“霸凌者”
2016-12-23 勃林格殷格翰中国 勃林格殷格翰中国
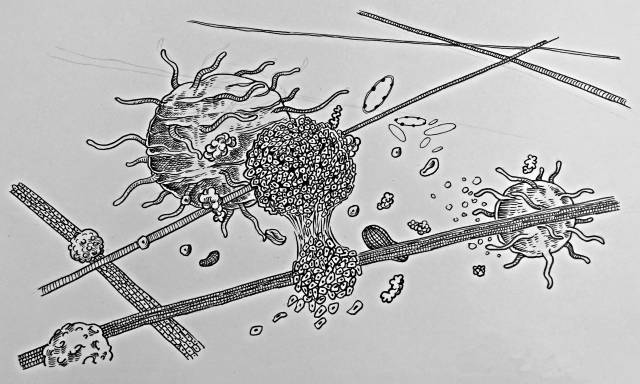
不止校园生活,人体内也会悄无声息地上演“霸凌故事”。而这一切的源头,起始于一个癌细胞的觉醒。 虽然和正常细胞出自同门,但这个癌细胞生来就知道自己唯一的使命:那就是—— 奋力活下去。 而且,不惜一切代价。 疯狂的叛逆者 人体内有几百万种细胞,不同种类的细胞聚合形成不同的组织和器官。 在正常组织和器官中,细胞的生长过程受到
不止校园生活,人体内也会悄无声息地上演“霸凌故事”。而这一切的源头,起始于一个癌细胞的觉醒。
 虽然和正常细胞出自同门,但这个癌细胞生来就知道自己唯一的使命:那就是——
奋力活下去。
而且,不惜一切代价。
疯狂的叛逆者
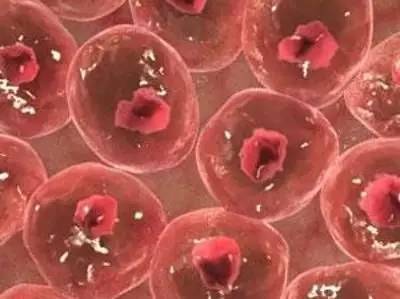
人体内有几百万种细胞,不同种类的细胞聚合形成不同的组织和器官。
在正常组织和器官中,细胞的生长过程受到精心的调控:是生存还是毁灭,对于细胞来说不是一道难题。
像所有正常细胞一样,癌细胞也遵循着这最基本的单细胞一分为二的生长原则。
通常情况下,细胞们各个行为规范,遵纪守法;但偶尔会有那么一个细胞特立独行,肆无忌惮的生长,在这阴森残酷的过度生长中,不断演化出疯狂的癌细胞。
癌细胞的座右铭:立志成为细胞的叛逆者。
癌细胞的疯狂生长就像花园里的野草,一旦失控生长,其他植物便逐渐凋亡。
虽然和正常细胞出自同门,但这个癌细胞生来就知道自己唯一的使命:那就是——
奋力活下去。
而且,不惜一切代价。
疯狂的叛逆者
人体内有几百万种细胞,不同种类的细胞聚合形成不同的组织和器官。
在正常组织和器官中,细胞的生长过程受到精心的调控:是生存还是毁灭,对于细胞来说不是一道难题。
像所有正常细胞一样,癌细胞也遵循着这最基本的单细胞一分为二的生长原则。
通常情况下,细胞们各个行为规范,遵纪守法;但偶尔会有那么一个细胞特立独行,肆无忌惮的生长,在这阴森残酷的过度生长中,不断演化出疯狂的癌细胞。
癌细胞的座右铭:立志成为细胞的叛逆者。
癌细胞的疯狂生长就像花园里的野草,一旦失控生长,其他植物便逐渐凋亡。
 那么,是什么激怒了正常细胞,一反常态,胡作非为了呢?
基因突变是这一研究中的重要理论。
基因和突变
19世纪中叶,奥地利的孟德尔修道士从研究豌豆植物的形状中确立了生物体遗传原理。
他发现,所有复杂生物体都通过同一种遗传机制将信息传递给子女,这种信息包被称为基因。
每一个基因都担负着组建一种人体性状的功能。
所以我们的生老病死等一切生命现象都与基因有关,不同的基因就含有不同的遗传信息。
1944年,我们知道了基因的物质表现是DNA:它是由两条相互盘绕的链组成双螺旋,两条链之间依靠碱基对牵手成功,每个DNA分子上有多个基因。
为了保证我们生物的基本特征能被长长久久的传递下去,每一个母细胞都可以精确忠实地复制自身DNA螺旋链,更重要的是,这种能力会被无私赋予她未来的子细胞。
大部分情况下,DNA的复制都能准确无误。但百密终有一疏。
1953年,科学家们发现有一小撮基因在受到化学物质的影响后,DNA的结构发生了改变,这一改变被称为“突变”;1976年,研究者进一步发现了背后的罪魁凶手——“原癌基因”。
每个原癌基因遵照自己独特的突变机制,不断发出强大的生长刺激信号。
从此细胞的正常生长发生偏离,走向黑暗。
那么,是什么激怒了正常细胞,一反常态,胡作非为了呢?
基因突变是这一研究中的重要理论。
基因和突变
19世纪中叶,奥地利的孟德尔修道士从研究豌豆植物的形状中确立了生物体遗传原理。
他发现,所有复杂生物体都通过同一种遗传机制将信息传递给子女,这种信息包被称为基因。
每一个基因都担负着组建一种人体性状的功能。
所以我们的生老病死等一切生命现象都与基因有关,不同的基因就含有不同的遗传信息。
1944年,我们知道了基因的物质表现是DNA:它是由两条相互盘绕的链组成双螺旋,两条链之间依靠碱基对牵手成功,每个DNA分子上有多个基因。
为了保证我们生物的基本特征能被长长久久的传递下去,每一个母细胞都可以精确忠实地复制自身DNA螺旋链,更重要的是,这种能力会被无私赋予她未来的子细胞。
大部分情况下,DNA的复制都能准确无误。但百密终有一疏。
1953年,科学家们发现有一小撮基因在受到化学物质的影响后,DNA的结构发生了改变,这一改变被称为“突变”;1976年,研究者进一步发现了背后的罪魁凶手——“原癌基因”。
每个原癌基因遵照自己独特的突变机制,不断发出强大的生长刺激信号。
从此细胞的正常生长发生偏离,走向黑暗。
 与原癌基因相抗衡的,是肿瘤抑制基因。 两者就像一辆平稳运行中的车辆,需要刹车和油门,原癌基因就如同油门,肿瘤抑制基因如同刹车,踩足油门和刹车故障的协力,便促成了癌症的发生和发展。
于是,癌症根源逐渐浮出水面:其实就是原癌基因和肿瘤抑制基因的博弈。
不过,正常细胞的叛变进而形成癌细胞,其不断扩张和强大,最终形成肿瘤,这是一个旷日持久的过程,因为这一暗黑势力的征途从来都不是一马平川的。
暗黑势力的征途
最大的障碍来自于细胞的信号传导系统,她严厉拒绝一切由于某个原癌基因的激活或某个肿瘤抑制基因的失活所引起的混乱。
信号传导系统藏身何处?
每一细胞的表面,有一系列受体,使细胞能感知生长或抑制,受体一端伸入细胞外部,穿越细胞膜,另一端则伸入细胞内部,释放信号进行传导。
正常细胞收到生长刺激信号后,会经过慎重的思考和评估,最终决定是否启动繁殖。
其次,我们人体自身免疫系统中有一类强悍的卫士-自然杀伤白细胞,也会筑起一道防线来识别和歼灭癌细胞的发育。
与原癌基因相抗衡的,是肿瘤抑制基因。 两者就像一辆平稳运行中的车辆,需要刹车和油门,原癌基因就如同油门,肿瘤抑制基因如同刹车,踩足油门和刹车故障的协力,便促成了癌症的发生和发展。
于是,癌症根源逐渐浮出水面:其实就是原癌基因和肿瘤抑制基因的博弈。
不过,正常细胞的叛变进而形成癌细胞,其不断扩张和强大,最终形成肿瘤,这是一个旷日持久的过程,因为这一暗黑势力的征途从来都不是一马平川的。
暗黑势力的征途
最大的障碍来自于细胞的信号传导系统,她严厉拒绝一切由于某个原癌基因的激活或某个肿瘤抑制基因的失活所引起的混乱。
信号传导系统藏身何处?
每一细胞的表面,有一系列受体,使细胞能感知生长或抑制,受体一端伸入细胞外部,穿越细胞膜,另一端则伸入细胞内部,释放信号进行传导。
正常细胞收到生长刺激信号后,会经过慎重的思考和评估,最终决定是否启动繁殖。
其次,我们人体自身免疫系统中有一类强悍的卫士-自然杀伤白细胞,也会筑起一道防线来识别和歼灭癌细胞的发育。
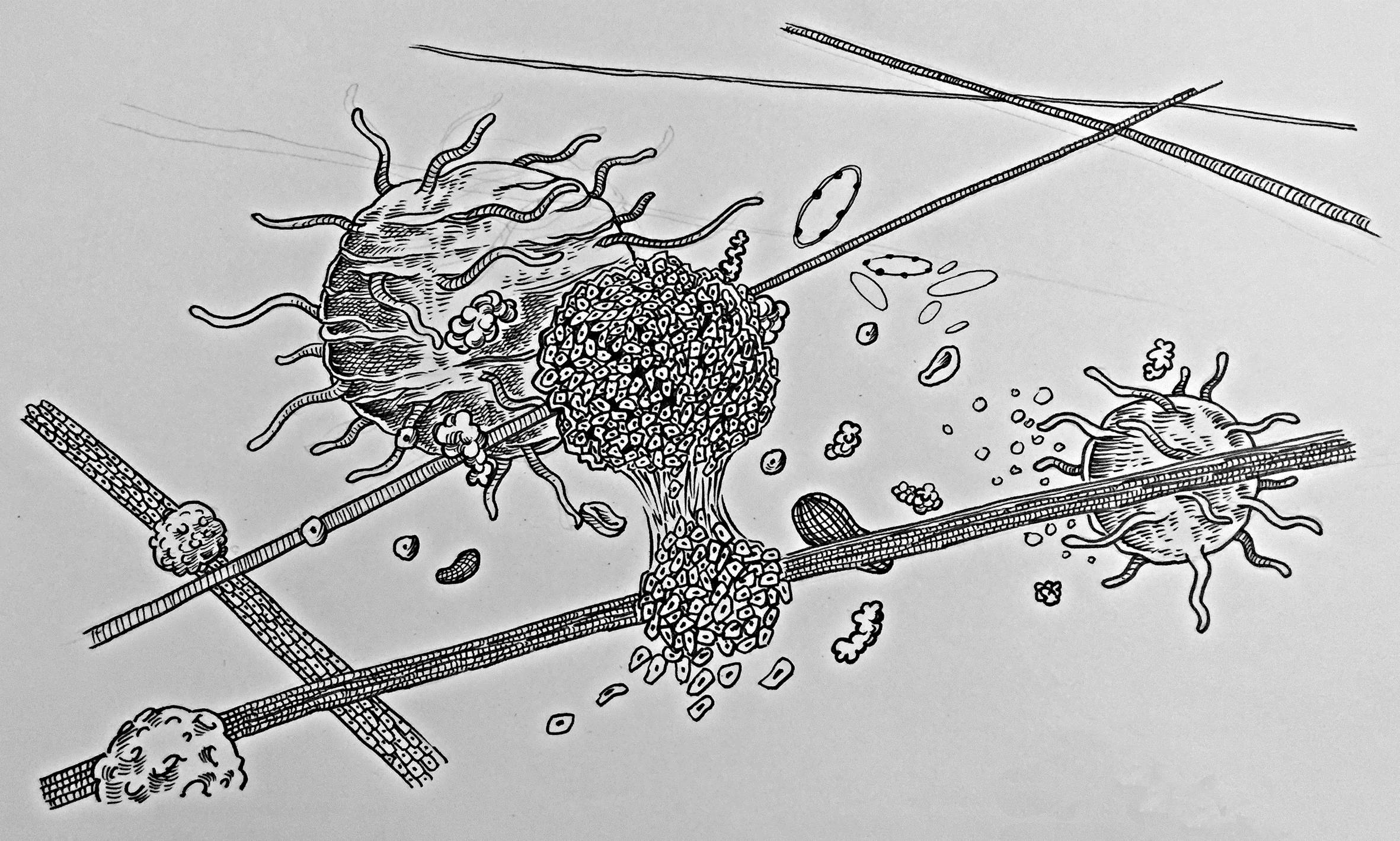 最后幸运的是,体内某些具有大无畏精神的细胞还会启动终级自杀,通过迅速自我牺牲来剥夺外来入侵癌细胞繁衍的合适寄主,以此来消灭全身各处的越轨癌细胞。
但是无论如何,在远征的途中,可能终将会有一小撮暗黑势力的癌细胞过关斩将,不断壮大,甚至在全身各处安营驻扎。
聪明的癌细胞,会借助破损的基膜进入皮下组织,进行疯狂扩张;也会借助血管和淋巴管进行远处移民,排除万难爬至管道的悬崖峭壁上进行繁殖和壮大。
每到一个新环境,癌细胞一定会面临严峻考验,但是达尔文的进化论告诉我们,终将会有少数拥有特别本领的细胞叛逆者会在战争中幸存,无所谓这场战争是正义还是邪恶的。
当然,在与癌细胞进行殊死搏斗时,受到威胁的我们绝不会坐以待毙。
生命智慧和医学文明终将站在一个战壕,同仇敌忾。
现在,这个人体细胞的“霸凌者”将遭遇内外夹击。
人类和癌症的战争,就此拉开。
最后幸运的是,体内某些具有大无畏精神的细胞还会启动终级自杀,通过迅速自我牺牲来剥夺外来入侵癌细胞繁衍的合适寄主,以此来消灭全身各处的越轨癌细胞。
但是无论如何,在远征的途中,可能终将会有一小撮暗黑势力的癌细胞过关斩将,不断壮大,甚至在全身各处安营驻扎。
聪明的癌细胞,会借助破损的基膜进入皮下组织,进行疯狂扩张;也会借助血管和淋巴管进行远处移民,排除万难爬至管道的悬崖峭壁上进行繁殖和壮大。
每到一个新环境,癌细胞一定会面临严峻考验,但是达尔文的进化论告诉我们,终将会有少数拥有特别本领的细胞叛逆者会在战争中幸存,无所谓这场战争是正义还是邪恶的。
当然,在与癌细胞进行殊死搏斗时,受到威胁的我们绝不会坐以待毙。
生命智慧和医学文明终将站在一个战壕,同仇敌忾。
现在,这个人体细胞的“霸凌者”将遭遇内外夹击。
人类和癌症的战争,就此拉开。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言