中科院在提升CAR-T细胞抗异质性肿瘤活性方面取得新进展
2022-07-31 中国科学院广州生物医药与健康研究院 网络
该研究中构建的双靶点CAR-T细胞具有提升CAR-T细胞抗异质性肿瘤细胞活性的能力,为临床免疫细胞治疗实体肿瘤提供新策略。
中国科学院广州生物医药与健康研究院研究员李鹏课题组与暨南大学李扬秋课题组合作,通过在传统CAR分子内引入DAP10分子调动内源NKG2D的广谱抗原识别功能,提升CAR-T细胞对异质性肿瘤的靶向能力。课题组近日在Molecular Therapy – Oncolytics上发表了研究论文。
CAR-T细胞在治疗血液肿瘤方面取得重大突破,但是对实体肿瘤的疗效却不佳,实体肿瘤的异质性是阻止CAR-T细胞治疗实体瘤的一大障碍。为减少CAR-T疗法中因肿瘤异质性导致的免疫逃逸和肿瘤复发,亟需改进和优化CAR分子对不同抗原的广谱识别功能。NKG2D是CD8阳性T细胞中表达的一种可识别多种配体的受体,DNAX激活蛋白10(DAP10)同NKG2D受体互作向T细胞传递信号。研究团队猜想,可以利用这一受体的特性增强CAR-T细胞对异质性肿瘤的细胞毒性作用。
研究团队首先设计了一种串联DAP10的嵌合分子,实验表明该嵌合分子可利用T细胞上的天然NKG2D受体靶向表达NKG2D配体的肿瘤细胞;之后将其与抗GPC3单链可变片段(scFv)串联,构建双靶点嵌合抗原体系,发现表达串联GPC3-DAP10嵌合受体的T细胞表现出双抗原靶向作用,在体内外可明显抑制异质性肿瘤细胞生长。
以上结果说明,使用全长DAP10分子替代传统CAR分子内部的跨膜序列,可以让CD8阳性T细胞内源表达的NKG2D受体参与肿瘤的识别与杀伤。因为NKG2D受体是一个具有多抗原识别能力的受体,所以该设计思路显著增加了传统CAR-T细胞对肿瘤细胞的广谱识别能力,减小了在CAR-T治疗中肿瘤免疫逃逸的可能性。因此,该研究中构建的双靶点CAR-T细胞具有提升CAR-T细胞抗异质性肿瘤细胞活性的能力,为临床免疫细胞治疗实体肿瘤提供新策略。
该研究工作主要由广州生物院博士生李尚霖和暨南大学博士后赵若聪为共同完成,李鹏和李扬秋为该论文的共同通讯作者。该研究得到国家自然科学基金、国家重点研发计划、广东基础与运用基础研究基金和广东省新药创制项目的支持。
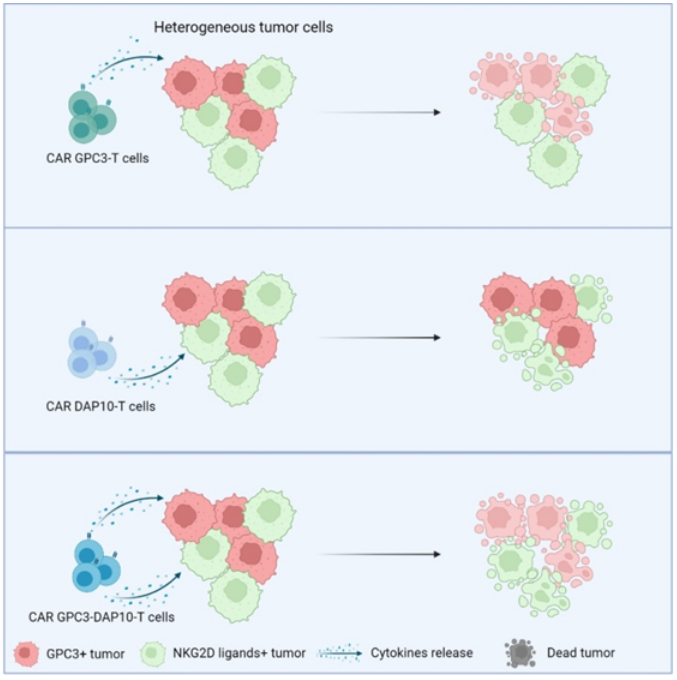
双靶点CAR-T细胞杀伤异质性肿瘤细胞示意图
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#中科院#
65
#CAR-#
46
#肿瘤活性#
46