Blood:MYB不足破坏造血干细胞的蛋白质平衡,导致年龄相关瘤变
2023-01-10 MedSci原创 MedSci原创 发表于上海
Myb不足引起的一系列改变结合在一起导致了蛋白质内稳态的失衡,潜在地创造了一个有利于疾病启始的细胞环境
MYB在整个造血系统的基因调控中起着关键作用,对正常造血干细胞 (HSC) 的维持至关重要。MYB获得性遗传调控异常参与多种白血病的病因学,而MYB基因的遗传非编码变异还是多种血液病的易感性因素,包括骨髓增生性肿瘤 (MPN)。
目前,将MYB水平的变化与疾病易感性联系起来的机制,特别是与疾病起始的年龄依赖性有关的机制,是完全未知的。在该研究中,研究人员建立了Myb缺乏的小鼠模型,该小鼠模型在晚年会发生MPN、骨髓增生异常和白血病,反映了同等人类疾病的年龄特征。
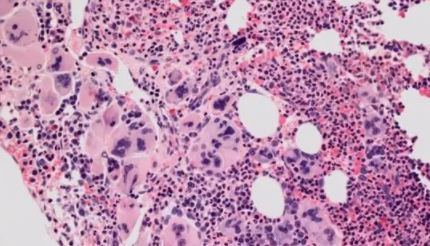
正常小鼠和Myb不足小鼠血液恶性肿瘤的发生率
研究显示,这种疾病起始的年龄依赖性是HSC固有的,涉及由多个基因表达的小影响引起的初始缺陷细胞状态和进一步微妙变化的逐步积累的组合。Myb不足的HSC功能受损。Myb不足在年轻和老年HSC中引起的基因表达存在明显差异。Myb依赖的基因表达差异反映在HSC的功能过程中。结合既往研究,研究人员观察到年轻的Myb缺乏小鼠的蛋白体活性改变,增殖指标升高,随后核糖体活性升高。
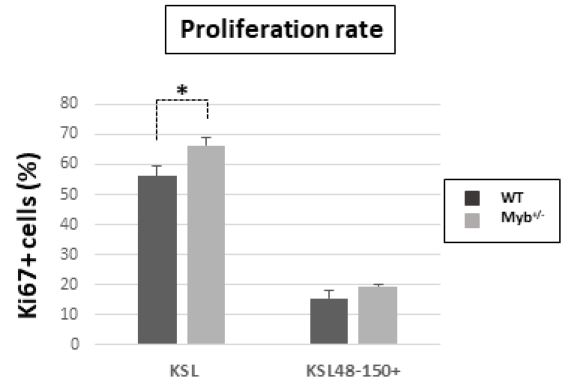
正常和Myb不足HSC的增殖率
最终,研究人员推测,Myb不足引起的上述改变结合在一起导致了蛋白质内稳态的失衡,潜在地创造了一个有利于疾病启始的细胞环境。
原始出处:
Mary L Clarke, et al. MYB insufficiency disrupts proteostasis in hematopoietic stem cells leading to age-related neoplasia. Blood blood.2022019138.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言