Nature:首次实时观察染色体末端修复过程
2016-10-23 佚名 生物谷
在一项新的研究中,来自美国宾夕法尼亚大学佩雷尔曼医学院的研究人员开发出首个系统来观察新合成的端粒中断裂的DNA的修复。这一进展对设计新的癌症药物产生重要影响。相关研究结果于2016年10月19日在线发表在Nature期刊上,论文标题为“Break-induced telomere synthesis underlies alternative telomere maintenance”。 维持染
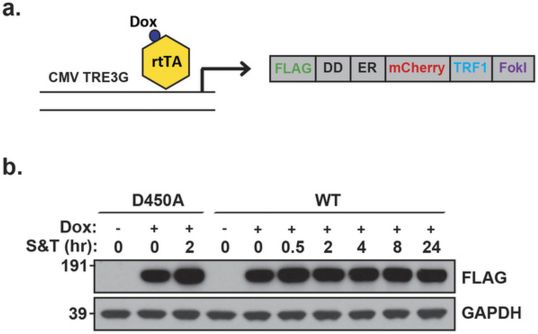
维持染色体的末端(被称作端粒)完整性允许细胞持续地分裂和实现永生。论文通信作者、宾夕法尼亚大学佩雷尔曼医学院癌症生物学副教授Roger Greenberg博士说,“端粒非常像鞋带末端上的鞋花---它们阻止DNA末端受到磨损。”
在大多数癌细胞类型中,端粒通过一种特定的被称作端粒酶的酶将重复性的端粒DNA序列加入到染色体末端上来保持完整。癌细胞也能够使用第二种涉及基于DNA修复的机制---被称作端粒延伸替代(alternative lengthening of telomeres, ALT)---的方法。一般而言,癌细胞选择其中的任何一种端粒维持方法就可变得永生。总的来说,大约15%的癌症(比如,软骨瘤、骨癌和脑癌)利用ATL过程来进行端粒延伸和维持。
当DNA发生断裂时,它触发乳腺癌抑制蛋白BRCA1和BRCA2等DNA修复蛋白发挥作用,并且与其他的辅助蛋白一起附着到受损的DNA片段上。这些蛋白让这种DNA片段延伸出来,从而允许它被端粒DNA互补序列所识别。一般而言,这种被称作同源重组的机制是两个几乎相同的DNA分子进行交换DNA构成单元(building block)时发生的。
在当前的这项新的研究中,研究人员发现端粒使用一种独特的修复过程来制造新的DNA,他们称之为“断裂诱导的端粒合成(break-induced telomere synthesis)”。他们发现端粒的同源重组不同于涉及BRCA1、BRCA2和Rad51蛋白的其他类型的同源重组,其中这些蛋白在乳腺癌患者和有风险患上乳腺癌的人体内发生突变。
Greenberg说,“这就是我们想要在癌细胞中阻止的东西,但是在此之前,当它在发生时,直接追踪这个过程是不可能的。这是首项研究实时地追踪同源重组的所有主要步骤。如今,鉴于我们更好地了解这个过程,在这个过程的不同点进行干扰来阻止癌细胞中的端粒不会持续延伸是可能的。这可能会将它们推向细胞死亡的边缘。”
Elisabeth Naschberger,1 Andrea Liebl,1 Vera S. Schellerer,2 Manuela Schütz,1 Nathalie Britzen-Laurent,1 Patrick K?lbel,1 Ute Schaal,1 Lisa Haep,1 Daniela Robert L. Dilley, Priyanka Verma, Nam Woo Cho, Harrison D. Winters, Anne R. Wondisford & Roger A. Greenberg.Break-induced telomere synthesis underlies alternative telomere maintenance.Nature.2016
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#Nat#
34
#染色体#
28