1例极度罕见的自身免疫性疾病
2021-11-15 洪巧珍 徐忠森 浙江省衢州市柯城区人民医院 “检验医学与临床杂志”公众号
内分泌疾病与自身免疫性疾病有着密不可分的联系,而且内分泌疾病及自身免疫性疾病的全身表现已经突破了不同系统的界限,可以表现为多系统、多器官受累,临床表现复杂多样。
前 言
内分泌疾病与自身免疫性疾病有着密不可分的联系,而且内分泌疾病及自身免疫性疾病的全身表现已经突破了不同系统的界限,可以表现为多系统、多器官受累,临床表现复杂多样。我国内分泌学奠基人朱宪彝教授在生前提出免疫内分泌的概念在实践中得到不断检验和证实,取得很好的临床效果。
检验医师在内分泌疾病和自身免疫性疾病的诊治起着至关重要的作用。本文报道1例累及甲状腺、胸腺、胰岛β细胞和中枢神经系统的自身免疫性疾病,经临床医师缜密的诊疗思维的指导下,和检验科医师的积极开展相关工作,进行了血液和脑脊液的自身免疫性抗体、中毒代谢性脑病、中枢神经和系统脱髓鞘疾病、桥本脑病和寡克隆蛋白电泳等相关检查,最后明确诊断为:自身免疫性多内分泌腺病综合征(APSⅢ型)、边缘性脑炎(GAD介导)、胸腺瘤。该病临床罕见,目前尚未见文献报道。为提高认识,提供临床帮助,本文报道如下。
案例经过
患者女,42岁。因“心悸、口干多饮2.5年,抽搐后1周”于2018年11月3日入院。患者于2016年4月16日出现心悸、左上睑下垂。外院查甲状腺功能升高,结合甲状腺彩超和甲状腺ECT检查,临床诊断:Graves病。同时胸部CT示:前上纵膈肿块(33×18mm),考虑胸腺瘤。
予以甲巯咪唑、口服溴吡斯的明治疗;2月后复查胸部CT胸腺瘤消失;2016年6月22日因口干、多饮、多食,伴体重下降及视物模糊,测随机血糖20mmol/L,以“糖尿病”入院治疗,入院后予胰岛素强化治疗。
住院过程中出现一次四肢抽搐,双眼上翻,口吐白沫,意识丧失,当时血糖9.7mmol/L,约5-6分钟后抽搐停止,意识缓慢转清。查脑电图提示:轻度异常、左侧头前部偏胜伴可疑尖波插入。头颅磁共振:右侧海马旁颞角较左侧扩大,两侧侧脑室后角旁少许缺血性改变。
血糖稳定后出院,出院诊断:糖尿病(1型糖尿病首先考虑)、Graves病、抽搐待查(癫痫考虑)、眼睑下垂(重症肌无力考虑)。
2018年10月27日夜间再次出现四肢抽搐1次,性状与前次类似,当时家属测手指末梢血糖9.8mmol/L。查24小时脑电图提示:中度异常,左侧略偏胜,左侧痫样放电。既往有隆胸手术病史,剖宫产1次。
家族史:无殊。体检:BMI20.7Kg/m2,神清,精神可,左侧眼球稍突出。双手无震颤。甲状腺无明显肿大,未闻及血管杂音。颜面部无浮肿,双肺呼吸音清,未及干湿性啰音,心律齐,未及病理性杂音,腹软,无压痛及反跳痛,双下肢无浮肿,足背动脉搏动正常;神经系统未引出病理反射。
检验案例分析
本次入院时血常规和粪便常规正常;尿常规:葡萄糖2+↑ 、酮体- 、白细胞-;生化:肝肾功能、电解质均正常;甲状腺功能正常范围、甲状腺过氧化物酶抗体>1300.0KIU/L↑、甲状腺球蛋白抗体>500.0KIU/L↑;女性肿瘤标志物7项均正常;抗核抗体阴性;IgG4阴性;抗谷氨酸脱羧酶抗体(GAD)19.58IU/ml↑、胰岛素自身抗体阴性、抗胰岛细胞抗体阴性;血液自身免疫性脑炎系列抗体、脱髓鞘疾病系列抗体均阴性,寡克隆区带阴性;胰岛素、C肽释放试验详见表1。
表1 胰岛素、C肽释放试验结果
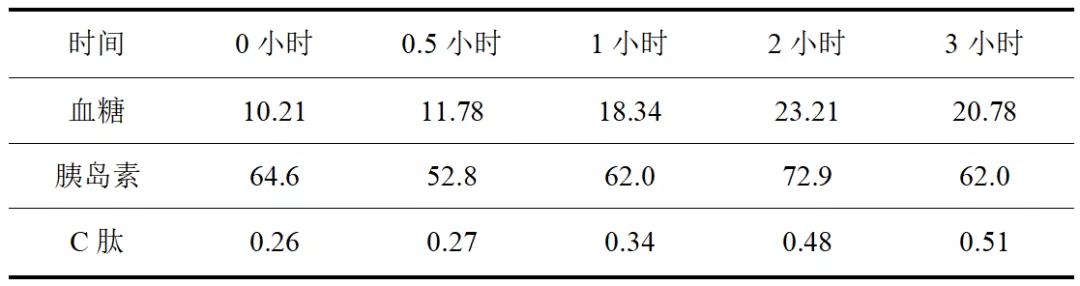
注:正常参考值:空腹胰岛素20.9-174.2pmol/L、空腹C肽0.78-1.89ug/L
脑脊液检查:外观透明、清晰、有核细胞计数1个/uL、脑脊液总蛋白测定257.0mg/L、腺苷脱氨酶3U/L、氯127.3 mmol/L、葡萄糖6.83 mmol/L、乳酸脱氢酶17 U/L、甲状腺过氧化物酶抗体<5KIU/L、甲状腺球蛋白抗体<10KIU/L、GAD1577.66 IU/ml↑↑↑,其余自身免疫性脑炎系列抗体、脱髓鞘疾病系列抗体均阴性,寡克隆区带阴性。
临床案例分析
患者初治时外院查甲状腺功能升高,结合甲状腺彩超和甲状腺ECT检查,临床诊断Graves病明确。经过2月抗甲状腺药物治疗,胸腺瘤消失,但出现血糖急剧升高,伴有酮症酸中毒,胰岛功能丧失,GADA阳性,符合1型糖尿病、糖尿病酮症酸中毒诊断标准。
在外院住院过程中发生癫痫,经过血糖监测,排除了低血糖。但对脑电图和头颅磁共振检查异常未引起重视。第二次发作癫痫后来院治疗,排除了低血糖、各种细菌性脑炎、病毒性脑炎、中毒性脑炎、桥本脑病、中枢系统脱髓鞘疾病,最后诊断:自身免疫性多内分泌腺病综合征Ⅲ型、Graves病、自身免疫性边缘性脑炎(GAD介导)、胸腺瘤。
治疗经过:入院后予以甲巯咪唑片10mg,1次/日、左甲状腺素钠片25ug1/日;胰岛素泵持续输注胰岛素(赖脯胰岛素);免疫球蛋白20g,静脉滴注×5天,28天后免疫球蛋白10g,静脉滴注×5天。
第3月时复查脑脊液GAD>2000IU/ml。改用甲泼尼龙500mg,静脉滴注×5天,继以甲泼尼龙80mg,静脉滴注×14天,后予泼尼松45mg/天,每2周减5mg;硫唑嘌呤片50mg,2次/天;左乙拉西坦片500mg,2次/天,治疗3月仍有癫痫发作,复查脑脊液GAD仍强阳性,遂停用糖皮质激素,改用利妥昔单抗治疗,至今无癫痫发作,现仍在随访中。
知识拓展
01
1型糖尿病(T1DM)和自身免疫性甲状腺疾病(AITD)
T1DM和AITD是较为常见的自身免疫性内分泌疾病,均由器官特异性T淋巴细胞介导的针对机体内分泌组织的自身免疫攻击所致。当T1DM和AITD发生于同一个个体时,我们称之为APSⅢ型[1]。
本例以典型的高甲状腺激素血症的表现起病,检查符合AITD,继之出现典型糖尿病症状,胰岛素/C肽释放试验提示胰岛素缺乏、GAD阳性,符合T1ADM,APSⅢ型诊断明确。TIDM和AITD好发于同一个体,且具有家族聚集倾向,提示二者在遗传学发病机制上具有密切的联系[2]。
免疫调控异常是TIDM和AITD最根本的致病原因,遗传易患性也是通过免疫调控而发挥作用的。因而,免疫调节治疗是治疗T1DM和AITD的根本策略。APS合并Graves甲亢时,需用同位素或甲巯咪唑治疗,其中131I疗效较好,因为APS患者免疫反应强,药物治疗容易复发。
02
AITD与胸腺瘤
胸腺瘤是最常见的纵隔肿瘤之一。胸腺瘤的发生往往伴随着自身免疫耐受的丢失和自身免疫性疾病的出现,故胸腺瘤与多种自身免疫性疾病相关,包括重症肌无力、系统性红斑狼疮、低丙种球蛋白血症以及AITD等[3]。也有合并自身免疫性脑炎(AE)、边缘性脑炎(LE)的文献报道[4-5]。机制并不十分清楚。
有意思的是Lohwasser等[6]曾报道抗甲状腺药物卡比马唑治疗Graves病合并胸腺增大,甲状腺功能正常后CT检查提示前纵膈肿物消失。本例经甲巯咪唑治疗2月,也出现胸腺肿物消失的现象,可能与抗甲状腺药物对Graves病患者有较强的免疫抑制作用相关。
03
GAD介导的边缘性脑炎(LE)
APS亦可累及其他非内分泌系统,累及神经系统时可引起自身免疫性脑炎(AE)。AE中符合边缘性脑炎者,称为边缘性脑炎(LE)。目前AE患病比例占脑炎病例的10%~20%,以抗NMDAR脑炎最常见,约占AE患者的80%,而由GAD介导的边缘性脑炎较罕见。
GAD为抑制性神经递质,是γ氨基丁酸(GABA)合成的主要限速酶,有研究发现,该抗体属于T1DM的重要免疫标志物之一,且该抗体能介导边缘性脑炎,与机体出现持续性癫痫存在较强的相关性[7]。
其具体作用机制尚不明确,仅有一些动物体内、体外实验发现GAD抗体能够抑制氨基丁酸的释放,可能损伤神经元,干扰大脑神经递质的合成,从而引起神经性疾病的发生。
GAD抗体还可引起连续重复的肌肉活动,异常的条件发射,增强前角神经元的兴奋性;还可降低小脑核中NMDA介导的一氧化氮水平,减少谷氨酸的突触数目。GAD介导的边缘性脑炎的临床表现包括1型糖尿病相关症状、肌无力、精神行为异常、癫痫发作(起源于颞叶)和近记忆力障碍为主要症状,脑电图与神经影像学显示符合边缘系统受累,脑脊液检查提示炎性改变,本例主要表现为癫痫发作及脑电图改变。
诊断LE时需排除感染性疾病、代谢性与中毒性脑病、桥本脑病、中枢神经系统肿瘤、遗传性疾病、神经系统变性病等。GAD介导的边缘性脑炎的治疗参照自身免疫性脑炎,包括:免疫治疗、对症治疗、支持治疗、康复治疗,合并肿瘤者进行切除肿瘤等抗肿瘤治疗。
案例总结
现代医学以器官进行分科和诊治的医学模式在提高专科诊治水平中起了积极作用,但不可否认的是单纯以器官为中心的诊断思维模式不仅有碍于疾病的治疗,而且还会使我们偏离临床研究工作的大方向。
临床专科医师须具备良好的内科学基础和整合理念,临床诊断时须考虑各专业,由表及里,由此及彼,探讨疾病的内在联系,找出疾病的根源所在。自身免疫性疾病的全身表现已经突破了不同系统的界限,可以表现为多系统、多器官受累,临床表现复杂多样。
APS患者内分泌系统及非内分泌系统的受累常呈序贯性,而非同时发生,临床医生在疾病诊治中须具有整体观念和科学缜密的临床思维,以病人为中心,重视患者的所有临床表现,提出诊断思路。检验医师须与临床紧密结合,结合现代检验技术,积极开展相关检验项目,验证临床诊断,以避免漏诊、误诊,从而使患者得到及早治疗。
专家点评
检验点评
专家:祝进,温州医科大学附属衢州医院(衢州市人民医院)检验科主任、主任技师、硕士生导师。
点评意见:本病例初发以甲状腺功能亢进入院,继而影像学检查发现胸腺瘤,临床治疗效果良好。两个月后再次以糖尿病(1型糖尿病首先考虑)、Graves病、抽搐待查(癫痫考虑)、眼睑下垂(重症肌无力考虑)入院,出院时癫痫原因未明确。
两年后癫痫再次发作,通过解读实验室检查常用项目“抗谷氨酸脱羧酶抗体(GAD)”异常很好的串联了患者的临床过程,为最终诊断“自身免疫性多内分泌腺病综合征(APSⅢ型)合并边缘性脑炎(GAD介导)及胸腺瘤”提供了关键证据。
本病例诊治提示应用整合医学理念在临床诊疗过程中的重要性。检验医师了解现代检验技术,积极开展相关检验项目,紧密结合临床,利用专业知识解读检验结果,联合临床医师使本病最终得以确诊。本病例临床罕见,体现了实验室诊断结果在整合医学中对临床工作具有较高的指导价值。
临床点评
专家:李成江,浙江大学医学院附属第一医院内分泌主任医师、教授、硕士生导师,原内分泌科主任,浙江省医学会内分泌分会候任主任委员。
点评意见:自身免疫性多内分泌腺病综合征(APSⅢ型)合并边缘性脑炎(GAD介导)及胸腺瘤临床罕见,极易误诊和漏诊。在本病例诊治中,临床医生很好地应用整体观念和科学缜密的临床思维,以病人为中心,在常见内分泌疾病表现中重视细节,把内分泌疾病与自身免疫性疾病结合起来,提出诊断思路。检验医师须与临床紧密结合,结合现代检验技术,积极开展相关检验项目,抽丝剥茧,去伪存真,最终得以确诊,对临床工作具有较高的指导性,具有较高的临床研究价值。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#罕见#
33
#免疫性疾病#
41