JBC:Gadd45a蛋白引发人类骨骼肌萎缩
2012-08-15 T.Shen 生物谷
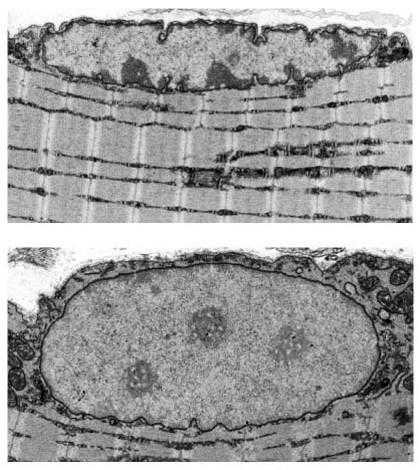
研究者发现了一种称为Gadd45a的蛋白质,其可以控制基因40%的活性来促使骨骼肌萎缩。而且研究者也研究了Gadd45a在骨骼肌细胞中进行的“恶劣勾当”,该蛋白质可以重新变成许多基因来引发细胞功能的混乱。 (Credit: Images courtesy of Christopher Adams lab, University of Iowa.) 你是否在为你慢慢变老,偶尔生病,遭受痛苦,眼看

研究者发现了一种称为Gadd45a的蛋白质,其可以控制基因40%的活性来促使骨骼肌萎缩。而且研究者也研究了Gadd45a在骨骼肌细胞中进行的“恶劣勾当”,该蛋白质可以重新变成许多基因来引发细胞功能的混乱。
(Credit: Images courtesy of Christopher Adams lab, University of Iowa.)
你是否在为你慢慢变老,偶尔生病,遭受痛苦,眼看着自己的肌肉萎缩松弛而沮丧?肌肉功能的衰退,无论是轻微的还是逐渐的,就像人类呼吸一样是一种人体的生理状态。尽管科学家们对于促使骨骼肌萎缩的原因知道的很少,但是他们知道这其中所参与的一些重要的效应蛋白质,刊登在近日的国际杂志Journal of Biological Chemistry上的一篇研究报告中,研究者发现了一种称为Gadd45a的蛋白质,其可以控制基因40%的活性来促使骨骼肌萎缩。而且研究者也研究了Gadd45a在骨骼肌细胞中进行的“恶劣勾当”,该蛋白质可以重新编程许多基因来引发细胞功能的混乱。
研究者Adams表示,如今我们发现了骨骼肌萎缩的一个关键分子机制,这将帮助我们开发出治疗骨骼肌萎缩病人的新型疗法。研究者集中研究蛋白质Gadd45a。之前的研究中,当骨骼肌受到了来自营养不良、神经损伤的压力的时候,骨骼肌会增加蛋白质ATF4的产生。这种蛋白质可以通过激活一系列基因来引发骨骼肌肌肉萎缩,但是具体机制并不清楚。
为了研究其分子机制,研究者进行了一系列实验来揭示ATF4的关键靶基因,结果揭示了ATF4可以通过激活Gadd45a基因来引发骨骼肌萎缩。深入研究揭示了Gadd45a并不需要其自身蛋白质来完成使骨骼肌萎缩的任务。意味着其并不依赖于ATF4途径。研究者表示,Gadd45a可以通过两种途径来影响骨骼肌,其引导骨骼肌细胞产生较少量的蛋白质,或者促使已经存在的蛋白质崩溃,最终结果就是引发骨骼肌萎缩。
研究小组试图发现Gadd45a如何来进行发挥作用,肌肉细胞的细胞核会因其形状发生改变而受压,当研究者将Gadd45a注射入肌肉细胞中时,肌肉细胞的细胞核便会像其受到压力一样发生形状改变。这就揭示了Gadd45a确实进入到了肌肉细胞的细胞核中来调节基因的表达和沉默。
Gadd45a可以通过增加mRNAs的水平来改变大约600个和肌肉萎缩相关的基因的表达,也就是40%的mRNAs都参与到了肌肉的衰退过程中。Gadd45a是肌肉萎缩的中央开关,如果你关闭了它,你就可以阻止肌肉萎缩的发生。相关研究由国立卫生研究院等机构支持。
编译自:Key Culprit Causing Muscle Atrophy Identified

doi:10.1074/jbc.M112.374777
PMC:
PMID:
Stress-induced Skeletal Muscle Gadd45a Expression Reprograms Myonuclei and Causes Muscle Atrophy*
Scott M. Ebert‡, Michael C. Dyle‡, Steven D. Kunkel‡§, Steven A. Bullard‡§, Kale S. Bongers‡, Daniel K. Fox‡, Jason M. Dierdorff‡, Eric D. Foster‡ and Christopher M. Adams‡§,1
Diverse stresses including starvation and muscle disuse cause skeletal muscle atrophy. However, the molecular mechanisms of muscle atrophy are complex and not well understood. Here, we demonstrate that growth arrest and DNA damage-inducible 45a protein (Gadd45a) is a critical mediator of muscle atrophy. We identified Gadd45a through an unbiased search for potential downstream mediators of the stress-inducible, pro-atrophy transcription factor ATF4. We show that Gadd45a is required for skeletal muscle atrophy induced by three distinct skeletal muscle stresses: fasting, muscle immobilization, and muscle denervation. Conversely, forced expression of Gadd45a in muscle or cultured myotubes induces atrophy in the absence of upstream stress. We show that muscle-specific ATF4 knock-out mice have a reduced capacity to induce Gadd45a mRNA in response to stress, and as a result, they undergo less atrophy in response to fasting or muscle immobilization. Interestingly, Gadd45a is a myonuclear protein that induces myonuclear remodeling and a comprehensive program for muscle atrophy. Gadd45a represses genes involved in anabolic signaling and energy production, and it induces pro-atrophy genes. As a result, Gadd45a reduces multiple barriers to muscle atrophy (including PGC-1α, Akt activity, and protein synthesis) and stimulates pro-atrophy mechanisms (including autophagy and caspase-mediated proteolysis). These results elucidate a critical stress-induced pathway that reprograms muscle gene expression to cause atrophy.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#JBC#
25
#萎缩#
30
#骨骼肌#
32
#肌萎缩#
32