日本大冢公司血管加压素受体拮抗剂托伐普坦(苏麦卡)在中国上市
2012-02-25 MedSci MedSci原创
2012年2月22日,选择性血管加压素(AVP)Ⅱ型受体(简称V2受体)拮抗剂托伐普坦(苏麦卡)上市会在上海召开。据悉,托伐普坦是全球范围内的首个血管加压素受体拮抗剂。此前,托伐普坦已获国家食品药品监督管理局(SFDA)正式批准,并开始在中国生产、销售。 血管加压素(AVP)又称抗利尿激素,在下丘脑合成,储存在垂体后叶,是调节人体水平衡最主要的激素。某些疾病会导致血管加压素水平异常增高,
2012年2月22日,选择性血管加压素(AVP)Ⅱ型受体(简称V2受体)拮抗剂托伐普坦(苏麦卡)上市会在上海召开。据悉,托伐普坦是全球范围内的首个血管加压素受体拮抗剂。此前,托伐普坦已获国家食品药品监督管理局(SFDA)正式批准,并开始在中国生产、销售。
血管加压素(AVP)又称抗利尿激素,在下丘脑合成,储存在垂体后叶,是调节人体水平衡最主要的激素。某些疾病会导致血管加压素水平异常增高,包括心衰、肝硬化、抗利尿激素分泌异常综合症(也称为SIADH),不同的病因其增高机理不尽相同。血管加压素增高增加水的重吸收,导致患者水肿和稀释性低钠血症。低钠血症会产生恶心、意识障碍、昏睡、注意力缺失、步态不稳和意外摔倒等症状。严重低钠血症可导致惊厥、昏迷、甚至死亡。
对于高容量性和等容量性低钠血症患者,目前并没有有效的治疗方法,临床上,限制液体摄入常被作为首选的方法。但限制液体摄入对病人而言是很难做到的,即便病人忍受痛苦严格遵守了限液医嘱,这种方法也只能提高血钠浓度不超过3~4 mEq/L。对于有肝腹水和心衰的患者,不建议滴注高渗盐水来纠正低钠血症,因为这样会加重患者的高容量状况,恶化病情的进展。现有的利尿剂均是通过抑制钠的重吸收而增加尿量,故在低钠血症时是不推荐使用的,也没有任何利尿剂被批准可在低钠血症时应用。
据介绍,托伐普坦是日本大冢公司原研的全新选择性血管加压素Ⅱ型受体(简称为V2受体)拮抗剂,它是世界上首个口服普坦类药物,也将是中国市场第一个和唯一的V2受体拮抗剂,可用于治疗由于肝硬化、心衰、SIADH所导致的高容量性和正常容量性低钠血症,并可改善患者的高容量状况。
托伐普坦与V2受体的亲和力是天然血管加压素的1.8倍,故可拮抗血管加压素作用,抑制水的重吸收,增加不含电解质的自由水排出,能有效纠正高容量和等容量性低钠血症,并且同时纠正高容量患者的水肿症状。国内外多个临床试验均证明了托伐普坦的有效性和安全性。患者口服后2~4小时就出现排水作用和血钠浓度增高,8小时后血钠与对照组相比显著增高,在至少1年的研究期内,患者血钠水平得以维持,常见的不良反应(5%)为口干和口渴。在中国进行的注册临床试验也验证了国外临床试验结果。
拓展知识:
美国FDA于2009年5月19日批准了日本大冢制药(Otsuka Pharm)的新分子化合药——托伐普坦片(Tolvaptan Tablets,商品名:Samsca)用于治疗高容或等容性低钠血症伴心力衰竭、肝硬化、抗利尿激素分泌异常综合征。
英文名】tolvaptan Tablet
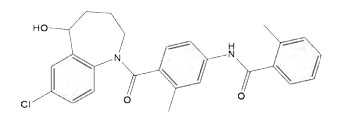
【化学名】N-[4-[(5R)-7-氯-5-羟基-2,3,4,5-四氢-1-苯并氮杂卓-1-甲酰基]-3-甲基苯基]-2-甲基苯甲酰胺。
【分子式】C26H25ClN2O3
【分子量】448.94
【主要成分】托伐普坦
【性状】白色片剂。
【适应症】治疗由充血性心衰、肝硬化以及抗利尿激素分泌不足综合征导致的低钠血症。
【用法用量】15mg/片,一次/日。或遵医嘱。
【药理毒理】一种血管加压素V2受体拮抗药(非肽类AVP2受体拮抗剂),可以升高血浆中钠离子浓度,帮助多余的水分从尿液排出。增强肾脏处理水的能力。多囊肾细胞内环磷酸腺苷(cAMP)积聚,其通过刺激囊液分泌和内衬细胞增生促进囊肿生长。托伐普坦是2型加压素受体拮抗剂,可抑制cAMP生成和聚积。在多种PKD动物模型研究中,托伐普坦显示出良好疗效。
【不良反应】口干、渴感、晕眩、恶心、低血压等。
【规格】15mg;30mg;60mg/片
【生产企业】日本大冢制药公司
{nextpage}
附录
|
动物 |
性别 |
经口 mg/kg |
|
大鼠( SD ) |
雄 |
>2000 |
|
雌 |
>2000 | |
|
狗( Beagle ) |
雄 |
>2000 |
|
雌 |
>2000 |
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








太贵了……
117
太贵。治病需要,求购
184
此药片颜色
142
#托伐普坦#
54
求购苏麦卡
129
#血管加压#
36
#加压素#
27
#苏麦卡#
33
#日本#
28
#拮抗剂#
38