对“非标准”产科抗磷脂综合征的进一步认识:2例病例报道
2023-04-05 岳静 柔济免疫 发表于上海
在此研究中分享了两例具有潜在致死性的NOAPS病例,她们并发严重先兆子痫、胎儿生长受限、肝破裂、早产、难治性复发性流产甚至死产。
抗磷脂综合征(APS)是一种获得性自身免疫性疾病,其特征是反复出现血栓形成和/或妊娠并发症,且抗磷脂抗体(aPL)升高。当血栓形成为主要临床表现时,称为血栓性APS(TAPS),当病理性妊娠为主要临床表现时,称为产科APS(OAPS)。确诊OAPS需要存在一个或多个典型的临床标准和至少相隔12周的持续aPL阳性。然而,部分OAPS患者仅符合APS诊断标准中的临床标准或实验室标准,被称为非标准OAPS(NOAPS)。在此研究中分享了两例具有潜在致死性的NOAPS病例,她们并发严重先兆子痫、胎儿生长受限、肝破裂、早产、难治性复发性流产甚至死产。
病例1
例1为36岁女性,怀孕28 + 1周,G2P0,既往有人工流产史。因突发血压升高,入本院急诊科就诊。患者既往病史无异常。此次怀孕接受了定期的产前检查,无异常。然而,她在 1 周前出现双下肢水肿,发现血压为 140-150/90-100 mmHg。自诉没有头晕、头痛或视力障碍。在急诊室,患者尿蛋白3+,血压170/94mmHg,初步诊断为“重度先兆子痫”并紧急入院。
表1展示了在住院期间患者的实验室结果。产科超声显示,相应妊娠周内胎儿生长明显减慢,考虑胎儿生长受限(FGR)。免疫分析表明与APS和干燥综合征(SS)相关的aβ2GPI-IgG/IgM、ANA、抗 SSA和抗 Ro52自身抗体升高。虽然病人既往没有妊娠并发症史,但在这次妊娠中诊断出严重的先兆子痫和FGR。结合实验室检查,考虑继发于某些自身免疫性疾病的NOAPS。给予“泼尼松20mg 口服 qd,他克莫司0.5mg 口服 qd,羟氯喹200mg口服 qd,阿司匹林100mg 口服qd,低分子肝素4000IU 皮下注射q12h”治疗。
在怀孕31周时,患者突然出现持续腹痛,伴随血压和血红蛋白水平的降低。紧急超声显示大量腹腔积液。考虑到腹膜内出血的风险,立即进行了紧急剖腹手术。在手术过程中,腹腔内可见大量血液积聚(约2,800毫升)和血凝块,但没有子宫破裂或胎盘早剥的迹象。通过紧急剖宫产分娩了一名1030克的女婴。Apgar得分分别为 3-6-8 分,被转移到新生儿重症监护室。外科医生仔细检查并发现胆囊底部下方的肝脏表面有1.5厘米的破裂伴有活动性出血(图1)。手术后,患者被送往ICU病房进一步治疗。患者恢复良好,8天后出院,新生儿康复3周后出院。然后建议患者在分娩后继续使用低分子肝素4000IU 皮下注射 qd,持续6 周。
分娩三个月后,患者在内科重新进行了评估。结果显示 Schirmer 试验呈阳性,aPL、ANA(均质模式)、抗 SSA(Ro) 和抗 Ro52 抗体持续升高。患者被诊断为继发于SS的OAPS。

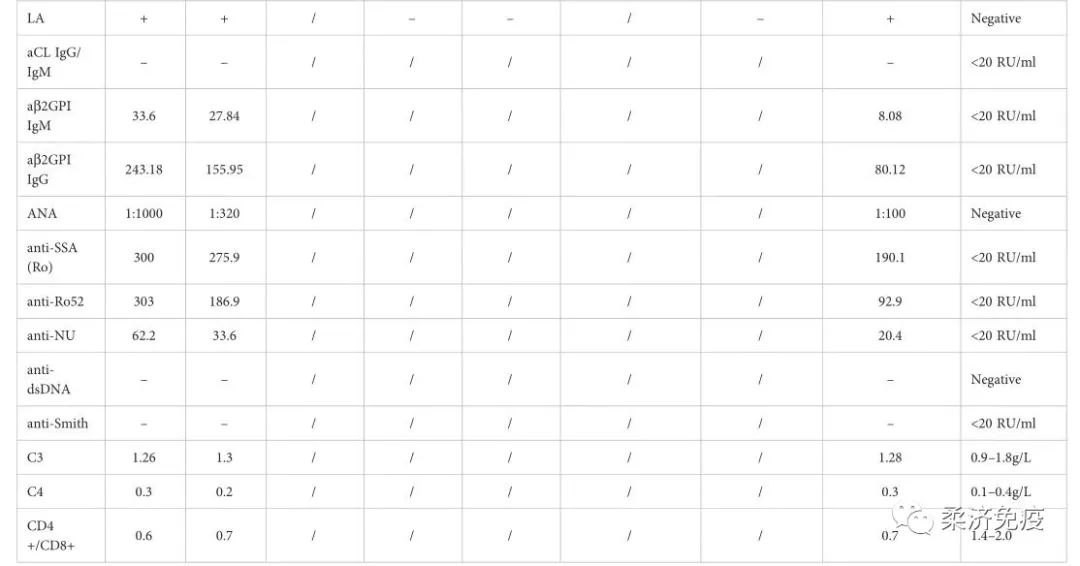
表1. 患者住院期间实验室结果

图1. “△”代表胆囊;“→”代表肝破裂
病例2
例2是一名31岁女性,怀孕30+4周,G6P1,既往连续4次流产(表2)。患者既往检查发现高滴度的抗磷脂酰乙醇胺(aPE)抗体。标准aPL、血栓形成(如蛋白C/S缺乏症和抗凝血酶III缺乏症)和其他自身免疫性疾病(如SLE和SS)的筛查结果均为阴性。此外,还排除了胚胎非整倍体、感染性疾病、子宫畸形、双亲染色体异常和母体内分泌疾病。
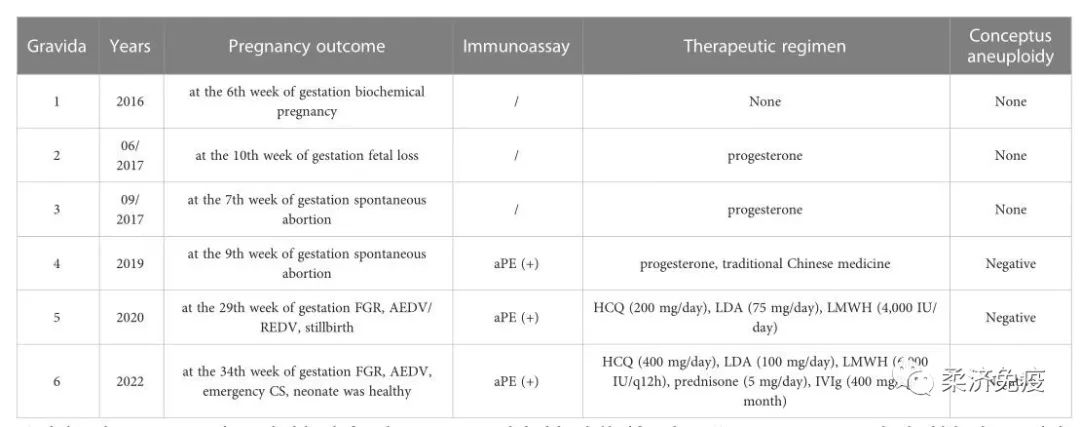
表2.患者既往流产史
由于不明原因的复发性流产和 aPE 阳性,在患者第五次妊娠前诊断为NOAPS。因此,在确认早孕时,开始予“羟氯喹200mg/天,阿司匹林75mg/天和低分子肝素4000 IU /天”治疗。尽管如此,脐动脉血流的彩色多普勒检查显示,妊娠 21 周时舒张末期流速(AEVD)消失/逆转。随着胎儿胎盘循环阻力的升高,胎儿生长也明显延迟。胎儿病情急剧恶化,患者拒绝终止妊娠,直到胎儿在怀孕第29周时胎死宫内。死胎没有明显的畸形,胎儿基因芯片分析也正常。尚无胎儿和胎盘的组织学评估。
在这次怀孕之前,标准aPLs仍然为阴性,但aPE持续呈阳性(表3列出了患者此次怀孕前后的实验室检查),考虑诊断为难治性和血清阴性OAPS,在长期HCQ治疗的基础上,患者确认怀孕时,给与“羟氯喹400mg /天,阿司匹林100mg /天,低分子肝素6000 IU / q12h和泼尼松5mg /天的治疗。此外,从妊娠第六周开始,以400mg / kg /月的剂量开始预防性免疫球蛋白联合治疗(每月连续两天15g)。
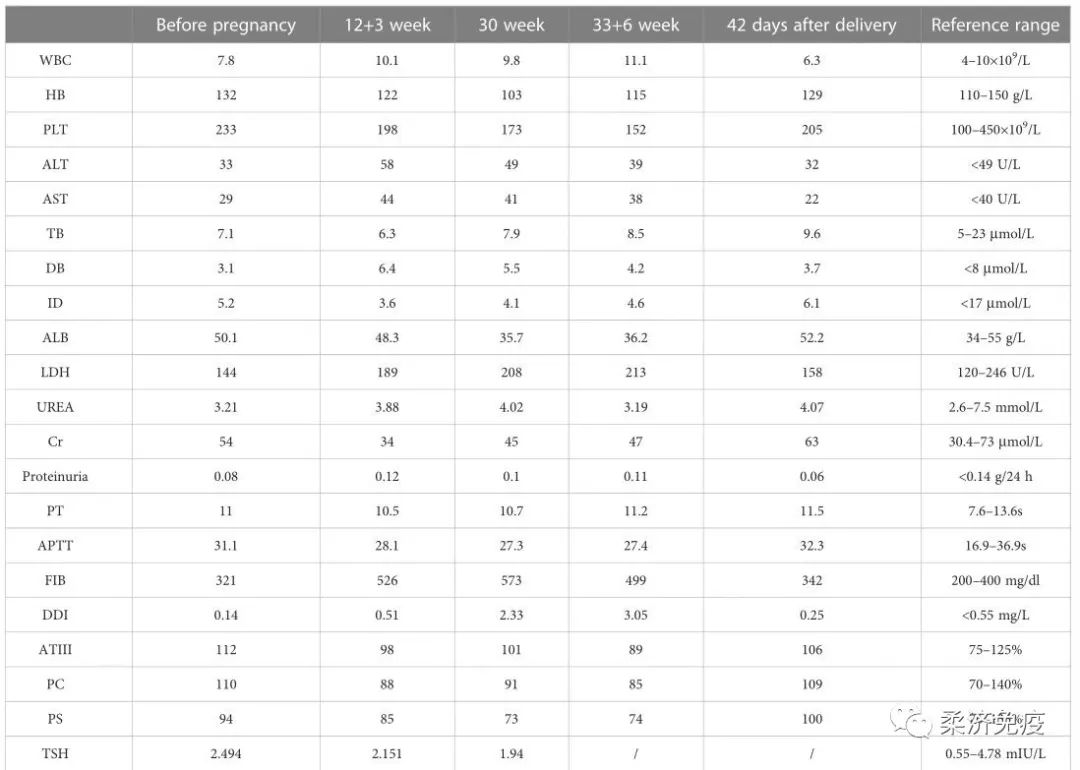

表3.患者怀孕前后的实验室检查
妊娠30周时,彩色多普勒超声显示胎儿生长指数小于相应胎龄的10%,AEVD呈间歇性。胎儿染色体微阵列分析未发现异常。在妊娠34周时,由于胎心无反应性和持续的AEVD,进行了紧急剖宫产术,并分娩了一名体重1900g的女婴,其Apgar评分分别为8-9-10分。母亲在术后第三天出院。分娩后继续服用低分子肝素4000IU/天持续1周。在产后6个月的评估中,母亲或孩子没有任何并发症。在随访期间(个月),患者没有出现任何活动性全身疾病的体征或症状,孩子健康。
临床上,有些妇女仅符合与OAPS相关的临床标准,但不符合实验室标准,包括aPL阴性或仅具有低滴度的aPL,或仅有一次或间歇性的aPL阳性,或“非标准”aPL阳性,这些患者被称为血清阴性APS或非标准OAPS。这里报告的两例病例都是罕见但可能致命的非标准OAPS,导致严重的先兆子痫,FGR,早产,肝破裂,复发性流产,甚至死产。因此,建议对早发性重度先兆子痫和/或复发性流产史的女性进行仔细评估,并在整个妊娠期间密切监测,以更好的改善此类患者的妊娠结局。
参考文献
Peng X, Tan X, Xing A. An advanced understanding of the heterogeneous clinical features of "non-criteria" obstetric antiphospholipid syndrome: Two case reports and a literature review. Front Immunol. 2023 Feb 14;14:1122127.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












学习了,谢谢分享
39