Nature:为何癌症免疫疗法副作用频出?最新研究发现PD-1全新作用
2023-06-25 王聪 “生物世界”公众号 发表于上海
PD-1阻断剂通常会导致T细胞攻击癌细胞之外的健康组织,造成严重、甚至危及生命的副作用,从而削弱癌症免疫疗法的益处。
以免疫检查点抑制剂为代表的癌症免疫疗法改变了癌症治疗格局,其中,阻断PD-1或PD-L1的抗体已经被批准用于治疗超过25种不同的癌症。
PD-1(程序性细胞死亡受体-1),其位于T细胞表面,而位于肿瘤细胞表面的PD-L1(程序性细胞死亡配体-1),PD-L1通过与PD-1的结合,促使肿瘤细胞获得免疫逃逸。因此,通过抑制剂来阻断PD-1与PD-L1之间的结合,能够帮助T细胞重新获得杀伤肿瘤的能力。
然而,PD-1阻断剂通常会导致T细胞攻击癌细胞之外的健康组织,造成严重、甚至危及生命的副作用,从而削弱癌症免疫疗法的益处。
2023年6月21日,耶鲁大学 Nikhil Joshi 团队在 Nature 期刊发表了题为:PD-1 maintains CD8 T cell tolerance towards cutaneous neoantigens 的研究论文。
这项最新研究揭示了PD-1在健康组织中发挥着组织稳态“看门人”的作用,因此,阻断PD-1的免疫疗法会扰乱这一作用,从而导致免疫相关不良事件的发生。这些发现可以帮助科学家预测、治疗甚至预防PD-1阻断剂免疫疗法的副作用。

虽然我们已经知道为什么阻断检查点受体会增强抗癌免疫反应,但还不清楚为什么这些免疫疗法也会在正常器官中引起不良事件。这些不良事件的出现表明,像PD-1这样的检查点受体持续保护了正常个体的健康组织免受免疫攻击。
目前,医生们还无法预测哪些患者在接受免疫治疗时会出现这些副作用,哪些健康器官会因免疫疗法而遭受攻击。这些副作用可能导致医生不得不暂停癌症患者的免疫治疗,这对免疫治疗的抗癌效果产生负面影响。
论文通讯作者、耶鲁大学免疫生物学副教授 Nikhil Joshi 表示,这项研究首次表明,PD-1在阻止T细胞攻击健康个体的正常组织方面发挥关键作用,这一发现可能有助于找到减少或预防免疫治疗副作用的方法。
我们的外周T细胞库包含有自身反应性T细胞(self-reactive T cells),也就是会攻击自身细胞、组织和器官的T细胞。免疫检查点受体,例如PD-1,被认为能够抑制自身反应性CD8 T细胞,从而诱导外周免疫耐受。然而,接受接受检查点抑制剂治疗癌症患者高频出现免疫相关不良事件,对这一观点提出了挑战。
在这项研究中,研究团队开发了新一代小鼠模型,以解决PD-1在阻止T细胞攻击健康皮肤中的作用。在该模型中,表皮中皮肤特异性表达的T细胞抗原会引起抗原特异性CD8 T细胞的局部浸润,这些细胞具有效应基因表达谱。
在这种情况下,PD-1通过阻止组织浸润性抗原特异性效应CD8 T细胞(1)获得功能完备的致病分化状态,(2)分泌大量效应分子,以及(3)进入表皮抗原表达细胞,从而维持皮肤耐受性。
然后,研究团队通过阻断PD-1来模拟免疫疗法,发现表皮抗原表达细胞被抗原特异性CD8 T细胞消灭,导致小鼠出现了一些与接受PD-1阻断剂治疗的癌症患者相同的皮肤疾病。研究团队还对正在接受治疗的癌症患者的皮肤活检进行了分析,结果显示,他们在病变和非病变皮肤中都存在克隆扩增效应CD8 T细胞,这进一步证实了小鼠实验中的数据。
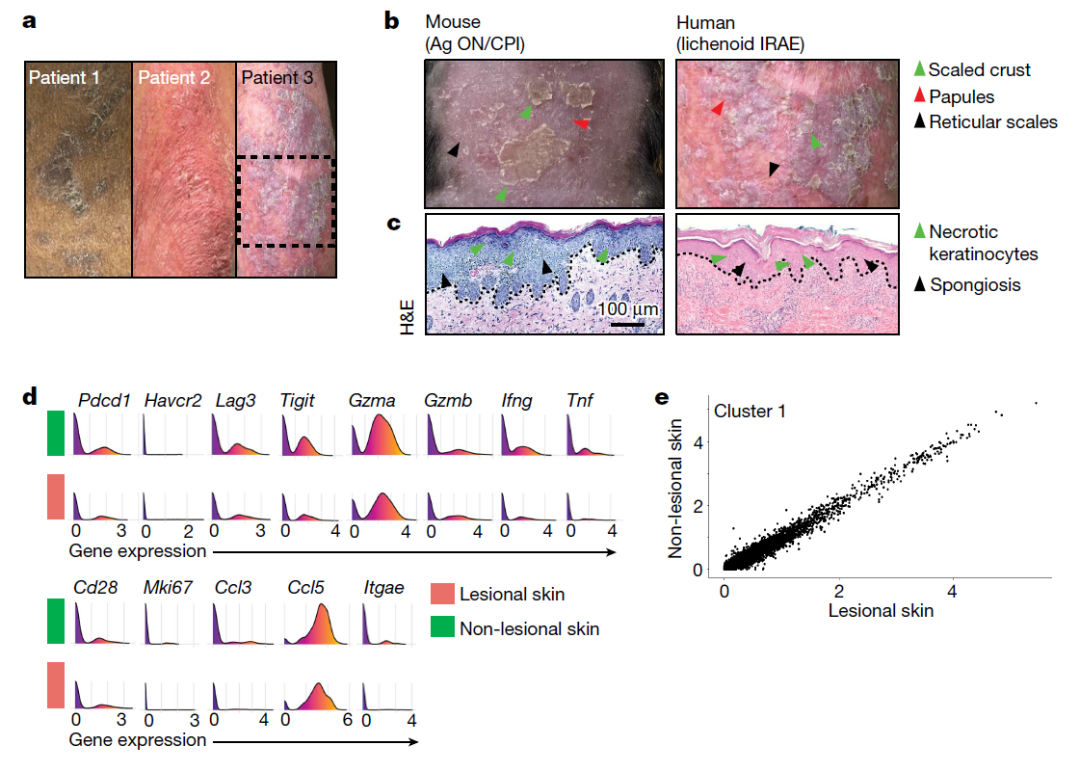
细胞毒性CD8 T细胞也存在于健康皮肤中,可能是免疫治疗时发生皮肤免疫相关不良事件的驱动因素
这些在小鼠和人类身上的实验数据支持一个新的观点——像PD-1这样的免疫检查点受体通过允许外周抗原特异性效应CD8 T细胞与无免疫病理组织中的抗原表达细胞共存,从而起到组织稳态看门人的作用。而PD-1阻断免疫疗法会干扰这些生理调节功能,从而导致不良事件。
这项研究为未来发展和改进免疫疗法以避免不良事件奠定了基础。
原始出处:
Damo, M., Hornick, N.I., Venkat, A. et al. PD-1 maintains CD8 T cell tolerance towards cutaneous neoantigens. Nature (2023). https://doi.org/10.1038/s41586-023-06217-y.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










、一六学7可了
35
谢谢分享
44