Nature Methods:革命性的CRISPR-CasRx筛选平台:开启癌症基因组新篇章
2024-03-01 生物探索 生物探索 发表于上海
开发高效、系统的技术平台,对lncRNA进行全基因组规模的功能筛选,对于揭示其在生理和病理过程中的作用至关重要。
引言
长非编码RNA(lncRNA)是一类长度超过200个核苷酸的RNA分子,它们不编码蛋白质,但在细胞的各种生理和病理过程中发挥着至关重要的调控作用。近年来,随着高通量测序技术的发展,研究人员逐渐揭示了lncRNA在基因表达调控、细胞分化、以及疾病发生发展中的重要作用,尤其是在癌症的发生机制中,lncRNA的异常表达与肿瘤的发生、发展、转移和药物耐药性密切相关。
尽管lncRNA的功能研究取得了显著进展,但目前已知的lncRNA功能仅占其总数的一小部分,大多数lncRNA的生物学功能仍然是未知的。这主要是因为lncRNA的表达具有高度的组织特异性和时空特异性,加之lncRNA本身的结构复杂多变,给功能性研究带来了巨大的挑战。因此,开发高效、系统的技术平台,对lncRNA进行全基因组规模的功能筛选,对于揭示其在生理和病理过程中的作用至关重要。2月26日Nature Methods报道的CRISPR-CasRx筛选平台为lncRNA的研究带来了新的方法,“Genome-scale pan-cancer interrogation of lncRNA dependencies using CasRx”。
近年来,基于CRISPR-Cas系统的基因编辑技术已成为生物学研究的重要工具。特别是CasRx(一种属于Cas13家族的RNA编辑工具),因其高效、特异性强的RNA靶向编辑能力,为lncRNA的功能研究提供了新的可能。与传统的DNA靶向的CRISPR-Cas9系统相比,CasRx直接作用于RNA,能够绕过lncRNA与编码基因重叠或靠近的限制,从而实现对lncRNA精准的功能性干预。此外,CasRx技术的应用,不仅可以帮助研究人员高效地筛选和验证与癌症等重大疾病相关的关键lncRNA,还能为后续的疾病机理研究和新药物开发提供强有力的支持。

lncRNA功能筛选的新方法:CasRx系统
Cas13d/CasRx
随着基因组科学的迅速发展,特别是在长非编码RNA(lncRNA)研究领域,研究人员迫切需要一种能够精确操作RNA分子的技术平台。CasRx系统,基于Cas13d,为我们提供了这样一种可能性。Cas13d是一种属于CRISPR-Cas系统的RNA导向的核酸酶,能够在RNA水平上实现高效、特异性的基因沉默。
Cas13d/CasRx技术的原理基于RNA干预机制,不同于传统的CRISPR-Cas9技术针对DNA进行编辑。CasRx系统通过设计特异性的导向RNA(gRNA),识别并靶向特定的lncRNA分子,进而触发Cas13d的切割活性,实现对目标lncRNA的精确沉默或编辑。
技术特点:
高特异性:CasRx系统可以通过设计特定的gRNA精确靶向特定的lncRNA序列,极大地减少了非特异性靶向的可能性。
操作简便:与DNA水平的基因编辑相比,RNA水平的编辑无需考虑细胞的修复机制,操作更为简便。
广泛适用:CasRx技术不受细胞类型的限制,适用于多种细胞和组织,为lncRNA功能研究提供了广阔的应用前景。
应用潜力:
功能基因组学研究:CasRx技术可以用于系统性地研究lncRNA在不同生物学过程中的功能,揭示其在疾病中的作用机制。
疾病治疗:针对与疾病相关的lncRNA进行靶向干预,为发展新的治疗策略提供了新思路。
基因治疗:利用CasRx技术进行RNA水平的编辑,为某些遗传性疾病的基因治疗提供了可能。
开发适用于全基因组lncRNA转录组筛选的CasRx平台
CasRx技术应运而生,为lncRNA的研究提供了新的视角。CasRx平台的开发,标志着我们在全基因组规模上对lncRNA进行功能筛选的能力迈出了重要一步。这一平台利用Cas13d的高特异性RNA靶向能力,结合系统生物学和高通量测序技术,能够在全基因组范围内快速、准确地识别和验证与疾病相关的lncRNA。
平台的核心组成包括:
高通量测序技术:为了实现对大量lncRNA的同时筛选,该平台采用了最新的高通量测序技术,保证了数据的准确性和高效性。
精准的gRNA设计:通过先进的生物信息学算法,为每个目标lncRNA设计特异性高的gRNA,确保了编辑的准确性和效率。
高效的Cas13d表达系统:优化的载体和表达系统保证了Cas13d在细胞中的高效表达和活性,使得RNA的编辑更为高效和稳定。
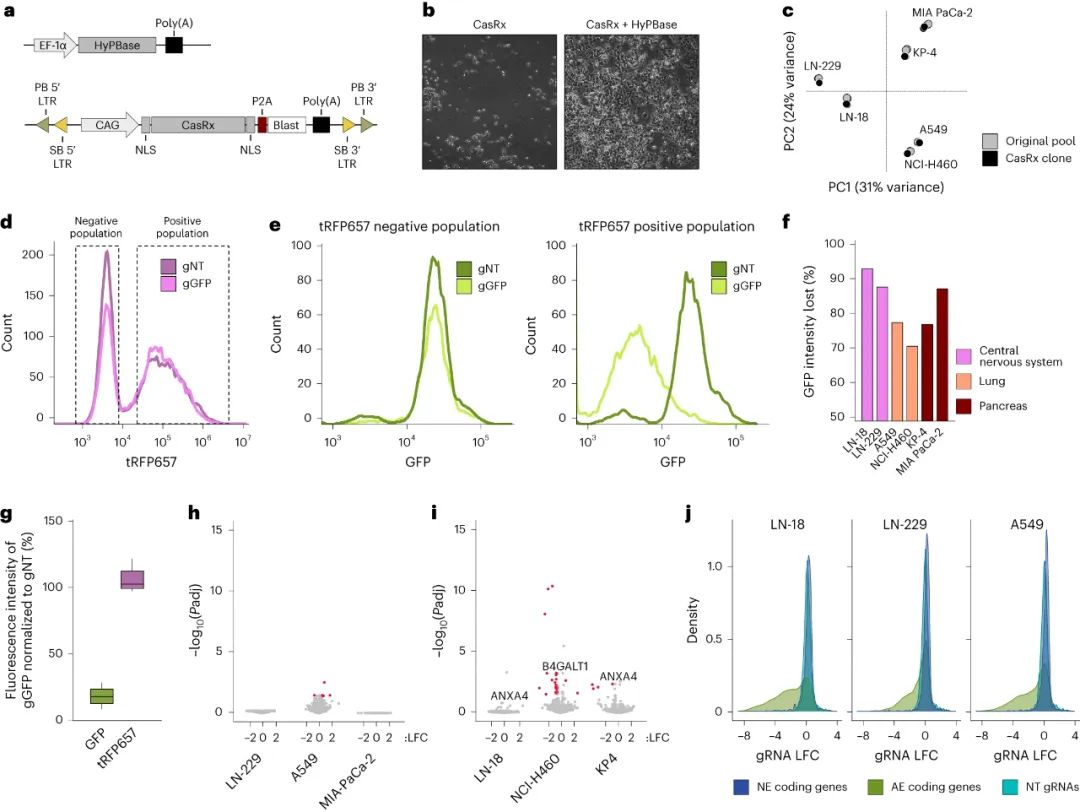
CasRx系统的优化(Credit: Nature Method)
平台的开发优势:
广泛的应用范围:不受细胞类型和组织来源的限制,可广泛应用于各种生物学和医学研究。
高效的筛选能力:能夠在短时间内对成千上万的lncRNA进行功能筛选,极大地提高了研究效率。
深入的功能解析:结合后续的生物信息学分析,可以深入理解筛选出的lncRNA的功能和作用机制。
利用CasRx克服以往筛选方法的限制
传统的lncRNA功能筛选方法存在许多限制,如特异性差、效率低、操作复杂等。CasRx技术的出现,有效地解决了这些问题。通过RNA水平的靶向编辑,CasRx技术避免了DNA水平编辑可能引起的基因组不稳定性,同时其高特异性和高效性使得lncRNA的功能筛选更加准确和快速。
特异性强:通过精确设计的gRNA,CasRx可以特异性地靶向和编辑目标lncRNA,减少了非特异性编辑的风险。
操作简便:相比于DNA水平的编辑,RNA水平的编辑操作更为简便,无需考虑细胞修复机制的干扰。
安全性高:由于CasRx作用于RNA水平,不涉及DNA的直接修改,因此安全性更高,避免了潜在的基因组不稳定问题。
全癌症范围内lncRNA依赖性的系统探索
Albarossa多路复用gRNA库的设计
在全基因组范围内对lncRNA依赖性进行系统探索的过程中,Albarossa多路复用gRNA库的创新设计成为了这一研究领域的重要突破。该库采用了一种独特的策略,将高效的CasRx技术与精密的gRNA设计相结合,以实现对全基因组lncRNA的高通量和高特异性筛选。
设计的核心:
精准的靶点选择:通过深入分析lncRNA的表达模式、功能预测以及在不同癌症中的差异表达,优先选择那些具有潜在生物学重要性和疾病相关性的lncRNA作为靶点。
多路复用gRNA设计:每个靶标lncRNA均设计多对gRNA,以增强编辑效率并降低假阴性结果的风险。这种多路复用设计不仅提高了筛选的覆盖率,也增加了结果的可靠性。
跨癌症类型的应用广泛性:Albarossa库在设计时充分考虑了不同癌症类型中lncRNA表达的异质性,确保了其在全癌症范围内的广泛适用性。
设计过程的创新点:
高级生物信息学分析:利用最新的生物信息学工具和算法,对海量的公共和专有数据进行深入分析,以指导gRNA的设计和优化。
综合表达水平和保守性:在选择靶点时,同时考虑lncRNA的表达水平和序列保守性,优先选择那些在多种癌症中高表达且序列高度保守的lncRNA,以提高筛选的效率和成功率。
功能性筛选与验证一体化:Albarossa库的设计不仅侧重于功能性筛选,还包括了后续的验证步骤,确保筛选出的lncRNA能够在后续实验中快速验证其功能和作用机制。
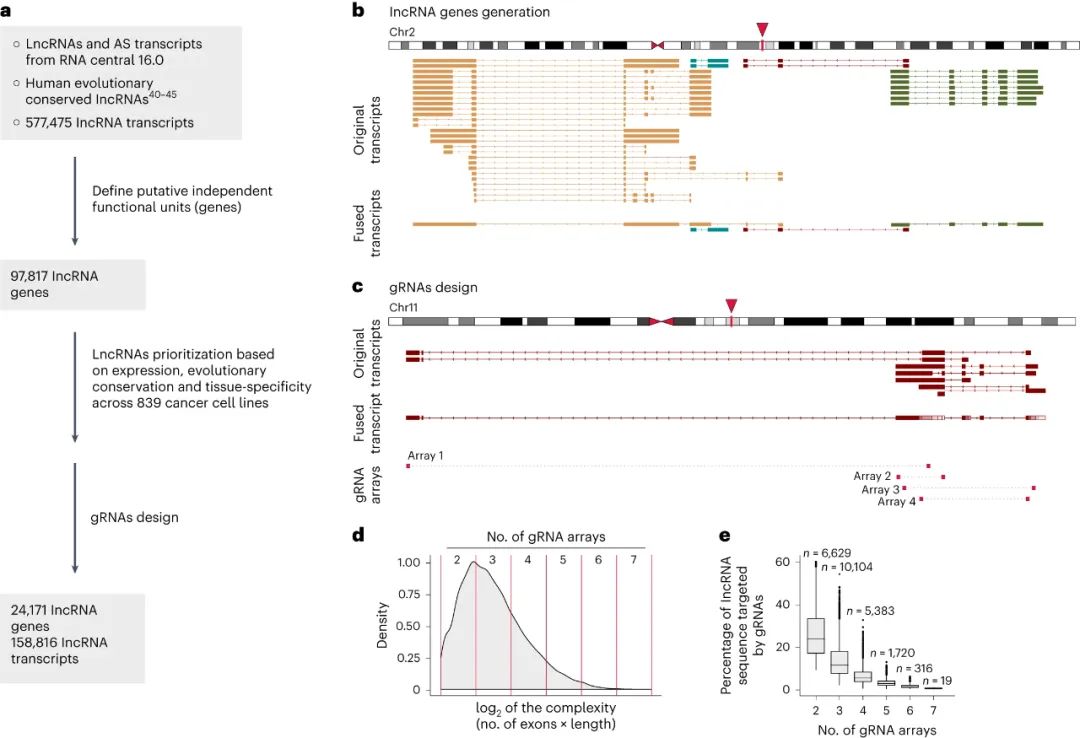
CasRx库的构建(Credit: Nature Methods)
Albarossa库的设计考虑到了lncRNA表达的组织特异性,通过精心挑选和设计gRNA,针对性地靶向那些在特定癌症中高表达的lncRNA。这种方法不仅提高了筛选的准确性,也极大地增强了其在不同癌症研究中的适用性。
通过对筛选结果和相关分子、表型数据的综合分析,研究人员能够揭示lncRNA在不同癌症进程中的作用机制,识别出可能的癌症驱动lncRNA,为后续的功能验证和临床应用打下坚实的基础。此外,这一策略还有助于发现新的癌症治疗靶点,为癌症患者提供更为个性化和有效的治疗方案。
筛选结果的分析与解读
识别出的背景特异性和共有的lncRNA依赖性
在进行全基因组lncRNA功能筛选的研究过程中,研究人员利用CasRx技术精确地靶向并敲低特定的lncRNA,从而探究它们在不同癌症背景下的作用。通过对筛选结果的深入分析,能够揭示lncRNA在多种癌症中的背景特异性依赖性和共有依赖性,这一发现为理解lncRNA的生物学功能和其在癌症发展中的角色提供了新的视角。
背景特异性依赖性的识别
背景特异性依赖性指的是某一lncRNA在特定癌症背景下显示出的必需性,而在其他类型的癌症中则不是必需的。这种依赖性的发现,揭示了lncRNA与癌症特定生物学过程之间的密切关系。例如,研究人员发现某些lncRNA仅在肺癌细胞中扮演关键角色,而在乳腺癌和结直肠癌中则不表现出相同的作用,这种现象可能与不同癌症类型中的信号通路活性或基因表达背景有关。
共有依赖性的发现
与此同时,研究人员也观察到一些lncRNA在多种癌症模型中均显示出依赖性,这类lncRNA可能参与了癌症发展的共通机制,如细胞周期调控、凋亡抑制等。这些共有依赖性的lncRNA为我们提供了潜在的广谱癌症治疗靶点,其抑制可能对多种癌症类型产生疗效。
筛选结果的深入分析
通过对筛选结果进行深入分析,研究人员能够根据lncRNA的背景特异性和共有依赖性,对它们进行分类,进而深入理解其在癌症中的作用机制。此外,这些分析结果还能帮助我们识别出对于特定癌症治疗潜在重要的lncRNA,为后续的功能研究和临床应用提供了重要指导。
结果验证:独立gRNA实验与细胞竞争实验
为确保筛选结果的准确性和可靠性,研究人员采用了两种关键的验证方法:独立gRNA实验和细胞竞争实验。这些方法帮助其进一步确认筛选出的lncRNA目标的功能重要性及其在癌症发展中的作用。
独立gRNA实验
在这一步骤中,研究人员选择了筛选过程中识别出的关键lncRNA目标,并设计了新的独立gRNA,以独立于初始筛选实验进行敲低。这种方法的目的是排除偶然性和特定gRNA可能导致的非特异性效应,从而增强结果的可信度。通过比较敲低效率和细胞表型的变化,能够验证这些lncRNA的确对癌症细胞的生存和增殖具有重要影响。
细胞竞争实验
此外,研究人员还进行了细胞竞争实验,以模拟更接近生理状态的环境。在这些实验中,敲低特定lncRNA的细胞与未处理的野生型细胞混合培养。通过监测一段时间后,敲低细胞在群体中的比例变化,可以直观地评估敲低特定lncRNA对细胞竞争力的影响。细胞竞争实验的结果提供了直接的证据,证明特定lncRNA在维持癌细胞竞争优势中的作用。
筛选命中靶标的功能分类和潜在的生物学意义
通过对筛选命中的lncRNA目标进行深入分析,研究人员能够将这些lncRNA进行功能分类,并探讨它们的潜在生物学意义。这些lncRNA广泛参与调控细胞生长、凋亡、迁移、侵袭以及细胞周期等多种重要生物学过程。
功能分类
将筛选出的lncRNA根据它们在癌症发展中的作用进行分类,如促进肿瘤生长、抑制细胞凋亡、调控细胞周期等。此外,还发现一些lncRNA通过影响细胞的代谢途径和信号传导路径来执行其功能,揭示了lncRNA在癌症发展中复杂的调控网络。
潜在的生物学意义
这些功能分类不仅有助于我们理解lncRNA在癌症发展中的作用机制,还为未来的癌症治疗提供了新的靶点。特别是那些在多种癌症类型中都显示出关键作用的lncRNA,可能成为广谱抗癌策略的重要组成部分。此外,对于那些具有背景特异性作用的lncRNA,它们可能为特定癌症类型提供精准治疗的可能性。
CasRx筛选技术在lncRNA研究中的创新与影响
CasRx筛选技术的开发和应用,标志着lncRNA功能研究领域的一个重大突破。这一技术不仅极大地提高了lncRNA功能筛选的效率和精确性,而且为深入理解lncRNA在癌症发展中的角色开辟了新的途径。通过全基因组规模的筛选,CasRx技术揭示了大量之前未知的、与癌症进程密切相关的lncRNA,为癌症生物学研究提供了新的视角和数据资源。
面临的挑战和未来的方向
尽管CasRx筛选技术在lncRNA研究中显示出巨大潜力,但仍面临一些挑战和局限性。例如,筛选过程中对gRNA设计的高度依赖可能导致特定lncRNA的敲除效率不一,影响最终结果的准确性。此外,筛选平台的优化、数据分析方法的提升以及筛选结果的生物学验证也是未来需要进一步改进的方向。
为了克服这些挑战,未来的研究可能需要集中于提高gRNA设计的精确性,开发更高效的数据分析工具,以及采用更严格的生物学验证流程。同时,引入机器学习和人工智能技术,可能为筛选过程提供更高效、更精确的策略。
对癌症治疗策略的潜在贡献
CasRx筛选技术在lncRNA研究中的应用,不仅为理解lncRNA的生物学功能提供了新的工具,也为癌症治疗策略的发展提供了新的思路。筛选出的lncRNA目标,特别是那些在多种癌症类型中显示出重要作用的lncRNA,有潜力成为新的治疗靶点。此外,通过深入分析lncRNA的功能网络,可能揭示出新的治疗机制,为癌症患者提供更有效的治疗选项。
Q&A
CasRx技术与CRISPR-Cas9技术有何不同?
CasRx技术基于CRISPR-Cas13系统,专门针对RNA进行编辑,而CRISPR-Cas9技术则是针对DNA的编辑。这意味着CasRx可以在不改变基因组DNA的情况下,精准地调控RNA的表达,为研究RNA功能和RNA相关疾病提供了新的工具。
如何确保筛选结果的准确性和可重复性?
确保筛选结果的准确性和可重复性,需要通过严格的实验设计、高质量的gRNA设计,以及精确的数据分析方法。此外,通过使用独立的验证实验,比如独立的gRNA实验和细胞竞争实验,可以进一步验证筛选结果的可靠性。
lncRNA在癌症发生发展中的作用是什么?
lncRNA在癌症的发生发展中扮演着多种角色,包括调控基因表达、参与表观遗传调控、影响细胞增殖和凋亡等。特定的lncRNA可以作为肿瘤抑制因子或肿瘤促进因子,影响癌症的发展进程。
未来lncRNA研究的方向有哪些?
未来lncRNA研究的方向将包括深入理解lncRNA的功能和作用机制、探索lncRNA在不同癌症中的角色、发展新的lncRNA靶向治疗方法。随着编辑技术的发展,特别是CasRx等技术的应用,预计将揭示更多未知的lncRNA功能,为癌症等疾病的治疗提供新的策略。
原文链接
https://www.nature.com/articles/s41592-024-02190-0
Montero JJ, Trozzo R, Sugden M, Öllinger R, Belka A, Zhigalova E, Waetzig P, Engleitner T, Schmidt-Supprian M, Saur D, Rad R. Genome-scale pan-cancer interrogation of lncRNA dependencies using CasRx. Nat Methods. 2024 Feb 26. doi: 10.1038/s41592-024-02190-0. Epub ahead of print. PMID: 38409225.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#lncRNA# #CRISPR-CasRx#
13