Virologica Sinica:国家疾控中心领衔,基于mNGS和扩增子测序的猴痘病毒临床样本全基因组快速鉴定和变异追踪
2023-12-26 测序中国 测序中国 发表于上海
研究显示,采用华大智造研发的DNBSEQ-G99进行扩增子测序的覆盖率达99.66%,能够对临床样本进行快速测序,从而促进获得高质量的MPXV基因组序列。
导读
猴痘病毒(MPXV)是一种长度为197kb的双链DNA病毒,由大约200个基因组成,可在人类和野生动物中引起疾病。近年来,人类猴痘病例逐渐增多,已成为全球关注的焦点。
核酸扩增和血清学检测能以低成本快速诊断猴痘病例,但这些检测不能用于监测MPXV的来源、谱系、传播和基因组变异。新出现的变异可能会使得样本中的病毒载量被低估,甚至导致误诊。为了更好地开展MPXV感染的预防和治疗,有必要制定具有成本效益和高质量的MPXV全基因组测序策略。
近日,来自中国疾病预防控制中心病毒病预防控制所、重庆市疾病预防控制中心、华大智造等单位的研究团队在Virologica Sinica期刊发表了题为“Rapid identification of full-length genome and tracing variations of monkeypox virus in clinical specimens based on mNGS and amplicon sequencing”的文章。研究团队利用多种测序平台对获取的猴痘病例样本开展了mNGS和扩增子测序及对比分析,并对这些平台的周转时间和所需成本进行了估算。研究显示,采用华大智造研发的DNBSEQ-G99进行扩增子测序的覆盖率达99.66%,能够对临床样本进行快速测序,从而促进获得高质量的MPXV基因组序列。
值得注意的是,该研究采用了DNBSEQ-G99测序平台具备的多时点数据输出模式(Bioanalysis by Sequencing, BBS),可在2小时内完成初始数据处理并给出分析报告,在12小时内获得完整病毒基因组,大大缩短了MPXV测序所需的时间,具有成本效益和高效率。BBS技术由中国疾病预防控制中心与华大智造联合研发,并于2021年公布。

文章发表在Virologica Sinica
主要研究内容
多种策略结合获取MPXV基因组信息
MPXV基因组测序的主要策略是宏基因组测序(mNGS)和扩增子测序。研究结果表明,扩增子测序以其成本效益和效率而闻名,能够对临床样本进行快速测序,从而促进获得高质量的MPXV基因组序列。同时,纳米孔测序技术增强了末端串联重复序列区域的组装,将扩增子测序与纳米孔测序整合可实现快速获取高质量的猴痘病毒全长基因组。
因为MPXV只占临床样本总DNA的一小部分(不到1%),为了对MPXV基因组进行测序,必须从临床样本中分离病毒并进行培养,再进行基因组测序;扩增子可用于富集或扩增病毒核酸。NGS和纳米孔测序平台已应用于MPXV基因组测序。NGS测序主要使用光学或其他技术,对同一来源的片段进行测序,精度高,但读取长度短,包括Illumina、华大智造MGI和Ion torrent测序平台。纳米孔测序受碱基组成偏差的影响较小,可以直接对长片段进行测序而无需扩增,如Oxford Nanopore的平台。
在此次分析比较中,研究团队收集了中国大陆首例输入性猴痘病例(MPXV/ChinaCQ-202209)和4例本土猴痘病例的水疱液(BF)、口咽(OS)、鼻咽(NS)和血清(SE)拭子样本,采用多种测序平台对上述样本开展了mNGS(DNBSEQ-G99、DNBSEQ-G400、NextSeq 2000)和扩增子测序(DNBSEQ-G99、GridION、Genexus)。
在扩增子测序中,研究团队使用了华大智造的ATOPlex平台进行PCR引物设计及基因组扩增,并使用MGIEasy Fast PCR-Free FS DNA library Prep Kit制备扩增子测序文库,在DNBSEQ-G99平台上采用SE100+10+10测序策略对文库进行测序。
在mNGS中,完成测序文库制备步骤后,将制备的DNB加载到规则阵列载片上,在华大智造测序平台DNBSEQ-G99(BBS模式,PE100+10+10)和DNBSEQ-G400(PE100+10+10)上进行测序。
数据显示,几乎所有测序都实现了高深度和覆盖率(图1A-B)。除来自输入性猴痘病例OS样本的mNGS(10×覆盖率 = 81.38%)和SE样本的扩增子测序(10×覆盖率 = 17.91%)外,上述测序生成了近乎完美的MPXV基因组组装。
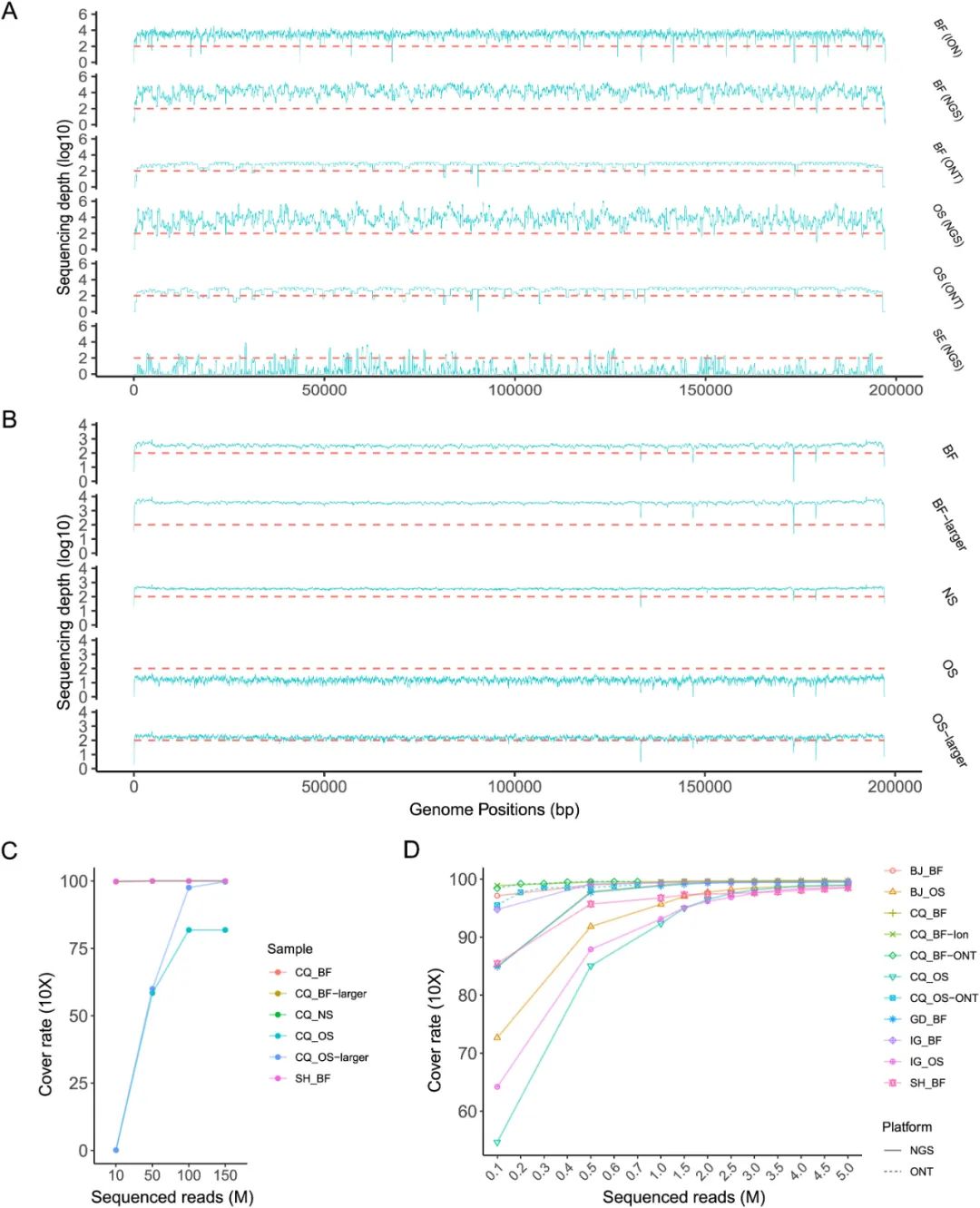
图1. 利用mNGS和扩增子对MPXV进行基因组测序。A:首例输入性猴痘病例扩增子测序深度;B:首例输入性猴痘病例mNGS深度。从所有猴痘病例的mNGS (C)和扩增子(D)数据集中随机取样,MPXV基因组覆盖率为10×。
在扩增子数据集中,口咽拭子样本ONT GridION测序的10×覆盖率最低(98.85%),DNBSEQ-G99的10×覆盖率最高,为99.66%(表1),主要区别在于ONT GridION扩增子的扩增片段稍大(1500~2000 bp vs 200 bp)。在mNGS数据集中,DNBSEQ-G99、DNBSEQ-G400测序水疱液样本的10×覆盖率最高分别为99.93%、99.99%。在NS样本中,这两种测序途径的覆盖率均大于99%。因此,具有较短扩增片段的扩增子可能更适合低病毒载量的样本。在血清扩增子数据集中,MPXV基因组的测序比例非常低,大部分基因组没有被检测到,可能是血清中MPXV基因组的断裂严重导致。因此,在MPXV基因组测序中应避免使用这些样本。
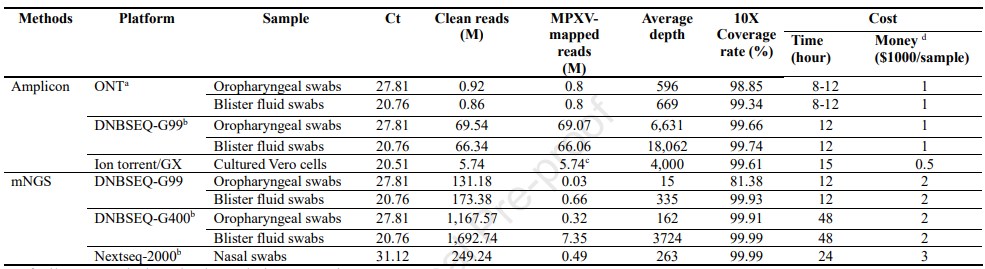
表1. 首例输入性猴痘病例测序数据汇总。
研究显示,增加测序深度可以提高MPXV基因组组装的质量(图1B)。相对于mNGS的10 M reads,扩增子测序最多可以5 M的reads实现全基因组覆盖(图1D)。对于高病毒载量样本来说,这个数量的一半就足够了。即使在病毒载量较低的样本中,ONT GridION扩增子测序也需要不到1 M 的reads。Genexus平台的测序深度在基因组中均匀分布,并且需要的reads较少(图1D)。
在传染病防控中,特别是未知病原体的鉴定,时间至关重要。研究团队估计了上述分析所需的时间和成本(表1)。对比周转时间,在扩增子测序及分析中,ONT GridION耗时为8-12小时,DNBSEQ-G99为12小时,Genexus为15小时;在mNGS中,DNBSEQ-G99为12小时,DNBSEQ-G400为48小时,NextSeq 2000为24小时。
总体分析来看,DNBSEQ-G99的耗时短,覆盖率高,reads数量大,可满足MPXV基因组测序需求。考虑到成本,研究团队认为,mNGS适用于对疱液等高病毒载量样本进行测序,其应用于口咽拭子等低病毒载量样本会导致成本过高。扩增子测序是提高基因组质量同时显著降低费用的一个有效方法。
值得一提的是,在该研究中,研究团队采用DNBSEQ-G99成功地对2022年9月中国内地报道的第一例输入性猴痘病例以及2023年6月初发现的一例病例进行了突变分析,并对病毒基因组进行了溯源分析。2022年9月,刚刚发布的华大智造基因测序仪DNBSEQ-G99,首次应用于传染病防控,助力该次溯源测序得到了高度可信的毒株序列全长。而DNBSEQ-G99具备的BBS模式,缩短了交付时间,进一步加速了病原体鉴定。该技术允许在测序开始后2小时内完成初始数据处理并给出分析报告,并在12小时内完成PE150测序,大大缩短了MPXV测序所需的时间。对于病毒载量较低的口腔拭子样本(Ct=27.81),DNBSEQ-G99也能够在12小时内获得完整的病毒基因组序列,且测序读长不受限,更加适用于公卫系统紧急、多元的检测场景。
鉴定MPXV宿主内突变
分析显示,MPXV基因组突变率较低,且发现了宿主内单核苷酸变异(iSNV),为感染宿主中病毒的遗传多样性和进化选择提供了重要信息。在口咽拭子中未发现杂合突变位点,在水泡液拭子中至少发现了4个杂合突变位点。两个基因位点(C16940T和C54262T)同时被mNGS、扩增子测序发现,频率约为50%,并使用Sanger测序进行了验证(图2A-C)。在口咽拭子和水疱液样本的扩增子测序和mNGS中,DNBSEQ-G99和DNBSEQ-G400检测到的突变点最多。
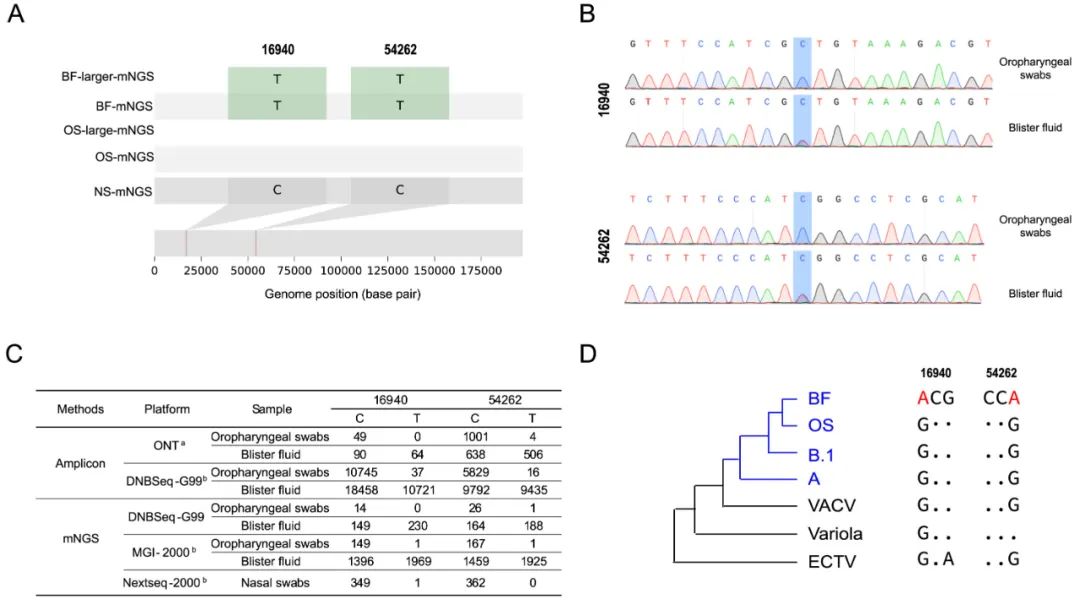
图2. MPXV的iSNV检测。A:两个iSNV在多个临床样本中的碱基差异。B:两个杂合iSNV的Sanger测序验证。C:两个杂合子iSNV的原始read计数。D:密码子的保守性,包括这两个iSNV。
结 语
该研究表明,目前的主流测序平台能够满足MPXV全基因组测序的要求,并准确识别样本中的基因组变异位点。病毒感染样本测序策略的选择应结合样本数量、预期持续时间和成本等因素仔细考虑。对于高病毒载量的样本,如水疱液,mNGS和扩增子测序都可以产生高质量的全长病毒基因组。对于病毒载量较低的样本,如口咽拭子,由于需要大量的测序数据,因此不建议直接进行mNGS,成本较高,扩增子测序可高效地对临床样本进行测序且成本较低,结合纳米孔测序可提升MPXV基因组中末端串联重复区域的组装质量。
研究团队将各种新的测序技术与扩增子富集策略相结合。即使对于低病毒载量的口腔拭子样本,也能使用DNBSEQ-G99在运行后2小时内完成初步分析,在12小时内获得完整的病毒基因组序列,大大缩短了MPXV测序所需的时间,为监测变异和对MPXV等重要病原体发出早期预警提供了重要帮助。
中国疾病预防控制中心病毒病预防控制所吴长城、阿茹罕,重庆市疾病预防控制中心叶盛为文章共同第一作者。北京大学生命科学学院陆剑教授,中国疾病预防控制中心病毒病预防控制所谭文杰研究员为文章的共同通讯作者。
论文原文:
Wu C, A R, Ye S, et.al, Rapid identification of full-length genome and tracing variations of monkeypox virus in clinical specimens based on mNGS and amplicon sequencing. Virol Sin. 2023 Dec 7:S1995-820X(23)00144-X. doi: 10.1016/j.virs.2023.12.002.
https://www.sciencedirect.com/science/article/pii/S1995820X2300144X?via%3Dihub=
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#猴痘病毒# #mNGS# #扩增子测序#
34