弥漫性软脑膜胶质神经元肿瘤
2019-09-15 晋薇 黄玺瑞 王琼 中国现代神经疾病杂志
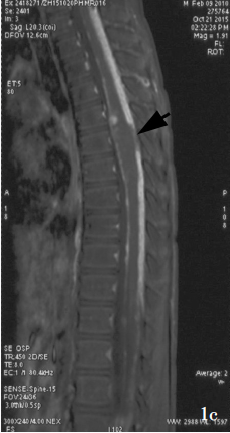
患儿男性,5岁9个月,因脑积水1.50个月,反复抽搐发作2次,于2015年11月25日入院。患儿于1.50个月前无明显诱因突发睡眠中意识障碍和抽搐发作,表现为双眼凝视、牙关紧闭、四肢屈曲抖动,呼之不应,意识障碍,大小便失禁,持续数分钟后自行缓解,意识逐渐恢复,无发热、呕吐、腹泻、头晕、头痛。外院头部CT检查(2015年10月8日)显示,双侧侧脑室、第三脑室明显增宽,考虑重度脑积水。腰椎穿刺脑脊液检

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





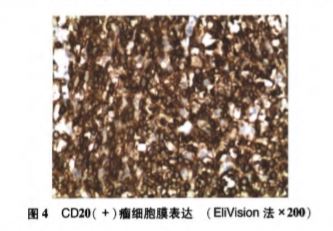





#软脑膜#
38
#弥漫性#
30