JAMA Cardiology:白细胞介素1基因位点和心包炎的变异
2024-01-16 Bob Wang MedSci原创 发表于上海
这项研究发现心包炎与白细胞介素1基因位点的2个独立序列变异之间存在关联。这一发现有可能有助于使用白细胞介素1-阻断药物开发更有针对性的个性化心包炎治疗。
心包炎是一种具有临床挑战性的疾病,其发病机制尚不完全了解。心包炎症可能由各种事件引发,包括病毒感染、心脏损伤和癌症,也可能作为系统性炎症疾病的一部分发生。然而,大多数病例在常规检查后被称为特发性。
尽管急性心包炎通常是良性和自我限制的,但15%至30%的患者会患上复发性心包炎,这是一个治疗挑战,并降低了与健康相关的生活质量和生产力。一部分患者对非甾体抗炎药或秋水仙碱的常规一线治疗没有反应或耐受。因此,尽管疗效不确定,并且有重大不良反应的风险,临床医生可能会求助于二线皮质类固醇治疗。
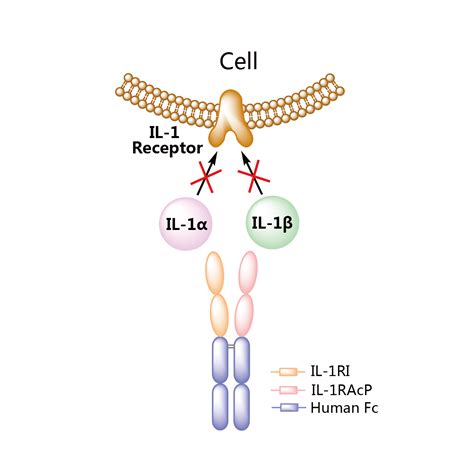
最近,对心包炎炎症的特定机制的了解已经出现,从而产生了新的治疗方案。一项基于人类心包样本和小鼠模型的研究支持了NLRP3炎症体介导的白细胞介素1(IL-1)细胞因子激活的重要性的理论。此外,随机临床试验已经证明了抗IL-1药物anakinra、rilonacept和goflikicept在复发性心包炎中的安全性和有效性。
IL-1抑制剂之前已被证明对治疗由NLRP3变异引起的疾病(例如施尼茨勒综合征)有效。关于心包膜炎遗传学的知识有限,据我们所知,没有全基因组关联研究(GWAS)已经出版。为了阐明心包炎的发病机制,2023年12月27日发表在JAMA Cardiology的文章,进行了GWAS,并使用广泛的表型和多组数据进一步分析了相关的序列变体。

这是对5个国家心包炎全基因组关联研究的荟萃分析。检查了心包炎相关变体与心包炎亚型(包括复发性心包炎)和继发表型之间的联系。为了探索机制,评估了与信使RNA表达(cis-eQTL)、血浆蛋白水平(pQTL)和DNA的CpG甲基化(ASM-QTL)的关系。包括来自冰岛、丹麦、英、美国和芬兰的数据。数据分析时间为2022年9月至2023年8月。
研究结果显示,在这项对4894名心包炎患者(诊断时平均[SD]年龄,51.4[17.9]岁,2734[67.6%]男性,不包括FinnGen队列)的全基因组关联研究中,在2q14号染色体上的白细胞介素1位点确定了2个独立的常见基因间变异。

图1:染色体2q14与心包炎的关联
铅变体是rs12992780(T)(效应等位基因频率[EAF],31%-40%;赔率[OR],0.83;95%CI,0.79-0.87;P = 6.67 × 10−16),IL1B下游和次级变体rs7575402(A或T)(EAF,45%-55%;调整OR,0.89;95%CI,0.85-0.93;调整P = 9.6 × 10−8)。
铅变体rs12992780与急性型(0.86)(异质性P = 0.03)相比,复发性心包炎的几率比较小(0.86),rs7575402与已知调节白细胞介素1生产的4个转录因子的CpG甲基化重叠结合位点有关:PU.1(由SPI1编码)、STAT1、STAT3和CCAAT/增强剂结合蛋白β(由CEBPB编码)。
综上所述,这项关于在IL-1位点识别变异的心包炎的GWAS研究鼓励了进一步研究和开发心包炎的IL-1阻断治疗。正如CpG甲基化关联所示,2种铅变体之一可能会通过影响转录因子与DNA的结合来影响心包炎风险。我们的结果为进一步研究提供了基础,例如潜在的基因型特异性药物反应和介导心包炎特异性关联的机制。
原文出处
Thorolfsdottir RBJonsdottir ABSveinbjornsson G, et al. Variants at the Interleukin 1 Gene Locus and Pericarditis. JAMA Cardiol. Published online December 27, 2023. doi:10.1001/jamacardio.2023.4820
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#心包炎# #白细胞介素1#
25