半年内国产6款Claudin18.2创新药物获批临床,全球在研进入热潮
前不久,石药集团宣布其靶向Claudin18.2的ADC药物SYSA1801获批临床,拟用于治疗晚期实体瘤患者。值得一提的是,在这之前今年已有5款靶向Claudin18.2的抗体药物获批临床,SYSA
柏思荟 - 创新药物 - 2021-06-26
可善挺(司库奇尤单抗)强直性脊柱炎适应症获批
北京4月28日电 (记者 李亚南)诺华制药(中国)28日宣布,可善挺(司库奇尤单抗)获得中国国家药品监督管理局批准,用于常规治疗疗效欠佳的强直性脊柱炎的成年患者。这是可善挺继此前批准用于治疗中重度斑块
中国新闻网 - 强制性脊柱炎,可善挺 - 2020-04-30
强效抑郁症疗法SAINT获批
也可以看到近年来关于抑郁症的发病机制以及治疗药物的研究取得快速发展,望这些治疗方案可以尽快进入临床,切实惠及患者。
生物探索 - 难治性抑郁,强效抑郁症疗法 - 2022-12-15
转移性膀胱癌的首选靶向治疗药物:Balversa(erdafitinib)在美国加速获批
强生公司近日表示,FDA已经加速批准其Balversa(erdafitinib)的营销申请,以治疗携带某些FGFR基因突变的局部晚期或转移性膀胱癌患者。
网络 - Balversa,转移性膀胱癌,Erdafitinib - 2019-04-13
两票制将席卷半个中国,第三批医改试点省份来了!
从第一批医改试点省份江苏、安徽、福建、青海,再到第二批的上海、浙江、湖南、重庆、四川、陕西、宁夏,全国医改试点省份突然增加到了11个。 据医改政策制定的人士透露,今年开始国务院医改办开始
赛柏蓝 - 两票制,医改 - 2016-11-15
辉瑞的Avastin生物仿制药——ZIRABEV在欧洲获批治疗多个转移性肿瘤
欧洲委员会(EC)近日批准辉瑞的ZIRABEV用于治疗转移性结肠或直肠癌、转移性乳腺癌、不可切除的晚期转移性或复发性非小细胞肺癌(NSCLC)、晚期或转移性肾细胞癌以及持续复发的转移性宫颈癌。
MedSci原创 - Avastin,生物仿制药,VEGF - 2019-02-20
肿瘤个性化治疗——肿瘤新抗原Neoantigen疗法首次获批进入临床试验
Achilles Therapeutics现已成为临床阶段的生物技术公司,获得监管部门的批准,开始其肺癌治疗的1/2期临床试验。该公司正在开发针对肿瘤"新抗原"的个性化T细胞疗法。
MedSci原创 - 个性化治疗,肿瘤新抗原,T细胞 - 2019-01-26
YESCARTA在日本获批用于治疗复发难治大B细胞淋巴瘤(DLBCL)
日本厚生劳动省(MHLW)已批准嵌合抗原受体(CAR)T细胞疗法YESCARTA®(axicabtagene ciloleucel)用于治疗患有复发难治大B细胞淋巴瘤(DLBCL)的成年患者。
MedSci原创 - CAR-T,Yescarta,日本厚生劳动省(MHLW),复发难治大B细胞淋巴瘤 - 2021-01-24
OPD重磅炸弹——勃林格新药Spiriva Respimat获批,将取代市场No.1药物
导读:勃林格殷格翰是呼吸疾病领域的领导者,该公司开发的COPD新药Spiriva Respimat于2007年被FDA拒绝。之后开展了全球最大的COPD临床研究,证明了疗效和安全性。近日,FDA终于批准Spiriva Respimat,该药与COPD市场中处方量排名第一的药物Spiriva HandiHaler具有相同的成分,但前者的气雾配方具有舒适性及便利性优势,尤其将使初诊COPD患者群体受益
生物谷 - 新药,勃林格 - 2014-09-28
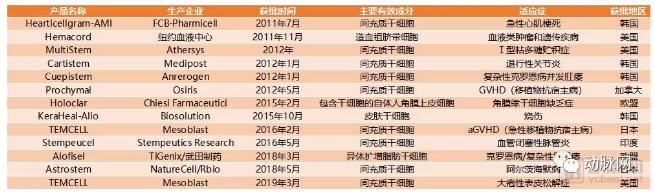
超10款产品获批,商业化待定,干细胞治疗是挣钱利器还是救世英雄?
近年来,国家在生物医药产业发布的一系列政策中,总少不了干细胞的内容。这个产业有种达摩克利斯之剑的味道,从字面看起来就有着强大的力量,但深究后却发现,处处都是与机遇并存的风险。
动脉网 - 干细胞治疗,生物医药产业,间充质干细胞,诱导多能干细胞 - 2019-11-22
国家药监局:2018年第二批医疗器械临床试验监督抽查情况
5月6日,国家药监局发布《关于2018年第二批医疗器械临床试验监督抽查情况的公告(2019年第38号)》。
国家药监局 - 医疗器械,临床试验 - 2019-05-06
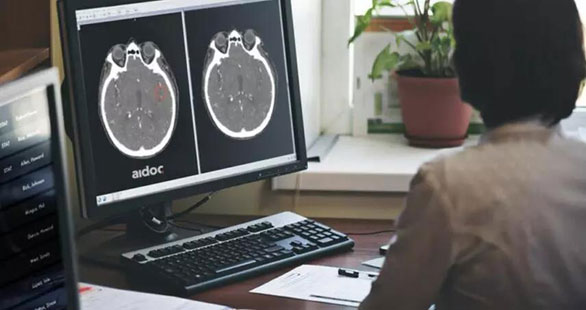
国内外医学影像AI产品接连获批,能填补放射科医生缺口吗?
CT、MRI等医学影像检查正发挥着越来越重要的作用。有超过75%的患者在诊疗过程中需放射科医生的帮助。但专业影像人才的培养速度远远赶不上需求增速,放射科医生面临着巨大缺口。
汉鼎好医友 - 医学影像 - 2020-03-12
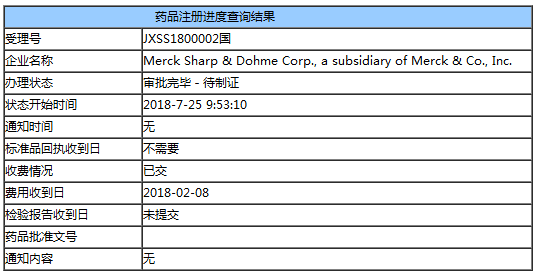
默沙东Keytruda获批,第2个PD-1药物正式登陆中国
2018年7月25日,默沙东PD-1单抗Keytruda(帕博利珠单抗)的中国上市申请(JXSS1800002)正式获得国家药品监督管理局批准,成为继百时美施贵宝Opdivo之后第2个正式在中国上市的PD-1/PD-L1单抗类药物(见:重磅!Opdivo在中国正式获批上市!定价猜想……)。Keytruda的中国上市时间比Opdivo晚了1个多月,但二者适应症不同。Opdivo用于二线治疗非小细胞肺
医药魔方Plus - Keytruda,默沙东 - 2018-07-26
曲妥珠单抗皮下制剂在华获批,给药仅2-5分钟!
与传统静脉输注给药30-90分钟相比,曲妥珠单抗注射液(皮下注射)可在2-5分钟内完成给药。
罗氏制药 - 乳腺癌,曲妥珠单抗皮下制剂 - 2022-10-10
为您找到相关结果约500个