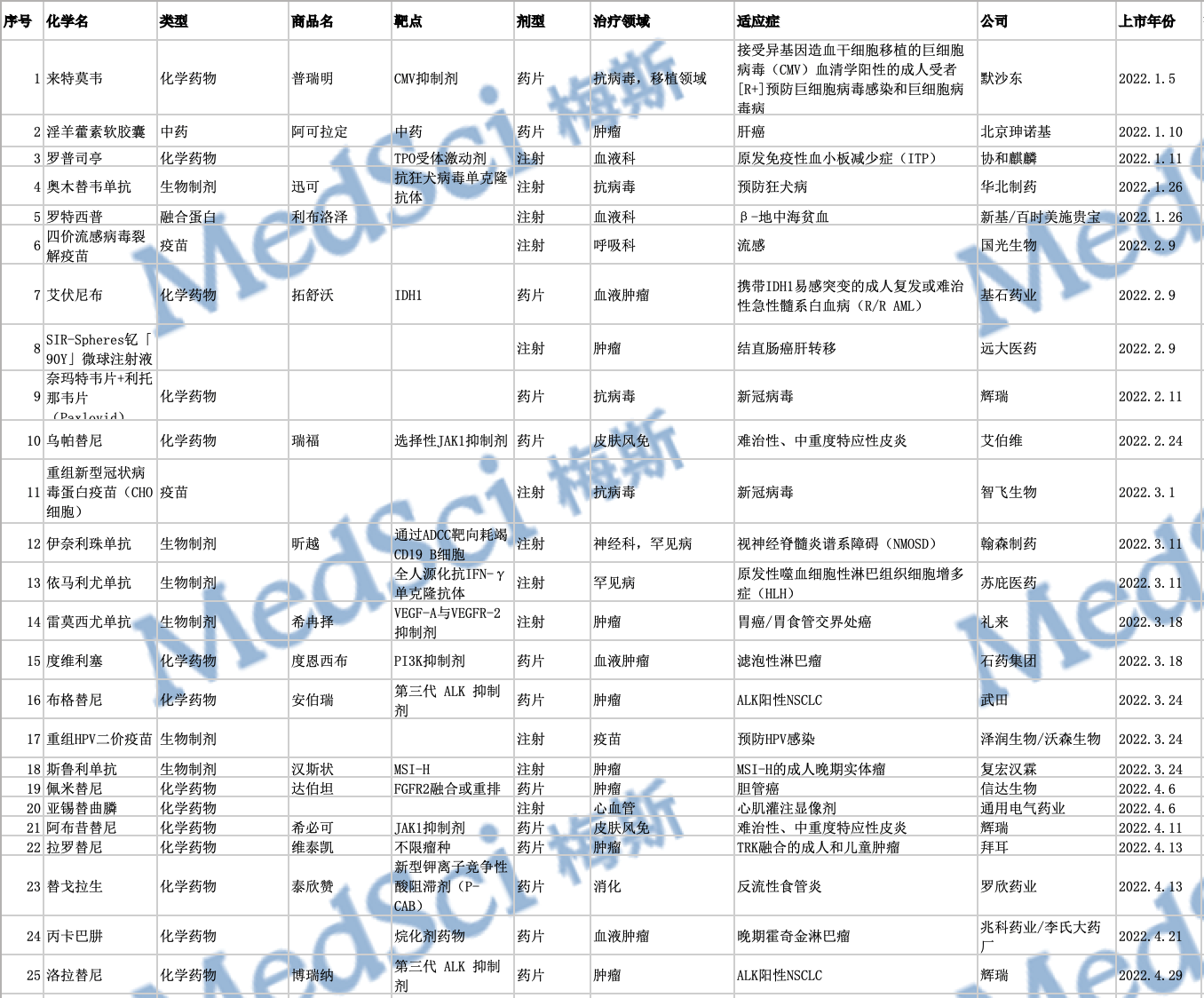
2022年中国NMPA批准上市的50款创新药物
2022年,中国药监局(NMPA)共批准了50款新药,其中进口新药有30款,国产新药有20款。从药物类型上看,包括28款化学药、13款生物药、5款疫苗以及4款中药。数量与2019年批准了51款新药,2
MedSci原创 - 创新药物,NMPA - 2023-01-13
国家食品药品监督管理总局批准布瑞亭在中国上市
国家食品药品监督管理总局(CFDA)4月26日正式批准默沙东麻醉领域的创新药物布瑞亭(舒更葡糖钠注射液)在中国上市。布瑞亭是全球首个、也是目前唯一批准上市的特异性结合性神经肌肉阻滞拮抗剂。
科学网 - 药品,上市 - 2017-04-28
中国NMPA批准ZEJULA(Niraparib)用于复发性卵巢癌患者的维持治疗
Zai Lab生物制药公司近日宣布,中国国家药品监督管理局(NMPA)批准了ZEJULA(Niraparib)的新药申请(NDA)用于对铂类化学疗法有完全或部分反应的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌患者的维持治疗
MedSci原创 - Niraparib,Zejula,NMPA - 2019-12-28
罗氏的Tecentriq在中国获得首个批准,用于治疗广泛期小细胞肺癌
罗氏制药公司近日宣布,经中国国家药品监督管理局(NMPA)批准,Tecentriq(atezolizumab)与化疗联合可用于广泛期小细胞肺癌(SCLC)患者的一线治疗,Tecentriq(atezolizumab
MedSci原创 - 广泛期小细胞肺癌,Tecentriq,NMPA - 2020-02-15
墨西哥宣布批准紧急使用两款中国新冠疫苗,中国新冠疫苗惠及全球数十个国家和地区
墨西哥外交部副部长玛尔塔·德尔加多·佩拉尔塔10日表示,墨西哥政府下属联邦预防卫生风险委员会已批准紧急使用两款中国研发的新冠疫苗。
网络 - 新冠疫苗 - 2021-02-11
中国批准首个国产阿尔茨海默症早诊示踪剂进入III期临床
18F-APN-1607是国内首个申报临床的tau蛋白示踪剂产品,也是新旭医药首个在国内进入临床试验III期的一类新药药物。目前tau蛋白已被医学界认可为AD的重要生物靶点。
亿欧 - 中国,临床,阿尔茨海默症 - 2020-11-05
骨质疏松症新药Evenity(romosozumab)获多国批准上市,中国临床试验也已开展
2019年1月,安进(Amgen)和优时比(UCB)宣布,其联合开发的用于治疗高骨折风险的骨质疏松症新药Evenity(romosozumab),已获得日本厚生劳动省颁发的上市许可,用于降低骨折高危男
MedSci - 骨质疏松症,Romosozumab - 2020-06-05
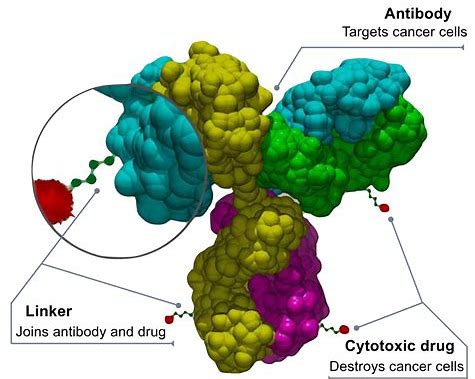
中国首款靶向CD30的抗体药物偶联物ADCETRIS(brentuximab vedotin)获得批准
武田中国今日宣布,靶向CD30的ADCETRIS(brentuximab vedotin)已获得中国国家药品监督管理局(NMPA)的正式批准。
MedSci原创 - 霍奇金淋巴瘤,淋巴瘤,CD30阳性 - 2020-05-16
JAMA:FDA加速批准药物的预批准研究和批准后研究有无差别?
2017年8月,发表在《JAMA》的一项研究调查了美国食品药物管理局(FDA)加速批准授权药物预批准和批准后研究的特点。研究结果显示,验证性试验和预批准试验具有相似的设计元素,加速批准授权药物的有效性通常在批准后3年内的批准后研究中得到证实。
环球医学 - 药物,FDA - 2017-09-18
阿斯利康第三代靶向肺癌药物Tagrisso获中国CFDA批准
英国制药巨头阿斯利康(AstraZeneca)近日宣布,中国食品和药品监督管理总局(CFDA)已批准抗癌药Tagrisso(omisertinib,AZD9291)40mg和80mg片剂,作为一种每日口服一次的药物
生物谷 - 阿斯利康,非小细胞肺癌,Tagrisso,EGFR-TKI,omisertinib,T790M,耐药突变 - 2017-03-30
中国监管机构批准阿斯利康的Tagrisso作为EGFR突变型NSCLC的一线治疗药物
阿斯利康近日表示,中国国家医疗产品管理局(NMPA)已经批准其Tagrisso(osimertinib),用于一线治疗局部晚期或转移性非小细胞肺癌(NSCLC)的成人患者,这些患者的肿瘤细胞具有EGFR
MedSci原创 - Tagrisso,EGFR,NMPA,一线治疗药物 - 2019-09-04
顶级学术期刊连发两文,需谨慎对待中国批准的治疗阿尔茨海默新药
一家中国生物技术初创公司以一种新型的植物性化合物改变肠道微生物来改善阿尔茨海默氏症患者的认知功能,这令神经科学家和药物开发人员大吃一惊。
生物世界 - 阿尔茨海默新药,争议 - 2019-11-07
首个超长效基础胰岛素类似物诺和达(R) 在中国获得上市批准
国家食品药品监督管理总局(CFDA)今天确认,正式批准由丹麦诺和诺德制药公司研发生产的超长效胰岛素类似物诺和达® (德谷胰岛素注射液)于9月20日在中国上市。该药物用于治疗成人2型糖尿病,是中国获批的首个超长效基础胰岛素类似物。
诺和诺德 - 美通社,胰岛素,诺和达 - 2017-10-10
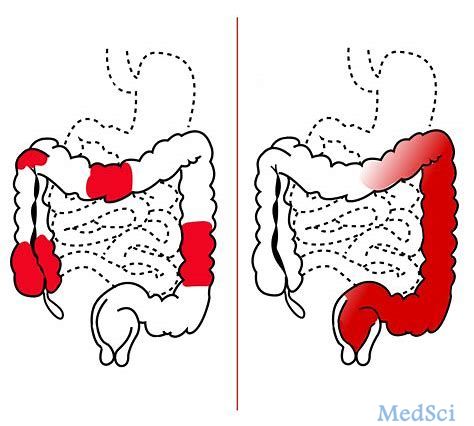
中国NMPA:批准Pellino-1抑制剂BBT-401治疗溃疡性结肠炎的IND
韩国制药公司Bridge近日宣布,中国国家药品监督管理局(NMPA)药品评审中心(CDE)批准了于2019年9月25日提交的IND,旨在寻求Pellino-1抑制剂BBT-401治疗溃疡性结肠炎(UC)
MedSci原创 - Pellino-1抑制剂,BBT-401,溃疡性结肠炎 - 2019-12-28
为您找到相关结果约500个