英国授权辉瑞/ BioNTech研发的新冠疫苗全面使用
英国周三批准了辉瑞-BioNTech联合研发的新冠疫苗用于紧急用途,并将在下周在英国推出,老年人与医务人员将排在优先接种。
MedSci原创 - 疫苗,辉瑞,BioNTech - 2020-12-02
EMA建议对辉瑞的Paxlovid进行有条件授权
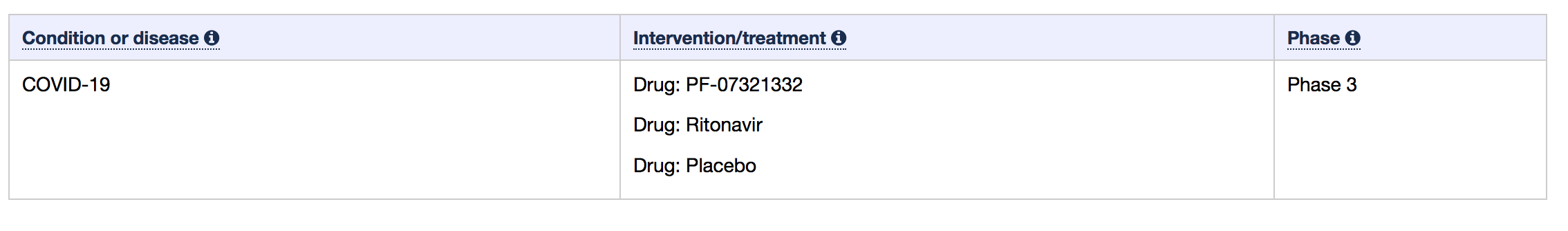
辉瑞上个月报告的试验结果显示,与安慰剂相比,Paxlovid 在症状出现后三天内服用可将住院或死亡风险降低 89%,在五天内服用可降低 88%。
MedSci原创 - Covid-19,Paxlovid - 2022-02-03
辉瑞的Bosulif在美国作为一线药物使用
辉瑞公司的Bosulif已经获准在美国治疗新诊断的Ph +慢性骨髓性白血病患者。这个决定是由英国Avillion公司根据与药物巨头达成的合作开发协议资助并进行的III期临床试验的数据得出的。BFORE研究(Bosutinib在一线慢性粒细胞性白血病治疗试验中)显示,Bosulif(bosutinib)400mg的患者在12个月(47.2%)的患者中,与使用伊马替尼imatinib 400mg
MedSci原创 - Bosulif - 2017-12-21
辉瑞/Astellas的Xtandi降低前列腺癌的扩散风险
试验结果显示,与单独使用激素疗法相比,将辉瑞和Astellas制药公司的Xtandi用于激素治疗显着降低了前列腺癌扩散的风险。根据III期PROSPER试验的结果,与非ADT单药治疗的非转移性去势前列腺癌(CRPC)患者相比,Xtandi(enzalutamide)加雄激素剥夺疗法(ADT)将发生转移或死亡的风险降低了71%。主要终点无转移生存期(MFS)的中位数为36.6个月,而接受Xt
MedSci原创 - 辉瑞/Astellas的Xtandi - 2018-02-06
辉瑞将向英国提供充足的COVID-19疗法Paxlovid
辉瑞的口服抗病毒候选药物 Paxlovid 是一种研究性 SARS-CoV-2 蛋白酶抑制剂,可在 COVID-19 感染的初期治疗 COVID-19。
MedSci原创 - Paxlovid - 2021-12-25
辉瑞计划继续推进Remoxy临床开发
辉瑞(Pfizer)10月22日宣布,已实现与止痛药Remoxy(oxycodone,羟考酮)缓释胶囊生产相关的技术里程碑,该公司将继续推进Remoxy的开发项目。今年早些时候,辉瑞收到FDA的指导意见,该公司计划开展额外的临床研究及所要求的其他行动,以解决2011年6月收到的完整回应函(CRL)。这些新的临床研究包括:一项关键的生物等效性研究,以弥补修改配方后的Remoxy与原配方的生物
生物谷 - 新药,FDA - 2013-10-24
EMA接受辉瑞新药BZA/CE上市许可申请的审查
欧洲药品管理局(EMA)表示,已接受对辉瑞(Pfizer)药物BZA/CE(bazedoxifene/conjugated estrogens,bazedoxifene/共轭雌激素)上市许可申请的审查。BZA/CE是一种潜在的新药物,用于绝经后女性雌激素缺乏症及具骨折风险的女性骨质疏松症的治疗。辉瑞预计在2013年得到EMA的
生物谷 - 新药,FDA - 2012-07-24
Teva停产重要儿童化疗药 辉瑞“救场”
今年下半年全球仿制药巨头梯瓦制药决定停止生产用于治疗严重癌症的儿童化疗药品后,辉瑞似乎要挺身而出“救场”。据FiercePharma报道,辉瑞目前正在提高长春新碱的生产量,试图弥补这一严重短缺。
新浪医药新闻 - 梯瓦制药,辉瑞,长春新碱 - 2019-10-16
辉瑞与Allogene合作开发癌症疗法
辉瑞公司和Allogene公司已达成协议,开发异体CAR T细胞疗法。财务细节没有披露,但据透露,这笔交易让辉瑞获得Allogene 25%的股权,而Allogene将从辉瑞获得16项临床前CAR T资产。辉瑞表示,它认为该协议"是一个有吸引力的机会,以高度专注和熟练的方式支持异基因CAR T疗法的持续开发。""异基因CAR T平台代表了一种潜在的治疗癌症的转化方法,我们对未来在这一领域的研究感到
MedSci原创 - 辉瑞与Allogene,CAR,T细胞疗法 - 2018-04-04
Takeda的Alunbrig在ALK阳性NSCLC的PFS击败了辉瑞公司的Xalkori
武田的Alunbrig在一项III期试验中击败了辉瑞公司的Xalkori无进展生存期(PFS),该试验测试了其作为ALK阳性肺癌一线治疗的功效。ALTA-1L试验纳入了275例ALK阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者,这些患者之前未接受过ALK抑制剂治疗。
MedSci原创 - Alunbrig,Xalkori - 2018-07-26
辉瑞在欧盟和美国提交肺癌药物dacomitinib 的申请
辉瑞公司已在大西洋两岸提交了其泛表皮生长因子受体(EGFR)酪氨酸激酶抑制剂dacomitinib用于特定形式的肺癌。该公司正在寻求该药物的批准,作为EGFR激活突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者的一线治疗。这些提交资料是基于第三阶段ARCHER 1050研究的数据,这是一项全球性的头对头试验,显示dacomitinib可能会提供比吉非替尼更有价值的临床意义。研究中接受dacom
MedSci原创 - 辉瑞,Dacomitinib - 2018-04-05
辉瑞中止旗下淋巴瘤药物Inotuzumab的后期临床研究
辉瑞虽然最近有三款癌症药物连续获得批准,但它也遇到了挫折,公司于5月20日声称正在停止一款用于治疗侵袭性非霍奇金淋巴瘤药物的一项后期临床试验,因为独立监督员发现这款药物可能无法改善患者的生存期。辉瑞表示将继续在其它血液癌症方面对这款名为Inotuzumab ozogamicin的试验药物进行研究。辉瑞肿瘤学业务单元负责临床开发和医疗事务的高级副总裁Mace Rothenberg在一项声明中说:
dxy - 淋巴瘤,辉瑞,药物,吉西他滨,Inotuzumab,临床研究 - 2013-05-28
FDA:欧洲批准辉瑞肺炎链球菌疫苗的扩展应用
辉瑞表示,旗下肺炎链球菌疫苗Prevenar 13的扩展应用获得欧洲卫生监管部门的批准,从而使该疫苗的适用人群更加宽广,可用于18至49岁的成年人。这款疫苗之前在欧洲被批准用于婴儿、幼儿和年龄在6星期至17岁的青少年及50或50岁以上成年人。Prevenar用于预防肺炎链球菌的13个菌株,肺炎链球菌能引起肺炎、耳朵感染,甚至致命的疾病,如肺炎球菌脑膜炎。这款疫苗在120多个国家被批准
丁香园 - 疫苗,肺炎链球菌,辉瑞,Prevenar,FDA - 2013-07-24
为您找到相关结果约500个