英国授权辉瑞/ BioNTech研发的新冠疫苗全面使用
英国周三批准了辉瑞-BioNTech联合研发的新冠疫苗用于紧急用途,并将在下周在英国推出,老年人与医务人员将排在优先接种。
MedSci原创 - 疫苗,辉瑞,BioNTech - 2020-12-02
EMA建议对辉瑞的Paxlovid进行有条件授权
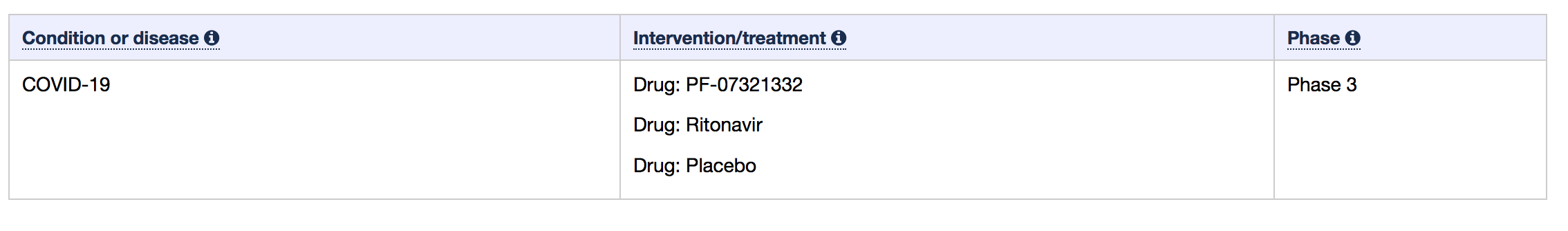
辉瑞上个月报告的试验结果显示,与安慰剂相比,Paxlovid 在症状出现后三天内服用可将住院或死亡风险降低 89%,在五天内服用可降低 88%。
MedSci原创 - Covid-19,Paxlovid - 2022-02-03
辉瑞的Bosulif在美国作为一线药物使用
辉瑞公司的Bosulif已经获准在美国治疗新诊断的Ph +慢性骨髓性白血病患者。这个决定是由英国Avillion公司根据与药物巨头达成的合作开发协议资助并进行的III期临床试验的数据得出的。BFORE研究(Bosutinib在一线慢性粒细胞性白血病治疗试验中)显示,Bosulif(bosutinib)400mg的患者在12个月(47.2%)的患者中,与使用伊马替尼imatinib 400mg
MedSci原创 - Bosulif - 2017-12-21
辉瑞将向英国提供充足的COVID-19疗法Paxlovid
辉瑞的口服抗病毒候选药物 Paxlovid 是一种研究性 SARS-CoV-2 蛋白酶抑制剂,可在 COVID-19 感染的初期治疗 COVID-19。
MedSci原创 - Paxlovid - 2021-12-25
FDA批准辉瑞的Xeljanz治疗溃疡性结肠炎
FDA已批准辉瑞公司的Xeljanz(tofacitinib)用于治疗中度至重度活动性溃疡性结肠炎。这是美国批准的第一种也是唯一的口服Janus激酶(JAK)抑制剂。"对一个溃疡性结肠炎病人有效的治疗方法可能对另一个病人无效,一些人还在与持续的症状作斗争。"这就是为什么我们的患者为他们提供不同治疗方案至关重要,"克罗恩结肠炎基金会总裁兼首席执行官Michael Osso说。该批准基于来自OCTA
MedSci原创 - Xeljanz,溃疡性结肠炎 - 2018-05-31
EMA接受辉瑞新药BZA/CE上市许可申请的审查
欧洲药品管理局(EMA)表示,已接受对辉瑞(Pfizer)药物BZA/CE(bazedoxifene/conjugated estrogens,bazedoxifene/共轭雌激素)上市许可申请的审查。BZA/CE是一种潜在的新药物,用于绝经后女性雌激素缺乏症及具骨折风险的女性骨质疏松症的治疗。辉瑞预计在2013年得到EMA的
生物谷 - 新药,FDA - 2012-07-24
Takeda的Alunbrig在ALK阳性NSCLC的PFS击败了辉瑞公司的Xalkori
武田的Alunbrig在一项III期试验中击败了辉瑞公司的Xalkori无进展生存期(PFS),该试验测试了其作为ALK阳性肺癌一线治疗的功效。ALTA-1L试验纳入了275例ALK阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者,这些患者之前未接受过ALK抑制剂治疗。
MedSci原创 - Alunbrig,Xalkori - 2018-07-26
葛兰素史克不再争夺辉瑞的消费者业务
葛兰素史克(GSK)透露,它将不会竞购辉瑞的消费者医疗保健业务,而在其竞争对手Benckiser退出潜在交易的几天后,该公司也退出了该业务。在一份简短的声明中,该公司首席执行官艾玛o沃姆斯利(Emma Walmsley)表示:"尽管我们将继续审查可能加快我们战略的机会,但它们必须符合我们的回报标准,而不会损害我们的资本配置优先次序。"
MedSci原创 - 葛兰素史克 - 2018-03-23
Duchenne肌营养不良症:辉瑞基因疗法的早期数据
辉瑞公司近日公布了PF-06939926的初始Ib期研究数据,结果显示实验性基因疗法导致男性Duchenne肌营养不良症(DMD)中微小肌营养不良蛋白表达增加。
MedSci原创 - Duchenne肌营养不良症,基因疗法,儿科,PF-06939926 - 2019-06-29
辉瑞在欧盟和美国提交肺癌药物dacomitinib 的申请
辉瑞公司已在大西洋两岸提交了其泛表皮生长因子受体(EGFR)酪氨酸激酶抑制剂dacomitinib用于特定形式的肺癌。该公司正在寻求该药物的批准,作为EGFR激活突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者的一线治疗。这些提交资料是基于第三阶段ARCHER 1050研究的数据,这是一项全球性的头对头试验,显示dacomitinib可能会提供比吉非替尼更有价值的临床意义。研究中接受dacom
MedSci原创 - 辉瑞,Dacomitinib - 2018-04-05
辉瑞中止旗下淋巴瘤药物Inotuzumab的后期临床研究
辉瑞虽然最近有三款癌症药物连续获得批准,但它也遇到了挫折,公司于5月20日声称正在停止一款用于治疗侵袭性非霍奇金淋巴瘤药物的一项后期临床试验,因为独立监督员发现这款药物可能无法改善患者的生存期。辉瑞表示将继续在其它血液癌症方面对这款名为Inotuzumab ozogamicin的试验药物进行研究。辉瑞肿瘤学业务单元负责临床开发和医疗事务的高级副总裁Mace Rothenberg在一项声明中说:
dxy - 淋巴瘤,辉瑞,药物,吉西他滨,Inotuzumab,临床研究 - 2013-05-28
FDA:欧洲批准辉瑞肺炎链球菌疫苗的扩展应用
辉瑞表示,旗下肺炎链球菌疫苗Prevenar 13的扩展应用获得欧洲卫生监管部门的批准,从而使该疫苗的适用人群更加宽广,可用于18至49岁的成年人。这款疫苗之前在欧洲被批准用于婴儿、幼儿和年龄在6星期至17岁的青少年及50或50岁以上成年人。Prevenar用于预防肺炎链球菌的13个菌株,肺炎链球菌能引起肺炎、耳朵感染,甚至致命的疾病,如肺炎球菌脑膜炎。这款疫苗在120多个国家被批准
丁香园 - 疫苗,肺炎链球菌,辉瑞,Prevenar,FDA - 2013-07-24
辉瑞放弃对阿尔茨海默病药物Bapineuzumab的研究
在得知又一项试验得出阴性结果之后,辉瑞公司决定停止对bapineuzumab的研究。 Bapineuzumab是一种旨在靶向作用于阿尔茨海默病患者脑部乙型淀粉样蛋白斑块的单克隆抗体药物。7月份辉瑞公司曾报告,一项对1,300例携带apo E4的阿尔茨海默病患者的Ⅲ期研究显示,bapineuzumab的药物效应为阴性。
网络 - 辉瑞,阿尔茨海默病,bapineuzumab - 2012-08-09
为您找到相关结果约500个