NAT REV DRUG DISCOV:肝癌的治疗现状与未来
免疫疗法将在5年内有望成为治疗肝癌的第一大疗法,给全世界的肝癌患者带来新的治疗方案。
药明康德 - 肝癌,治疗,现状与未来 - 2018-11-01
妇科恶性肿瘤免疫治疗中国专家共识(2023年版)
免疫治疗作为第四大抗肿瘤治疗方法,已在癌症治疗领域取得了突破性进展,其中免疫检查点抑制剂已广泛应用于多种恶性肿瘤的治疗,在妇科恶性肿瘤领域也积累了较多的临床证据和经验。
中国癌症杂志 - 妇科恶性肿瘤 - 2023-11-01
2024 CSCO小细胞肺癌指南重磅更新!化疗骨髓保护创新药曲拉西利获I级推荐、1A类证据
该指南参考了国际国内最新研究进展与临床证据,对我国小细胞肺癌临床药物和治疗方案的选择进行了更新推荐。
网络 - 2024-04-30
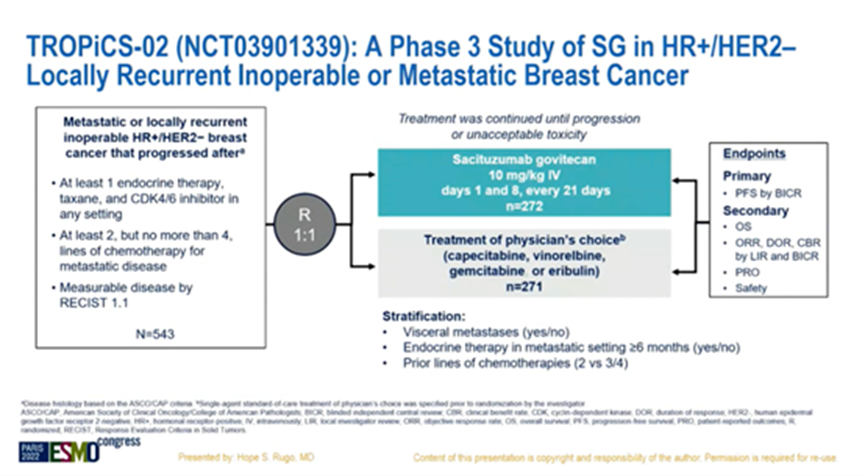
Trop2 ADC药物戈沙妥珠单抗治疗肺癌III期临床获成功(TROPiCS-02研究)
TROPiCS-02研究是一项全球、多中心、开放标签的III期研究,543例患者按1:1的比例随机分组,接受SG(第1、8天静脉注射,10mg/kg,周期为21天)或医生选择治疗(TPC,艾立布林、卡
找药宝典 - TROP2,戈沙妥珠单抗 - 2023-07-08
梁军教授:肝癌系统治疗的今昔与未来
近年来在与“癌王”博弈中,新型靶向治疗和免疫治疗的崛起改变了肝癌系统治疗的格局,为中国肝癌大国的摘帽增加了新希望。
ioncology - 肝癌系统治疗,今昔,未来 - 2019-09-18
FDA批准Hemlibra用于减少或防止某些A型血友病的出血频率
美国FDA批准了Hemlibra (emicizumab - kxwh)用于防止或减少成人和儿童A型血友病患者出血的频率,这些患者体内有一种叫做因子VIII(FVIII)抑制剂的抗体。"降低出血频率或防止出血事件是血友病患者疾病管理的重要组成部分。这一批准提供了一种新的预防治疗方法,它已经被证明可以显着减少因子VIII抑制剂的A型血友病患者出血的次数。" FDA药物评估和研究中心血液和肿瘤产品办公
MedSci原创 - Hemlibra,A型血友病患者 - 2017-11-19
跨国医疗企业点赞中国速度,将携创新产品参展第二届进博会
“在中国,创新药品的上市速度正在加快,今年5月我们研发的靶向药多泽润在中国获批,实现了中国与欧美几乎同时获批。去年,我们研发的3款药物经过国家谈判也纳入了医保目录,降价幅度很大,为中国的肿瘤患者带来了很大福利。”辉瑞生物制药集团中国区总经理吴琨说。9月10日,包含辉瑞、罗氏、强生、默沙东、医科达等在内的5家跨国医疗企业出席第二届中国国际进口博览会(以下简称进博会)医疗展区抗癌专题会,纷纷点赞中
澎湃新闻 - 医疗企业,创新产品,中国速度 - 2019-09-10
创新靶向药RET抑制剂Pralsetinib扩展适应症获美国FDA批准,用于治疗甲状腺癌
近日,美国食品药品监督管理局(FDA)加速批准了创新靶向药RET抑制剂普拉替尼(pralsetinib)的扩展适应症,用于治疗携带RET变异的甲状腺癌患者。这是肿瘤精准治疗领域的又一重要里程碑。
医谷网 - FDA,美国,基因突变 - 2020-12-03
Miracor Medical 宣布 PiCSO® 获得 FDA 试验用器械豁免许可
该研究的主要疗效终点为第 5 天时通过心脏磁共振成像 (CMR) 测量的梗死面积
网络 - FDA 试验用器械豁免 (IDE) 许可,前壁 ST 段抬高型心肌梗死 (STEMI) 患者,间歇性冠状窦闭塞,冠脉微血管阻塞 - 2022-08-23
新一代强效ROS1抑制剂泰莱替尼(AB-106)获优先审评资格!cORR高达92.5%
该试验旨在评估泰莱替尼在中国ROS1阳性非小细胞癌患者中的的安全性、耐受性和疗效。
全球好药资讯 - ROS1,ROS1阳性肺癌,信达生物,泰莱替尼,葆元医药 - 2023-12-23
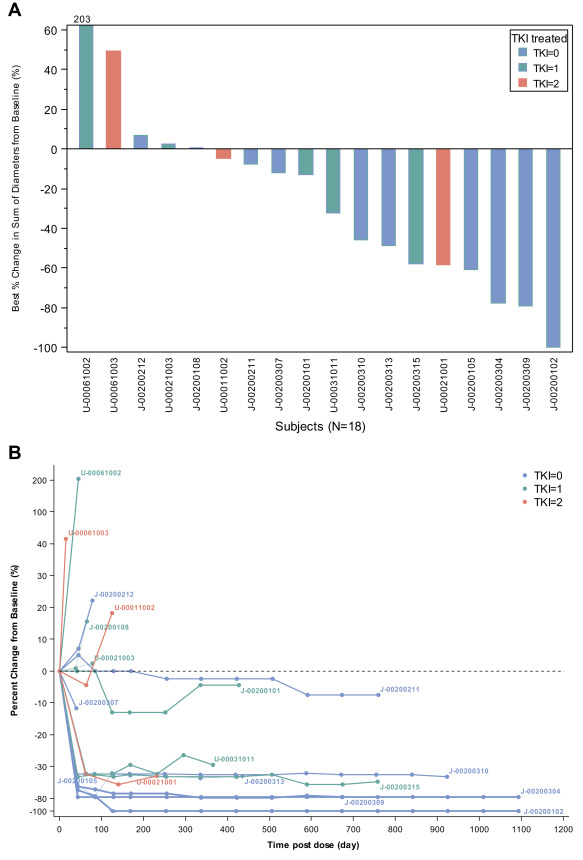
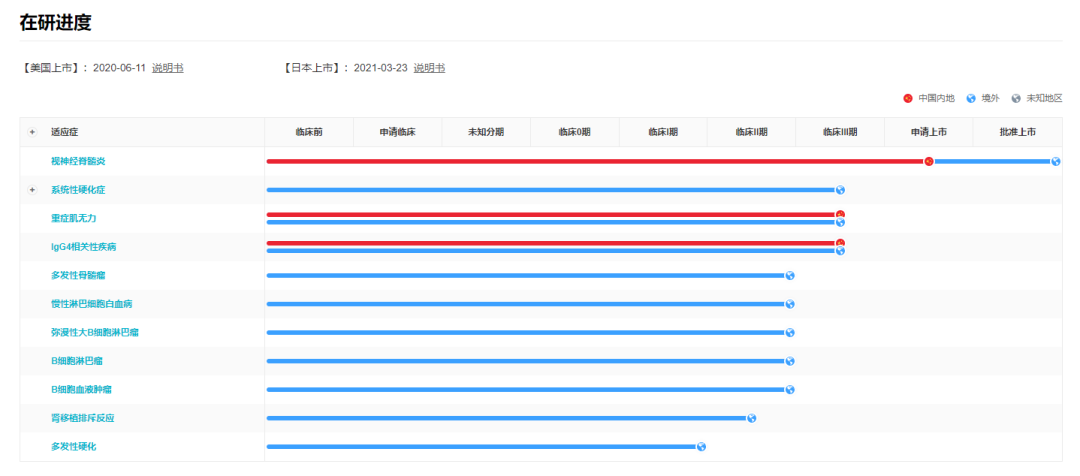
NMPA批准Uplizna(伊奈利珠单抗)治疗视神经脊髓炎谱系疾病(NMOSD)
2022年03月11日,中国国家药监局(NMPA)官网最新公示, 抗CD19单克隆抗体伊奈利珠单抗(inebilizumab)获批上市用于治疗视神经脊髓炎谱系疾病(NMOSD)患者。
网络 - 视神经脊髓炎谱系疾病 - 2022-03-14
全力推进基因疗法,FDA发布6大新指南
近日,美国FDA局长Scott Gottlieb博士发表声明,宣布FDA将继续大力推进基因疗法的开发,并发布了6大新指南。在今天的这篇文章中,药明康德微信团队也将为各位读者整理分享新指南的具体内容。
药明康德译自FDA - 基因疗法,FDA,指南,创新疗法 - 2018-07-16
2014上半年FDA批准的新药
2014年已走过一半时间,仅从FDA的新药审批结果来看,医药行业吹来暖风。2014上半年FDA批准了18个新药,相比2013上半年有明显增长。GSK、强生、诺华、礼来、阿斯利康、默沙东等大型药企在今年各有斩获。 由于2012年小型制药企业递交新药上市申请的数量激增,FDA的新药批准数量在2012年达到了39个的历史高点。随着2013年FDA批准的新药数量急剧下降至27个,人们也开始对全球新药研发
生物探索 - 新药,FDA - 2014-07-02
葛兰素史克再生障碍型贫血药物将获FDA审批
葛兰素史克称,美国联邦食品和药物管理局已经将在美国使用Promacta为商标名,在欧洲使用Revolade为商标名的eltrombopag确定为在治疗严重再生障碍型贫血上,具有“突破性疗效”的药物。
腾讯财经 - 新药,FDA - 2014-02-07
为您找到相关结果约500个