化药口服固体制剂连续制造技术指导原则(试行)
为指导企业研发,统一审评尺度,助力ICH《Q13:原料药和制剂的连续制造》指导原则在国内实施,在国家药品监督管理局的部署下,药审中心组织起草了《化药口服固体制剂连续制造技术指导原则(试行)》。根据《国
国家药品监督管理局药品审评中心 - 化药口服固体制剂 - 2023-03-28
给药沟通:医生必须掌握的5C原则
先来看一则笑话:一个县长被免职了,气成了植物人,被送到医院。医生诊断后说:“给他念个官复原职的通知兴许就好了。”妻想:“既然要念,干脆念个厅长,让他高兴高兴。”哪知县长一听挺身而起,大笑气绝。医叹:“不遵医嘱,擅自加大剂量。”(来自网络)其实,这种笑话在现实中同样可以找到影子。新闻一:2014年9月3日,京华时报曾报道:中国红十字会统计显示,我国每年医疗损害事件造成约40万人非正常死亡,是交通
健康界 - 医生,医患沟通技巧,药 - 2015-08-26
急性髓系白血病新药临床研发技术指导原则
为鼓励抗肿瘤新药研发,在国家药品监督管理局的部署下,药审中心组织制定了《急性髓系白血病新药临床研发技术指导原则》。根据《国家药监局综合司关于印发药品技术指导原则发布程序的通知》(药监综药管
国家药品监督管理局药品审评中心 - 急性髓系白血病 - 2023-02-18
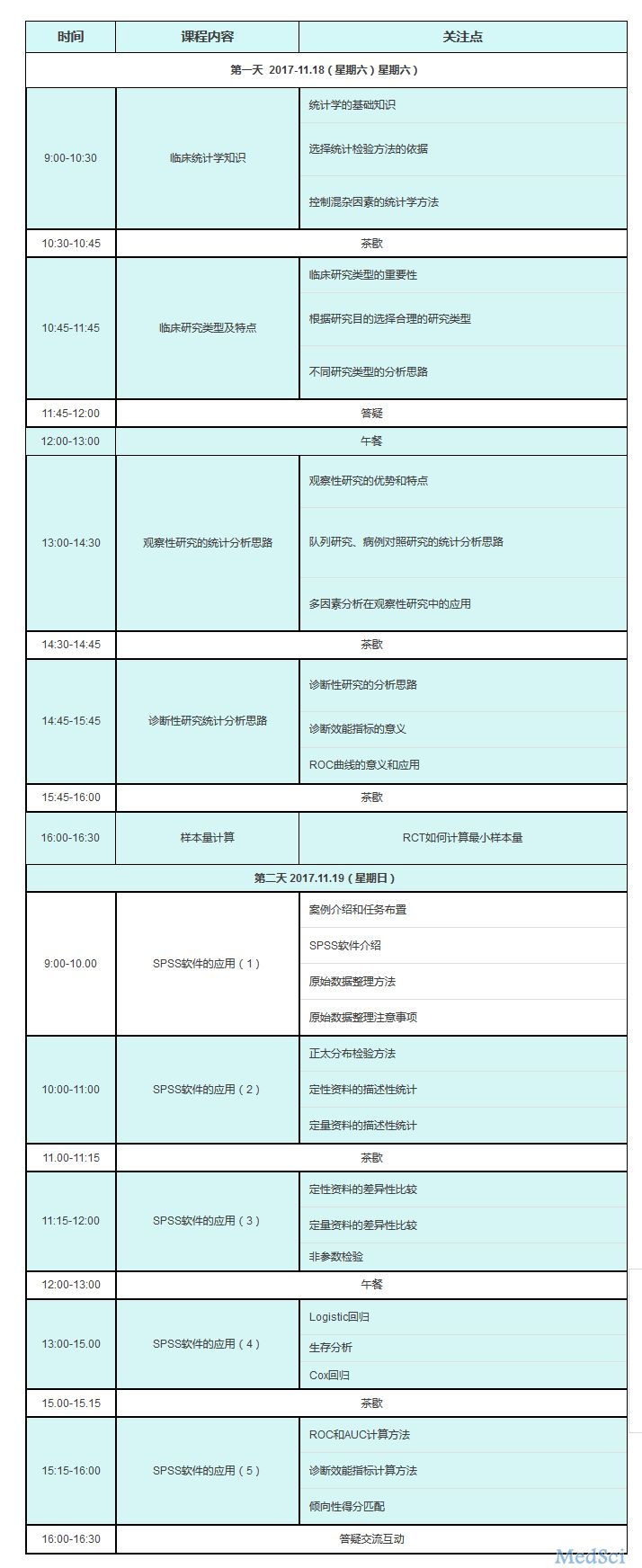
双十一特别呈现-临床常用统计方法选择的原则
梅斯医学将于11月18-19在上海(徐汇区宜山路425号光启城办公楼3楼)举办第三届统计策略学习班!通过系统性的学习,双十一期间报名有惊喜哦!系统性教您各种临床研究类型如何选择统计方法,注意的细节和问题,SPSS软件手把手操作,解决您实际动手中遇到的困扰,通过本次课程能够独立使用软件统计数据。系统性教您各种临床研究类型如何选择统计方法,注意的细节和问题,SPSS软件手把手操作,解决您实际动手中
MedSci原创 - 临床常用统计方法 - 2017-11-13
成人2型糖尿病药物临床研发技术指导原则
为鼓励2型糖尿病药物临床研发,进一步规范临床研究设计和相关技术要求,在国家药品监督管理局的部署下,药审中心组织制定了《成人2型糖尿病药物临床研发技术指导原则》。
国家药品监督管理局药品审评中心 - 成人2型糖尿病,药物临床研发技术 - 2023-02-28
他达拉非片生物等效性研究技术指导原则
不断丰富完善仿制药个药指导原则并持续推进一致性评价工作,进一步指导他达拉非片生物等效性研究的实施和评价
国家药品监督管理局药品审评中心 - 他达拉非片 - 2022-11-29
抗肿瘤药物说明书不良反应数据汇总指导原则
随着抗肿瘤药物研发的进展,越来越多的研究表明,一种药物可以应用于不同瘤种、同一瘤种的不同阶段或人群,还可以与不同作用机制的药物联合。药品说明书是药品安全性信息最主要的载体,是指导安全、合理使用药品的重
国家药监局药审中心 - 抗肿瘤药物 - 2022-04-22
总局发布医疗器械临床试验设计指导原则
1月8日,食品药品监管总局发布通告称,为贯彻落实中共中央办公厅、国务院办公厅《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号),加强医疗器械产品注册工作的管理,进一步提高注册审查质量,鼓励医疗器械研发创新,国家食品药品监督管理总局组织制定了医疗器械临床试验设计指导原则(见附件),现予发布。
新浪医药新闻 - 医疗器械,CFDA,指导原则 - 2018-01-09
基因治疗产品长期随访临床研究技术指导原则(试行)
为指导和规范基因治疗类药物临床试验,提供可参考的技术规范,在国家药品监督管理局的部署下,药审中心组织制定了《基因治疗产品长期随访临床研究技术指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发
CDE - 基因治疗 - 2021-12-08
FDA仿制药一致性评价指导原则
I. 简介II. 背景III. 一致性 A. 一致性定义 B. 一致性范围内的指南1. 在待处理的公民请愿、复议申请和终止申请中提出的一致性问题2. 有关FDA仍在考虑中的问题3. 更适合通过其他机制回复的问题 C. 一致性范围外的指南1. 一致性定义中的特殊情况2. 一致性范围外的主题3. 一致性范围外的实体IV. 提交一致性评价
MedSci原创 - FDA,仿制药,一致性评价 - 2018-11-01
抗菌药物临床应用指导原则(征求意见稿)(2014版)
目录第一部分 抗菌药物临床应用的基本原则抗菌药物治疗性应用的基本原则抗菌药物预防性应用的基本原则抗菌药物在特殊病理、生理状况患者中应用的基本原则附录1抗菌药物在预防某些细菌性感染中的应用附录2抗菌药物在预防手术部位感染中的应用附录3抗菌药物在预防特殊诊疗操作部位感染中的应用第二部分 抗菌药物临床应用管理一、医疗机构建立抗菌药物临床应用管理体系二、抗菌药物临床应用实行分级管理三、病原微生物检验四、注
2014-01-01
放射性体内诊断药物非临床研究技术指导原则
为推动和规范我国放射性体内诊断药物的研发,在国家药品监督管理局的部署下,药审中心组织制定了《放射性体内诊断药物非临床研究技术指导原则》(见附件)。根据《国家药监局综合司关于印发药品技术指导原则发布程序
CDE - 指导原则 - 2021-05-13
为您找到相关结果约500个