这些人不得接种新冠疫苗
我国从2020年12月15日开始对重点人群开展新冠病毒疫苗接种工作,目前已经过去了两个多月的时间,现在各地的新冠病毒疫苗接种工作进展如何?接种证明能否替代核酸检测报告?老人、孕妇、备孕期、哺乳期妇女…
央视网 - 新冠疫苗 - 2021-02-26
病例分享:查梅毒却引出另一种疾病!
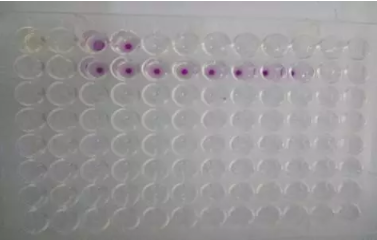
前几日,本院某内科病房女患者检测术前四项,梅毒检测中的梅毒螺旋体颗粒凝集试验(TPPA)呈现不一样的检测结果(见下图第一排1-4号孔):未致敏颗粒凝集,成阳性反应(++),致敏颗粒沉淀为(-)。
检验视界网 - 梅毒,非特异抗体,自身免疫检测 - 2017-12-02
德药管机构警告:慎用诺氟沙星等氟喹诺酮类药物
德国联邦药品与医疗器械管理局8日警告说,使用诺氟沙星、左氧氟沙星等氟喹诺酮类药物可能产生“严重且持久”的副作用,抗感染治疗时一定要慎用此类药物。此外,该机构还发布了有关限制此类药物使用的新规定。
新华网 - 德药管机构,诺氟沙星,氟喹诺酮类 - 2019-04-11
德国警告慎用诺氟沙星等药物,或产生严重且持久副作用
德国联邦药品与医疗器械管理局8日警告说,使用诺氟沙星、左氧氟沙星等氟喹诺酮类药物可能产生“严重且持久”的副作用,抗感染治疗时一定要慎用此类药物。此外,该机构还发布了有关限制此类药物使用的新规定。
新华社 - 诺氟沙星,药物,副作用 - 2019-04-09
国家版药品监控目录发布 20家上市公司人心惶惶!
7月1日晚间,国家卫生健康委办公厅、国家中医药局办公室正式发布《关于印发第一批国家重点监控合理用药药品目录(化药及生物制品)的通知》(以下简称“通知”),神经节苷脂、脑苷肌肽、奥拉西坦等20种药品被列入首批目录通知要求,各医疗机构要建立重点监控合理用药药品管理制度,加强目录内药品临床应用的全程管理。值得注意的是,上述20种药品均为化药及生物制品,首批国家重点监控合理用药药品目录中未包含中药注
新浪医药新闻 - 国家版药品监控目录 - 2019-07-04
限期将至,白内障“神药”莎普爱思滴眼液或将停产?
莎普爱思制药有限公司(以下简称莎普爱思)发布公告称,公司曾于2017年12月7日收到原浙江省食品药品监督管理局《转发国家食品药品监督管理总局关于莎普爱思滴眼液有关事宜的通知文件
医谷网 - 白内障 - 2020-10-29
临床医生如何委托代理申请专利
2、尽量详细的填写“技术交底书”(代理人会提供模板)。如为结构型产品,需提供产品CAD制图;如为化合物或制备方法等需提供结构式、流程图、结构框图等;如为外观设计专利,提供产品的六面视图。3、将技术交底书交与代理人,同时签订专利申请代理合同及委托书等文件,缴纳申请费及代理费。4、配合代理人补充相关技术资
MedSci原创 - 临床医生,委托,代理,申请专利 - 2015-03-04
国办印发文件开展仿制药质量和疗效一致性评价
仿制药是与原研药具有相同的活性成分、剂型、给药途径和治疗作用的药品。开展仿制药质量和疗效一致性评价工作,要求已经批准上市的仿制药品,要在质量和疗效上与原研药品能够一致,临床上与原研药品可以相互替代。
新华社 - 仿制药,疗效,质量 - 2016-03-08
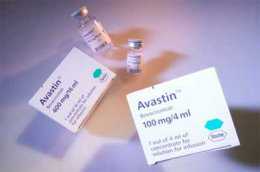
Drug Saf:贝伐珠单抗不良事件报告分析
贝伐珠单抗最初于2004年由美国FDA批准用于治疗转移性结肠癌和其他实体瘤,是第一个血管内皮生长因子(VEGF)抑制剂。但上市前的临床试验检测某些不良事件的能力有限,因此FDA和生产商需要收集和监测上市后的不良事件报告。 研究者从美国FDA不良事件报告系统(AERS)数据库中检索了2004年2月~2009年9月报告的贝伐珠单抗的新不良事件,对贝伐珠单抗和其他所有药物进行失衡分析,通过设置比例报告
环球医学网 - 贝伐珠单抗,不良事件,美国FDA - 2012-07-23
强效降压药进入医保目录,上海开出全国首张处方
《国家基本医疗保险、工伤保险和生育保险药品目录(2022年)》新增了ARB类强效降压药——美阿沙坦钾片,助力中国高血压患者从这一创新降压药物的治疗中获益,实现早期血压达标。
梅斯医学 - 降压药,美阿沙坦钾片 - 2023-03-01
深度透视:国内化学药企新药批文的赚钱效应
药品批文可以视为药品生产企业的“弹药库”,药品批文能否持续获得可以作为生产企业持续成长的一种标准。
医学经济报 - 新药批文,赚钱效应 - 2015-03-20
电视剧药品广告植入,胃药能不能这样吃?
如今的电视剧,广告植入已成常态,其中药品广告植入也不少见,有些还特别尴尬,比如古装剧里出现感冒冲剂。最近热播的《我的前半生》里也有大把植入,当主角们加班加点、压力倍增时,胃药怒刷了一波存在感。
澎湃新闻 - 胃药‘用药规范’ - 2017-07-16
儿科用药研发可参考成人数据
5月18日,国家食品药品监督管理总局发布《成人用药数据外推至儿科人群的技术指导原则》,鼓励研发企业在儿科人群用药开发早期阶段,就数据外推与监管部门进行沟通,最大程度利用已有数据,减少不必要的儿科研究,进一步鼓励研制儿科用药
健康报 - 儿科,用药 - 2017-05-22
为您找到相关结果约500个