重磅:FDA批准功能性治愈乙肝药物研究,未来有望上市
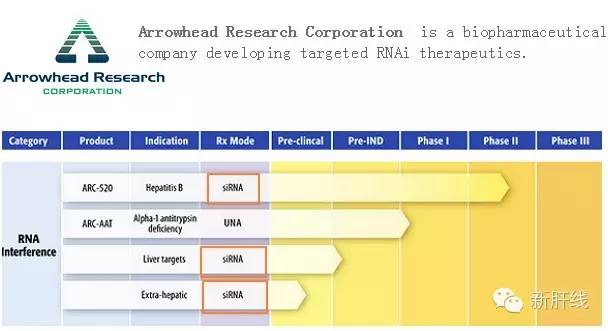
2014年8月,总部位于加利福尼亚州帕萨迪纳市的生物技术公司Arrowhead宣布公司开发的用于治疗乙肝的RNAi药物ARC-520取得良好研究数据。2015年3月,Arrowhead耗资3500万买进了诺华抛弃的RNAi项目,此外在2011年,Arrowhead以同样的方式买进了被罗氏放弃的RNAi项目。 目前,Arrowhead公司有3种RNAi药物处于临床开发阶段,乙肝药物ARC-520是
MedSci原创 - FDA,乙肝 - 2016-02-16
默沙东抗真菌药物诺科飞®注射液剂型在华上市
泊沙康唑口服混悬液可用于预防侵袭性曲霉菌和念珠菌感染及治疗口咽念珠菌病,泊沙康唑肠溶片及泊沙康唑注射液均可用于预防侵袭性曲霉菌和念珠菌感染及治疗侵袭性曲霉病。
默沙东 - 2022-12-21
国家药监局已累计批准54个创新医疗器械产品上市
近年来,国家药监局贯彻落实《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)和《中央办公厅国务院办公厅关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号),深入推进医疗器械审评审批制度改革,加速医疗器械创新发展。自《创新医疗器械特别审批程序》发布以来,截止2018年12月31日,已有197个产品进入创新医疗器械特别审查通道,批准神经外科手术导航定位
国家药品监督管理局 - 创新医疗器械产品 - 2019-01-13
新包装HPV疫苗上市 新增药品追溯码和热稳定标签
新改版的宫颈癌九价疫苗已于5月份在中国内地上市,疫苗包装上印着“九价人乳头瘤病毒疫苗(酿酒酵母)”的简体中文,还增加了药品追溯码和热稳定标签,消费者可以通过扫码查询疫苗溯源信息辨别真伪,还能通过热稳定标签的颜色判断疫苗是否变质
北京青年报 - HPV疫苗,包装,药品 - 2019-06-15
4家上市,16家完成融资,医疗服务产业还有多少想象空间?
相对于火热的创新药、创新器械,以及科创板带来的更为多样的退出机制,2019年的医疗服务产业,略显得低调。
动脉网 - 医疗服务,市场发展 - 2019-10-24
国内获批上市的5款PD-L1抑制剂
国内获批上市的5款PD-L1抑制剂:阿得贝利单抗、舒格利单抗、恩沃利单抗、阿替利珠单抗和度伐利尤单抗。
网络 - PD-L1抑制剂,国内获批 - 2023-03-26
中国真实世界证据论文荣登BMJ“中国专辑”
真实世界证据在中国的实施究竟面临着哪些困难?为推进真实世界证据在中国的发展,我国医药界需要付诸哪些行动?针对这些问题,四川大学华西医院中国循证医学中心主任孙鑫教授、国家食品药品监督管理总局药品不良反应监测中心李馨龄处长及同事于2018年2月5日,在《英国医
MedSci原创 - 真实世界证据,BMJ,中国专辑 - 2018-02-08
NMPA授予Tagrisso(osimertinib)上市许可,治疗EGFR突变的非小细胞肺癌
国家医疗产品管理局(NMPA)已授予Tagrisso(osimertinib)作为一线治疗的上市许可。
MedSci原创 - NMPA,Tagrisso,EGFR突变,非小细胞肺癌 - 2019-09-05
CALC中国专场:国际学术舞台需要中国声音
设立初衷,美梦初圆 CALC中国专场的设立源于白教授在荷兰阿姆斯特丹参与上届WCLC的切身感受。“中国学者参会人数众多,但往往是旁观者,缺乏主持和发言机会,亟待一个在全世界面前集体亮相的舞台”。在这种想法驱动下,他积极与WCLC组织方进行沟通,并最终促成中国专场呈现在全球学者面
中国医学论坛报 - 肺癌,诊断,筛查 - 2013-11-06
CALC中国专场:点睛中国研究、指明未来方向
关键点1 中国研究或改变临床实践 CTONG 0806研究作为本届WCLC新闻发布会唯一推荐的中国研究,是仅有的2项受推荐的肿瘤内科治疗研究之一,也是继今年美国临床肿瘤学会
中国医学论坛报 - 肺癌,研究 - 2013-11-06
今日,施一公创立的诺诚健华递交港股上市申请
今日(10月17日),根据港交所信息,诺诚健华(Innocare)已递交港股上市申请,联席保荐人为摩根士丹利和高盛。
医谷 - 签,诺诚健华,肿瘤药物研发,港股上市,施一公 - 2019-10-17
首个国产重组人乳头瘤病毒疫苗“馨可宁”获批上市
国家药品监督管理局12月31日消息,近日,国家药品监督管理局批准厦门万泰沧海生物技术有限公司的双价人乳头瘤病毒疫苗(大肠杆菌)(商品名:馨可宁(Cecolin))上市注册申请,该药是首家获批的国产人乳头瘤病毒疫苗目前全球已上市的HPV疫苗有3种,分别是英国葛兰素史克公司生
国家药品监督管理局 - 人乳头瘤病毒,馨可宁,上市 - 2020-01-01
2005-2015年FDA抗肿瘤新药上市申请失败原因大盘点
为了掌握美国FDA否决抗肿瘤新分子实体药物新药上市申请的原因,美国FDA药品评审中心的管理人员系统调查了2005年3月17日到2015年3月17日这十年间,向美国FDA提交的抗肿瘤新分子实体药物新药上市申请的审批情况对美国FDA否决的抗肿瘤新分子实体药物,详细研究了新药上市申请被拒绝的深层原因,以期对从事抗肿瘤新分子实体药物研发的企业提供参考。 一、2005-2015年抗肿瘤新分子实体药物新药
新康界 - 抗肿瘤新药 - 2015-07-29
为您找到相关结果约500个