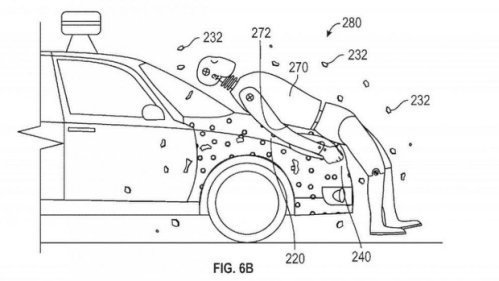
临床医生可以申请哪些类型专利?
2016年11月1日,中央全面深化改革领导小组审议通过《关于深化职称制度改革的意见》,自2016年11月1日起实行。《意见》提出“探索以专利成果、项目报告、工作总结、工程方案等成果形式替代
中国组织工程研究杂志 - 专利 - 2020-12-31
化药创新药临床申请量翻番
近日,国家食品药品监督管理总局发布《2017年度药品审评报告》指出,我国去年共审评批准化药创新药临床试验申请399件,涉及170个品种,较2016年创新药临床试验批准数量翻了一番;在审评批准创新药临床试验的品种中
健康报 - 化药,创新药,临床申请 - 2018-03-26
临床医生如何自己申请专利
1、判断所拥有的技术是否属于可以申请专利的范畴确定自己的技术方案可以申请的专利类型。2、撰写专利申请文件发明专利的申请文件:发明专利请求书,说明书(必要时应有附图),权利要求书,摘要及其附图,纸质各一式两份或电子版各一份。涉及氨基酸或核苷酸序列的发明专利申请,说明书中应包括该序列表,并把该序列表作为说明书的一个单独部分提交,同时应提交符合国家知识产权局规定的记载有该序列表的光盘或软盘。实用新型
MedSci原创 - 临床医生,申请专利 - 2015-03-04
临床医生如何委托代理申请专利
1、初步判断所拥有的技术是否属于可以申请专利的范畴;或与代理人沟通,确定技术内容是否可以申请专利。2、尽量详细的填写“技术交底书”(代理人会提供模板)。3、将技术交底书交与代理人,同时签订专利申请代理合同及委托书等文件,缴纳申请费及代理费。4、配合代理人补充相关技术资
MedSci原创 - 临床医生,委托,代理,申请专利 - 2015-03-04
一大波重磅新药申请临床获CDE受理
尽管solanezumab之前的两项 III 期临床研究EXPEDITION1(n=1012)和 EXPEDITION 2(n=1040 )均告失败,均未能改善AD患者的认知和生活自理能力,礼来最终还是决定再
医药魔方数据 - 新药,临床申请 - 2016-06-16
又一个罕见病药物免临床申请上市
近日,根据新药研发监测数据库(CPM)显示,辉瑞研发的罕见病药物氯苯唑酸获CDE免临床受理,通过《接受药品境外临床试验数据的技术指导原则》进行上市申报,之前在国内未进行过临床实验。
医谷综合报道 - 辉瑞,罕见病,临床试验 - 2019-07-31
临床发表的SCI在2018年国自然(NSFC)申请中的作用
今天,我们来聊一下:临床发表的SCI与国自然(NSFC)的关系。
解说国自然 - 临床发表,SCI,国自然(NSFC),申请 - 2017-12-23
国药新冠疫苗国内上市申请获受理,III期临床仍在继续
24日,国药集团北京生物制品研究所的新型冠状病毒肺炎灭活疫苗(Vero 细胞)上市申请获国家药监局药审中心(CDE)受理。目前,受理号已经在CDE官网显示。
亿欧 - III期临床研究,新冠疫苗,受理 - 2021-01-11
国外上市急需药品可以直接在CDE申请上市,免做临床
8月8日,药品审评中心(CDE)发布了《关于征求境外已上市临床急需新药名单意见的通知》,其对近年来美国、欧盟或日本批准上市新药进行了梳理,遴选出了Alectinib Hydrochloride 等48个境外已上市临床急需新药名单,可提交或补交境外取得的全部研究资料和不存在人种差异的支持性材料,直接提出上市申请。
生物探索整理自CDE - 急需药品,药品管理,CDE,境外 - 2018-08-09
临床医生为什么要申请专利?
MedSci原创 - 专利 - 2015-09-08
抗肿瘤新药首次人体临床试验申请临床相关资料准备建议
优化临床试验审评审批制度是当前改革重点之一,临床试验方案将成为临床审评重点,内容结构完整的、高质量、可评价的临床试验方案是高效完成审评的保障。抗肿瘤新药是全球创新药研发热点,在当前创新药临床试验申请中大约占40%。然而,现阶段抗肿瘤药物首次
NMPA - 抗肿瘤,新药 - 2018-12-12
参展申请
analytica China 是亚洲的国际级展览盛会,它吸引了来自全球的参展商聚集到中国上海这块被全世界看好的市场上。在其他重要的经济地区,如印度和拉美等地,类似展会也正在筹划中。2008年的展出的重点是面向化工、制药、食品饮料和环保等领域的分析测试仪器、实验室技术与管理以及化学制品和试剂。 来自分析仪器和生命科学领域知名的国内外领先企业已经纷纷表示将会参加本次展会。analytica Chin
会议 - 2008-06-17
为您找到相关结果约500个