认识应激性心肌病
2023-10-02 重症医学 重症医学 发表于陕西省
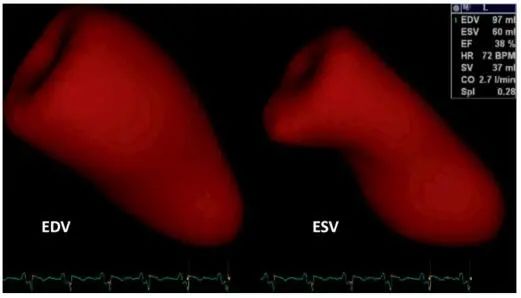
应激性心肌病是一种急性可逆的综合征,以室壁运动异常为主要特征,可能存在心尖部运动减低或心室基底部阶段性反常运动。
引言
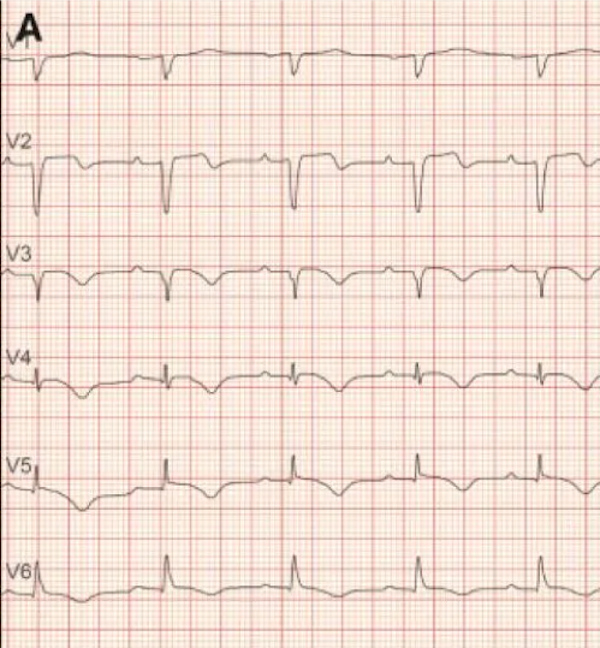
一位76岁的老年女性的一个亲密的朋友去世了。数小时后她开始出现胸痛,大汗和呼吸急促。她来到急诊室,心电图显示心前区导联T波倒置,心肌肌钙蛋白升高。
这就是应激性心肌病心肌缺血的典型表现。
辨别应激性心肌病与急性冠脉综合征的差别对于临床医师来说至关重要,因为他们的病生理学改变及治疗的差别是非常大的。
应激性心肌病是一种急性可逆的综合征,以室壁运动异常为主要特征,可能存在心尖部运动减低或心室基底部阶段性反常运动。尽管最终结局一般比较好,但是在临床过程的早期,患者可能出现心源性休克(4%),恶性室性心律失常(1-2%)和死亡(1-1.5%)。在ICU中应激性心肌病可能使其他的情况变得更加复杂,特别是蛛网膜下腔出血。具有这些复杂表现的患者通常给临床治疗带来了挑战。本文目的在于提高对应激性心肌病病生理学鉴别的认识来帮助职业医生治疗这个有趣的综合征。
诊断
Mayo Clinic提出的诊断标准如表1所示。应激性心肌病是一种神经心源性现象—情绪应激,其他应激状态,药物,特殊的儿茶酚胺类或神经损伤会刺激其发生,但是缺乏适当的外部应激因子不能够诊断。大多数患者表现为胸痛和/或呼吸困难,并且绝经后妇女高发,其原因尚不清楚。心电图表现异常,30-50%患者表现为ST段抬高和心前区导联T波倒置,奇怪的是大多在休息是发作。心肌钙蛋白升高即便是适当的升高。利用冠脉血管造影排除梗阻性冠状动脉疾病(CAD)对于排除急性冠脉综合症(ACS)并且做出诊断是十分关键的。特殊的基底部心尖球形综合征能够通过心室造影、超声心动图或MRI检查发现;MRI缺少延迟钆显像能够排除缺血性心肌坏死或心肌炎。据报道有多种不同的形式(心尖部室间隔运动功能减退和“倒章鱼篓”,基底部运动功能减退和正常心尖部功能),这可能与潜在的神经病原学有很大的关系。这些不同形式的准确发病率和地理分布可以从一项最新的国际性注册研究(INTERTAK)的数据中得到澄清。所观察到的右室受累的案例超过30%.
不管其存在多种不同的表现形式,应激性心肌病最主要的特征就是这事一个短暂的并且能够在数天到数周内消退的综合征。从这个意义上说,诊断的建立需要排除ACS并且要通过辨别标记物和症状来得到确认。

发病机理
应激性心肌病起初是Dote等在日本提出的,由于左心室的形状类似于日本渔民的章鱼鞘而被称为“Takotsubo心肌病”。由于缺乏梗阻性冠状动脉疾病的形态学上的表现而认为冠脉痉挛是其发生机制,但是后来这种观点并未得到支持—在这些患者中自发的冠脉痉挛极其罕见(药理学因素激发痉挛是一个困难重重的领域)并且更重要的是室壁运动障碍与单个冠状动脉的解剖学分布并不一致。
应激性心肌病缘于儿茶酚胺类的过度分泌。很多的证据支持这种发病机制。应激性心肌病患者血浆儿茶酚胺水平升高,伴随神经肽-Y水平的升高,其伴随着交感神经节后和肾上腺嗜铬细胞的儿茶酚胺而生成,在应激时释放。应激性心肌病患者进行心肌活检发现心肌收缩带坏死,一个与儿茶酚胺过剩(例如嗜铬细胞中)相关的罕见的细胞异常,这与心肌梗死的凝固性坏死是截然不同的。心尖球形综合征能够在应激性心肌病大鼠模型中得到复制,并且能利用肾上腺素阻滞剂的预处理来阻止其发生。
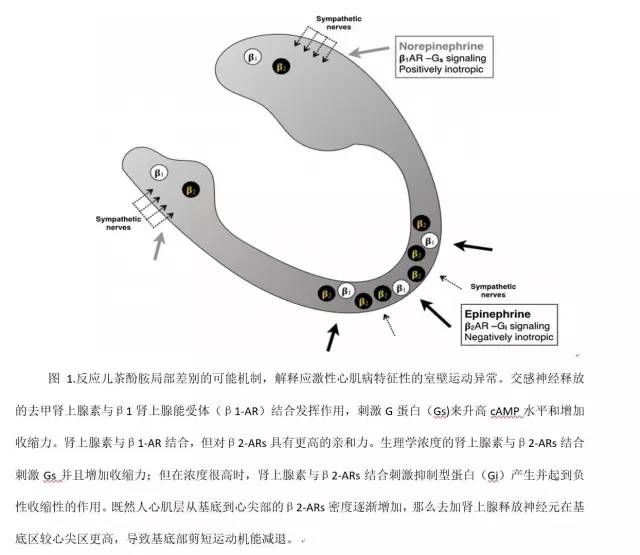
近年来提出高水平肾上腺素对心肌G蛋白信使的影响是应激性心肌病特征性心尖反常运动的发生机制(图1)。去甲肾上腺素通过与β1-肾上腺素受体(β1-AR)结合刺激G蛋白(Gs)升高cAMP水平来增加收缩力。肾上腺素也能与β1-AR结合,但对β2-ARs有更高的亲和力。生理浓度的肾上腺素与β2-ARs结合刺激Gs并增加收缩力;但是在高浓度时情况发生了改变,肾上腺素与β2-ARs结合刺激抑制型G蛋白(Gi)并产生负性收缩作用。既然人心肌的β2-ARs浓度从基底到心尖逐渐增加,那么和它想匹配的Gs到Gi的转换也就能解释应激性心肌病时心尖区室壁运动的异常。临床前的模型也支持这种假说,心尖部功能障碍对肾上腺素有反应而不是去加肾上腺,这是由于PKA介导的β2-ARs磷酸化从而发生从Gs到Gi的转换。
这种机制也能够解释应激性心肌病的痊愈过程。β2-ARs与抑制型G蛋白能够抑制心律失常并且刺激保护机制,也促进心肌再生。伴随循环中肾上腺素的清除,肾上腺素水平回复正常水平,收缩力增强,也就有助于解释心肌功能障碍的快速解决的机制。
应激性心肌病的其他机制也归因于病理生理学。虽然心外膜冠状动脉痉挛可能并不常见,但是冠脉微血管收缩可以是自发的。研究也表明冠脉血流和心肌血流速率的异常都是反映微血管系统的指标。氧化应激诱导的儿茶酚胺过度分泌也可能是潜在的机制。
在一些患者中室壁运动异常表现形式不同的原因并不明确。基因遗传性可能是答案的一部分,但是我们的理解还不够充分。有趣的是,G蛋白受体激酶多态性增加遗传基因和Gs-to-Giβ2-ARs的结合,这可能与经典的应激性心肌病有很大的联系。为何女性受累者占优势仍然是个谜—有人认为可能与雌激素有关,但是大多数患者是绝经后的女性。β1/β2-ARs的比值改变或微血管功能障碍的遗传易感性可能是相关因素
治疗
应激性心肌病的治疗主要是支持治疗。ACS患者在心导管介入治疗前先开始抗血小板治疗,这可能需要中止。据报道心尖运动不良可以造成心尖部血栓形成,但是常规抗凝并不能表示没有记录的血凝块。
肾上腺素受体使病理生理趋向阻止再复发,即使缺少随机临床实验的支持,但仍有动物实验模型数据来支持这一实践。当存在血流动力学不稳定时这可能不是可取的—不管是低血压、心衰或者心源性休克。一些患者需要药理学支持。非儿茶酚胺类药物例如米力农或左西孟旦与儿茶酚胺类相比是更好的选择。在一些患者也需要机械支持手段,比如主动脉球囊反搏术、左室辅助装置或极少见的静-动脉体外膜肺氧合。应激性心肌病缓解的自然病程通常是快速的。连续的成像研究有助于明确临床过程。
据报道复发是极罕见的(2-10%)。同上β阻滞剂的病理生理学意义在不存在禁忌症的情况下可以继续使用。QT延长的患者有发生心律失常的风险直到QT间期恢复正常。
神经损伤时应激性心肌病与心源性功能异常之间存在很多的重叠,例如蛛网膜下腔出血,外伤性脑损伤和中风。曾经被称为“脑性T波”可能是对应激性心肌病的反应。在一些病例中发生“神经源性肺水肿”可能是潜在未被认知的应激性心肌病导致的。诊断是十分重要的,因为尽管长期预后是较好的,但仍有潜在的并发症,心律失常和其他一些并发症。涉及心肌、神经和肺功能的多学科协作路径对于患者的管理是十分有帮助的。
总结
应激性心肌病的表现与急性缺血性心肌病是很难分辨的,但其具有的特征是不存在冠状动脉狭窄和特征性的基底部顶端运动异常。其病生理学是儿茶酚胺过剩,引起分布性的心肌顿抑,这可以解释其分布性和β肾上腺素能受体的药理学作用。认识到这种病理生理学过程是重要的,因为其能指导治疗并且也能够解释为何临床医生应该追求强力的支持措施来期待痊愈。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言