STTT:四川大学胡以国团队发现慢性髓系白血病发病和进展的调控新机制
2023-03-05 网络 网络 发表于四川省
慢性粒细胞白血病(CML)是一种影响血液及骨髓的恶性肿瘤,它的特点是产生大量不成熟的白细胞,这些白细胞在骨髓内聚集,抑制骨髓的正常造血。
慢性粒细胞白血病(CML)是一种影响血液及骨髓的恶性肿瘤,它的特点是产生大量不成熟的白细胞,这些白细胞在骨髓内聚集,抑制骨髓的正常造血。
2023年3月1日,四川大学胡以国团队在Signal Transduction and Targeted Therapy在线发表题为“TSPAN32 suppresses chronic myeloid leukemia pathogenesis and progression by stabilizing PTEN”的研究论文,该研究表明TSPAN32通过稳定PTEN抑制慢性髓系白血病的发病和进展。该研究发现TSPAN32是Philadelphia (Ph+)白血病发病的关键节点因子。该研究发现TSPAN32的表达被BCR-ABL抑制,而伊马替尼治疗后TSPAN32异位表达抑制了Ph+细胞系的增殖。Tspan32过表达在小鼠模型中显著阻止BCR-ABL诱导的白血病进展,并损害白血病干细胞(LSCs)增殖。
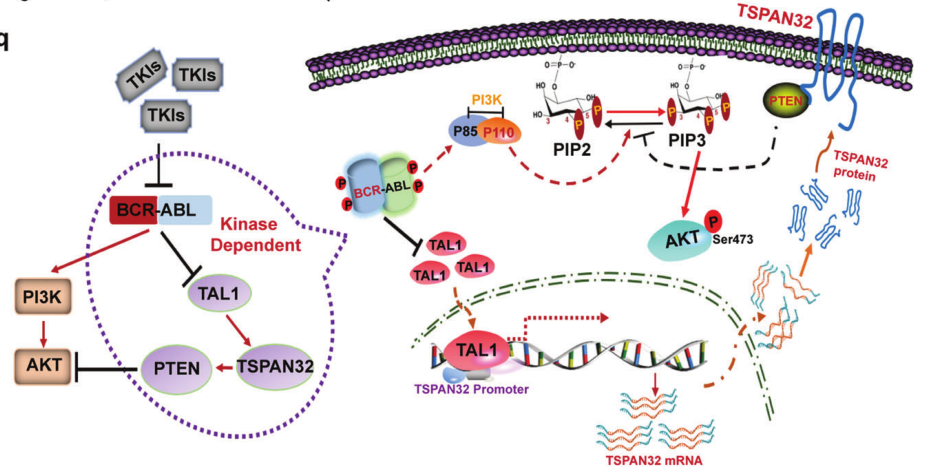
在机制上,TSPAN32被证明与PTEN相互作用,增加其蛋白水平并导致PI3K-AKT信号活性降低。该研究还发现BCR-ABL通过抑制TAL1来抑制TSPAN32。TAL1异位表达显著增加TSPAN32 mRNA和蛋白水平,说明BCR-ABL通过降低TAL1表达来抑制TSPAN32转录。总的来说,该研究发现了一个由“BCR-ABL-TAL1-TSPAN32-PTEN-PI3K-AKT”组成的新信号轴。该研究的发现进一步补充了BCR-ABL在CML发病机制中转化潜力的已知机制。这种新的信号轴也为靶向PI3K-AKT治疗CML提供了一种潜在的手段。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言