心源性休克和急性心力衰竭中应用机械循环支持的全新证据
2019-06-11 康德 王映冰 重症医学
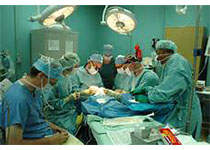
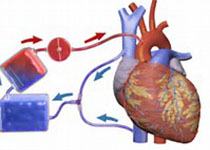
研究目的 本综述的主要目的是强调和总结最近发表的短期机械循环支持用于治疗心源性休克的研究。需要注意的是,本文重点介绍的是经皮植入装置
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#机械循环支持#
28
#急性心力衰竭#
0
#心源性休克#
28
#心源性#
29