ATVB 解放军中部战区总医院向光大教授团队发现炎症细胞源性MYDGF抑制内皮细胞LDL穿胞及抗动脉粥样硬化
2023-10-17 论道心血管 论道心血管 发表于上海
该研究揭示了炎症细胞源性MYDGF作为炎症细胞和血管内皮细胞的crosstalk因子发挥抑制内皮细胞LDL穿胞及抗动脉粥样硬化的作用。
随着社会经济发展、人民生活水平提高和人口老龄化,动脉粥样硬化发生率呈逐年增高趋势,严重危害着人们的身心健康。因此,探索防治动脉粥样硬化安全有效的方法,对改善患者预后具有重要临床意义。
低密度脂蛋白(LDL)颗粒通过穿胞的方式穿过完整血管内皮细胞,并在内皮下间隙沉积是动脉粥样硬化发生发展的关键环节,但是,如何抑制血液循环中LDL在内皮细胞的穿胞仍需进一步研究。炎症与动脉粥样硬化的发展密切相关,慢性炎症已成为动脉粥样硬化的治疗靶点。然而,研究发现抗炎治疗并不总是改善心血管疾病结局,甚至发现抗炎治疗与危害信号相关,这驳斥了炎症在动脉粥样硬化中完全有害的观点。尽管炎症细胞在动脉粥样硬化中的有害作用已被提出多年,但目前炎症细胞对动脉粥样硬化的潜在益处知之甚少。
髓源性生长因子(MYDGF)是一种主要由骨髓衍生的单核和巨噬细胞(炎性细胞)产生的分泌蛋白,在心血管、代谢性等多种疾病中发挥较为关键的作用。本团队之前的研究表明,MYDGF可以促进肠道L细胞合成和分泌胰高血糖素样肽-1、减轻糖尿病小鼠足细胞损伤、缓解血管内皮细胞炎症、减少肝细胞脂肪沉积并改善非酒精性脂肪肝病、增加小鼠骨量并缓解骨质疏松症。然而,炎症细胞源性MYDGF与内皮细胞LDL穿胞的关系目前尚不清楚。
2023年9月28日,解放军中部战区总医院向光大教授团队在Arterioscler Thromb Vasc Biol杂志上发表“Inflammatory Cell-Derived MYDGF Attenuates Endothelial LDL Transcytosis to Protect Against Atherogenesis”论文,揭示了炎症细胞源性MYDGF作为炎症细胞和血管内皮细胞的crosstalk因子发挥抑制内皮细胞LDL穿胞及抗动脉粥样硬化的作用。

首先,研究者对炎症细胞特异性MYDGF敲除小鼠的主动脉内膜层进行RNA-seq分析,发现与小窝相关内吞、大分子穿胞密切相关的条目明显被富集,因此推测MYDGF与LDL穿胞可能存在相关性。为初步探索MYDGF与内皮细胞LDL穿胞的关系,在临床及小鼠实验中,研究者发现下肢动脉粥样硬化人群及动脉粥样硬化小鼠血清MYDGF表达水平与对照组相比明显下降,且LDL穿胞相关分子(Cav1和Cavin-1)表达显著增加,血清MYDGF与Cav1、Cavin-1 mRNA呈负相关关系。因此,研究者推测MYDGF是否通过影响LDL穿胞抑制内膜下LDL堆积以发挥改善动脉粥样硬化的作用。研究亦验证了MYDGF主要来源于炎症细胞,尤其是巨噬细胞和单核细胞。
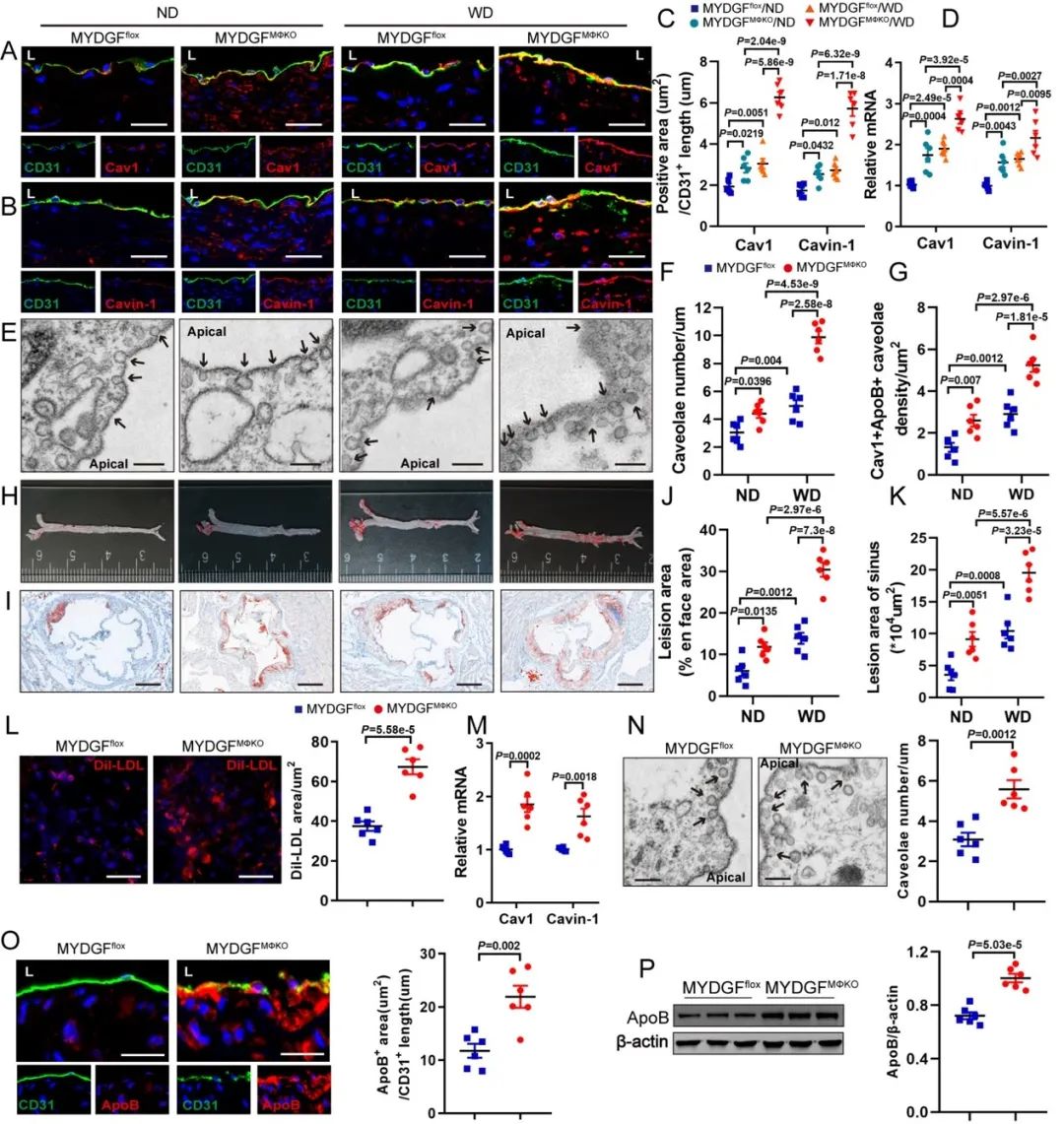
基于上述结果,研究进一步阐明了炎症细胞源性MYDGF与内皮细胞LDL穿胞的深入联系。研究者选用Ldlr敲除及炎症细胞特异性MYDGF敲除小鼠(MYDGFMΦKO),构建动脉粥样硬化模型以及开展Dil-LDL急性跟踪实验,结果显示炎症细胞源性MYDGF缺乏加重内皮细胞LDL穿胞、促进内皮细胞对LDL的摄取、增加内皮下间隙ApoB的沉积,从而加重动脉粥样硬化。
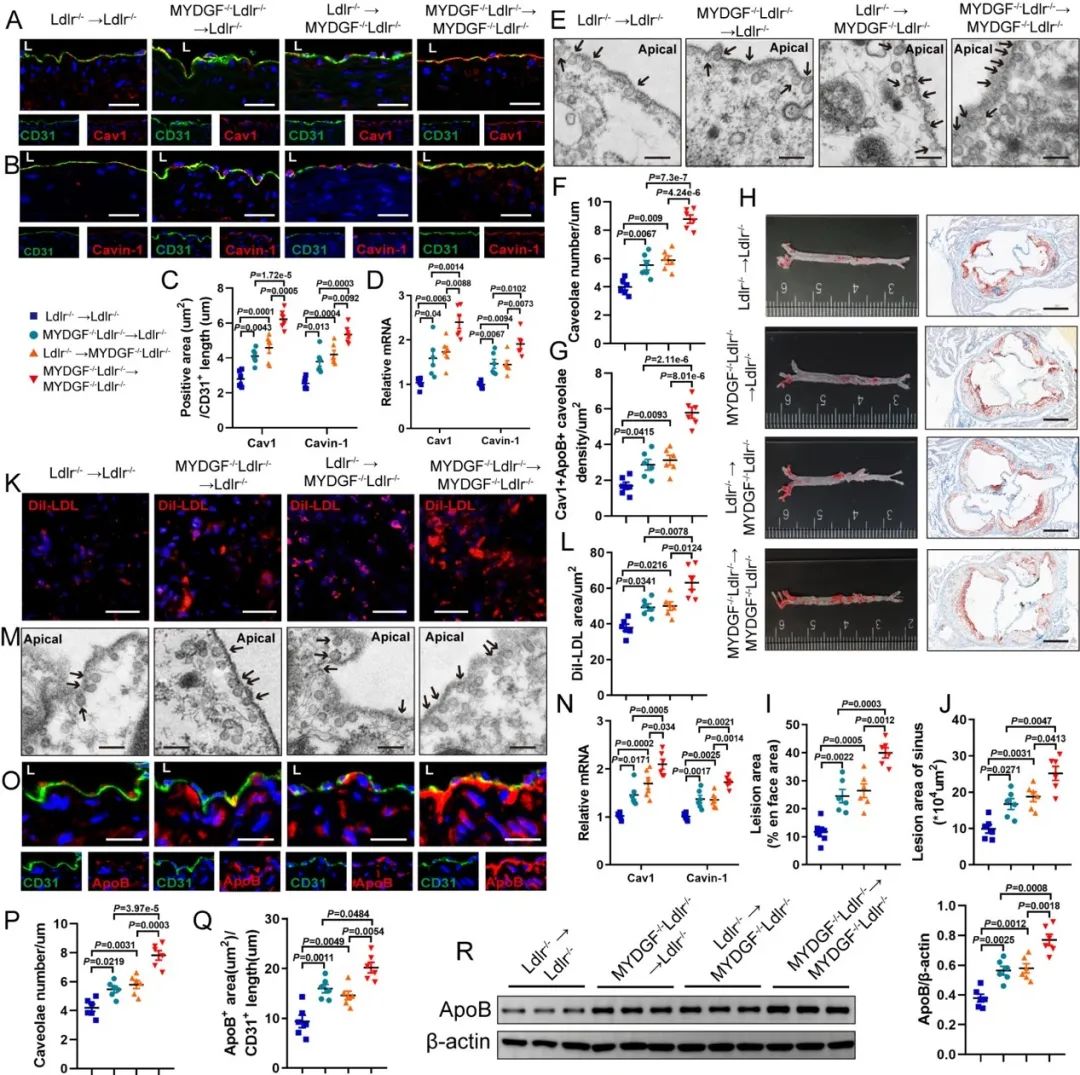
研究者通过骨髓移植恢复炎症细胞MYDGF表达以及构建炎症细胞MYDGF过表达小鼠模型进一步证实炎症细胞源性MYDGF对内皮细胞LDL穿胞的调控作用,结果发现,炎症细胞MYDGF恢复及过表达时,内皮细胞Cav1和Cavin-1的表达降低、内皮细胞小窝数量减少、内皮下间隙ApoB表达减少,表明炎症细胞源性MYDGF具有抑制小鼠内皮细胞LDL穿胞、减少内皮下间隙ApoB堆积从而缓解动脉粥样硬化的作用。体外实验中,MYDGF+/+小鼠来源的巨噬细胞和重组MYDGF可减少MAECs对LDL的穿胞和摄取,进一步证实了体内试验的结果。
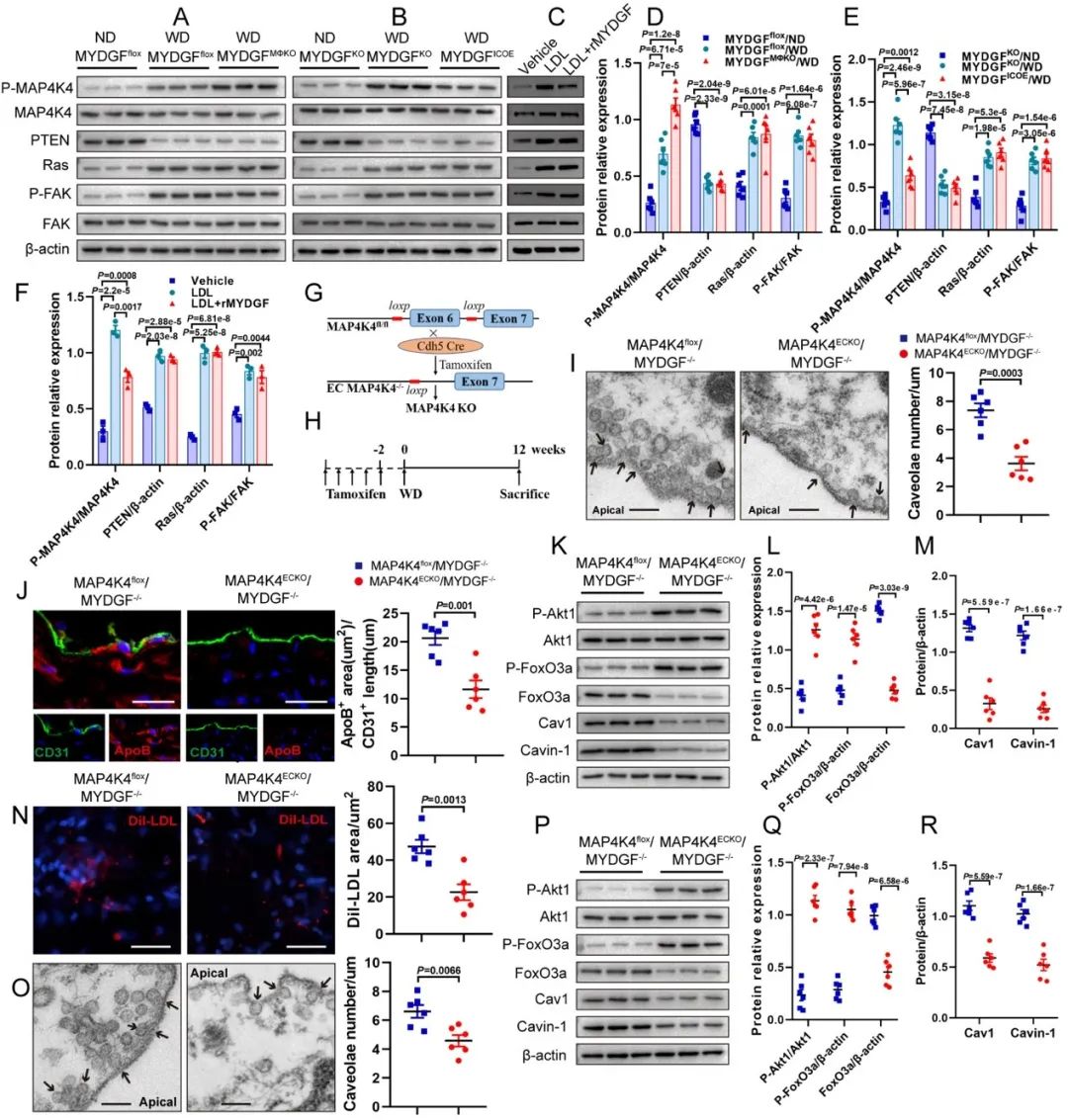
在具体机制研究中,研究团队首先对RNA-seq进行KEGG分析,发现PI3K/Akt信号通路和FoxO信号通路被显著富集,说明PI3K/Akt和FoxO信号通路有可能参与MYDGF对内皮细胞LDL穿胞的调控作用,且已知Akt信号受MAP4K4的调节,因此,在体内和体外实验中探索了炎症细胞源性MYDGF调控LDL穿胞的分子机制。通过动物及细胞实验,研究者证实MYDGF可能通过抑制内皮细胞MAP4K4、增加Akt1,以及减少FoxO3a信号级联反应来减少内皮细胞LDL穿胞、改善动脉粥样硬化。
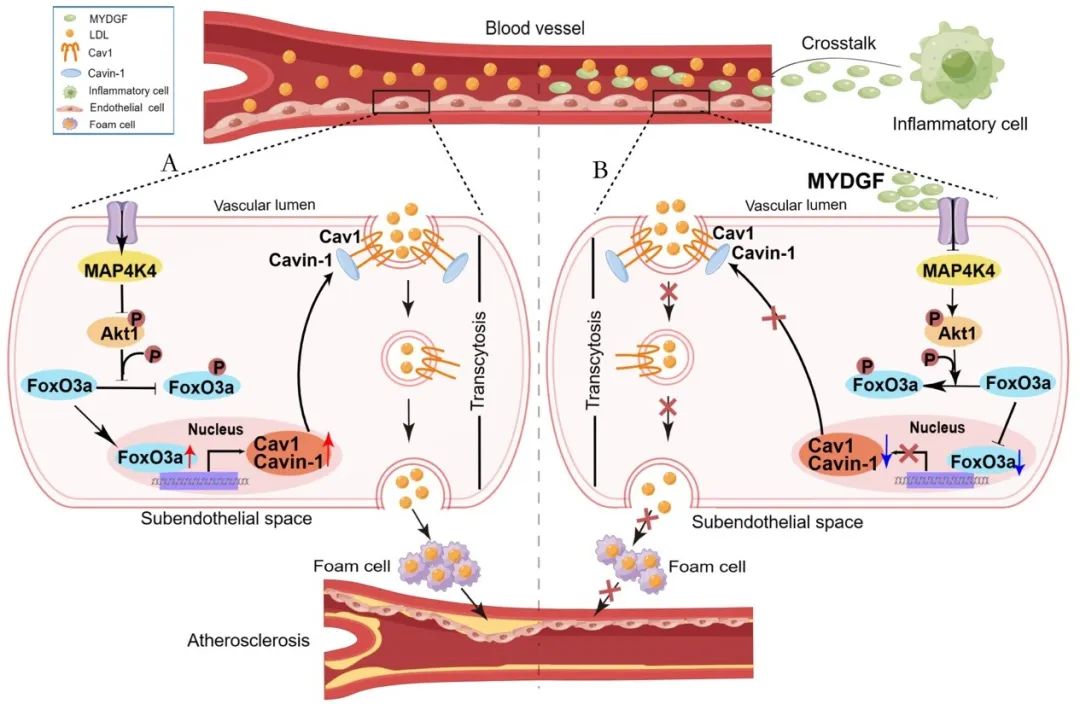
综上,该研究表明,炎症细胞源性MYDGF作为炎症细胞和血管内皮细胞的crosstalk因子发挥抑制内皮细胞LDL穿胞的作用,MAP4K4/Akt1/FoxO3a信号级联反应可能介导了MYDGF对LDL穿胞的调节作用。该发现为MYDGF可能成为动脉粥样硬化的新治疗药物提供了理论基础,炎症细胞在动脉粥样硬化中的有益作用值得进一步关注。
本研究由解放军中部战区总医院向光大教授团队完成,向光大教授、乐岭教授为本文共同通讯作者,博士生徐金玲为本文第一作者。本项目受到多项国家自然科学基金的资助。
原文链接:
https://doi.org/10.1161/ATVBAHA.123.319905
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#动脉粥样硬化#髓源性生长因子(MYDGF)是一种由炎性细胞产生的分泌蛋白,与血管内皮细胞的crosstalk因子发挥抗动脉粥样硬化的作用,这为#MYDGF#可能成为动脉粥样硬化的新治疗药物提供了理论基础,炎症细胞在动脉粥样硬化中的有益作用值得进一步关注。
40