读书报告 | 高TMB的MSS胃肠道肿瘤的突变分析
2024-01-03 iCombo iCombo 发表于上海
该研究认为TMB和正向调节抗肿瘤免疫的基因突变的组合可能是患者选择免疫检查点抑制剂治疗的一个有前景的工具,同时该研究也为免疫检查点抑制剂和靶向细胞周期蛋白D1或FGFs的药物的组合提供了新的见解。
导读
与错配修复缺陷(dMMR)或微卫星高不稳定性(MSI-H)无关的高肿瘤突变负荷(TMB-H)的胃肠肿瘤的基因组特征尚未得到很好的研究。本文是探索MSS胃肠道肿瘤与TMB-H分子特征的最大样本量研究。研究结果显示,MSS胃肠道癌症中TMB-H的患病率为3.29%,并非所有与TMB-H相关的突变都能提高抗肿瘤免疫应答。特定的基因突变如SMAD2、MTOR、KEAP1、NFE2L2、RB1、TERT和RASA1可能会削弱TMB-H的抗肿瘤免疫应答,而其他16个基因(CDC73、CTNNA1、ERBB4、EZH2、JAK2、MAP2K1、MAP2K4、PIK3R1、POLE、PPP2R1A、PPP2R2A、PTPN11、RAF1、RUNX1、STAG2和XPO1)突变可能与TMB-H的抗肿瘤免疫应答增强有关,而不依赖dMMR/ MSI-H。同时该研究构建了一个预测免疫检查点抑制物疗效的模型(mTMB)。
该研究认为TMB和正向调节抗肿瘤免疫的基因突变(如mTMB)的组合可能是患者选择免疫检查点抑制剂治疗的一个有前景的工具,同时该研究也为免疫检查点抑制剂和靶向细胞周期蛋白D1或FGFs的药物的组合提供了新的见解(Lancet Oncol.2023 Feb;24(2):151-161. doi: 10.1016/S1470-2045(22)00783-5)。
研究背景
PD-1或PD-L1免疫检查点抑制剂(ICIs)的引入使癌症治疗发生了革命性的变化,然而ICIs疗效存在差异表明还需继续识别和验证预测ICIs有效性的生物标记物。
基于Keynote-158研究结果,高肿瘤突变负荷(TMB-H)被认为与ICIs的持久反应有关,美国 (FDA)批准Pembrolizumab用于治疗TMB-H(≥10突变/兆基)晚期实体肿瘤。然而,KEYNOTE-158研究结果不涉及所有肿瘤类型,肿瘤组织类型不同导致临床获益差别较大,并且一些常见的癌症(如结肠直肠癌)未纳入研究的前瞻性生物标记物分析中。此外,评估仅限于总体应答率(ORR),而不是生存优势,这些限制了TMB作为一种高效有力生物标志物的应用。
MSI-H被认为是ICIs疗效的积极预测因子。然而,超过90%的胃肠道肿瘤是微卫星稳定(MSS),对MSS型胃肠癌患者的研究显示,TMB-H作为ICIs有效性的预测生物标志物的结果喜忧参半。
一些研究显示在不考虑错配修复缺陷(dMMR)或MSI-H状态的情况下,TMB-H胃癌的ORR高于TMB-L;而另一些研究表明在MSS型胃癌和结直肠癌中,TMB-H与临床获益(如ORR、PFS和OS)无显著关联。因此,尽管FDA批准了Pembrolizumab作为MSS胃肠道肿瘤ICIs疗效的预测生物标志物,但仍需谨慎使用。
越来越多的证据表明,新抗原的质量可能比数量更能准确地预测ICIs的疗效。基因突变可以对多肽呈递、瘤内异质性和肿瘤免疫微环境产生影响,这都影响新抗原的免疫原性。然而,目前的TMB评分系统没有考虑到这一复杂的生物学过程。因此,更好地了解TMB-H且MSS胃肠道肿瘤分子特征可以为未来患者选择、肿瘤-免疫相互作用的生物学以及开发更合理的免疫治疗组合提供新的见解。本研究旨在探讨TMB-H相关的分子特征对肿瘤免疫微环境的影响以及ICIs对MSS胃肠道肿瘤的生存益处。
研究设计
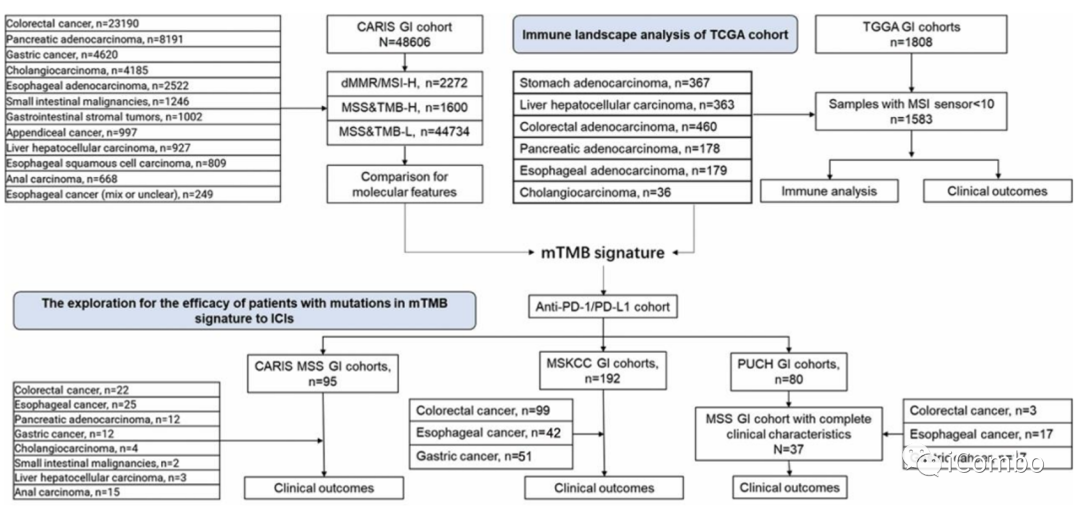
研究结果
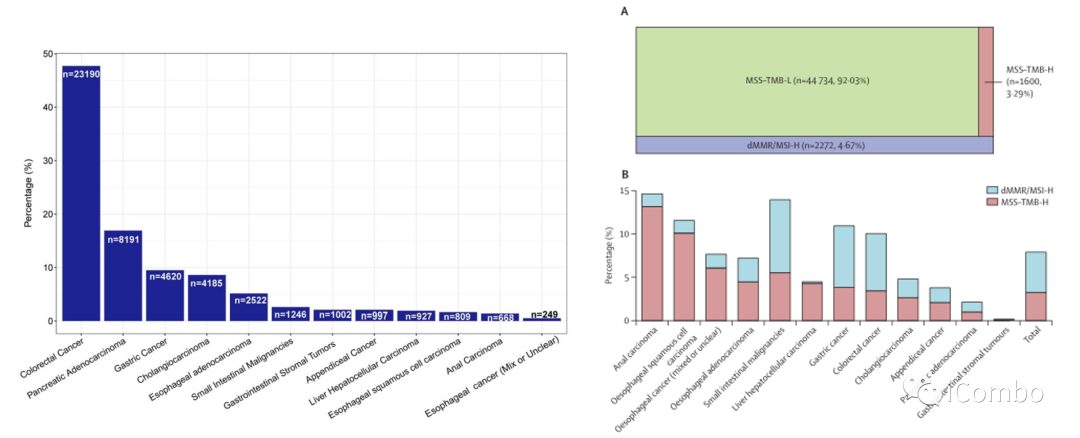
CARIS队列中最常见的肿瘤类型是结直肠癌;MSS-TMB-H在整个队列中占比3.29%,dMMR/MSI-H和MSS-TMB-L分别为4.67%和92.03%
MSI和TMB状态在12种不同肿瘤组织中的分布:MSS-TMB-H的占比从0.10%到13.17%,最高为直肠癌(13.17%[88/668]),其次是食管鳞癌(10.01%[81/809]),最低的是胃肠道间质瘤(0.10%[1of 1002])
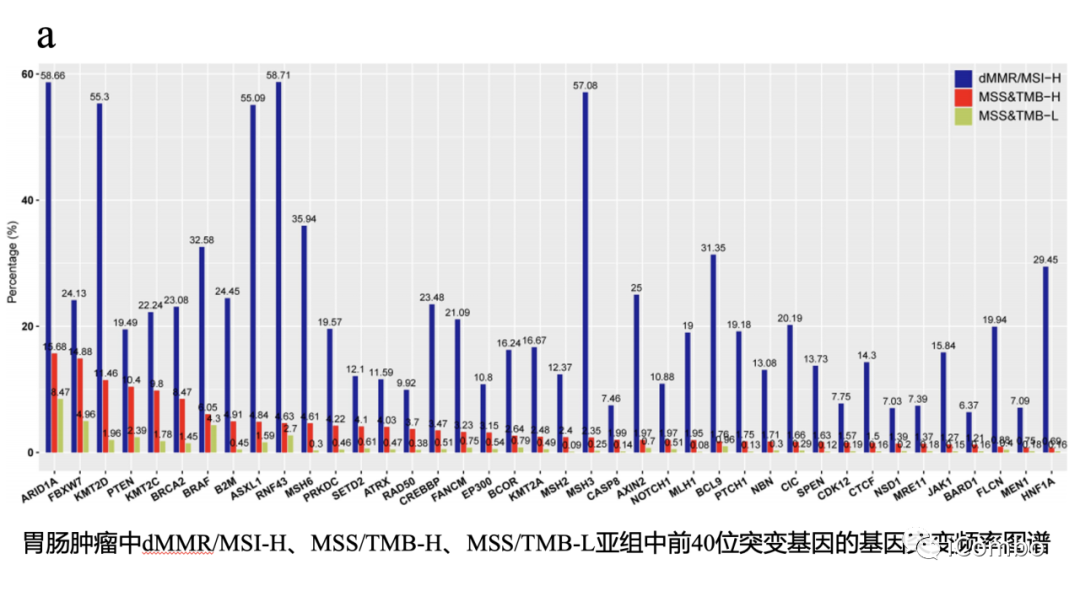

基因突变在dMMR/MSI-H亚组最常见,其次是MSS-TMB-H和MSS-TMB-L亚组
移码突变在dMMR/MSI-H亚组中丰富,而无义突变在MSS-TMB-H亚组中丰富
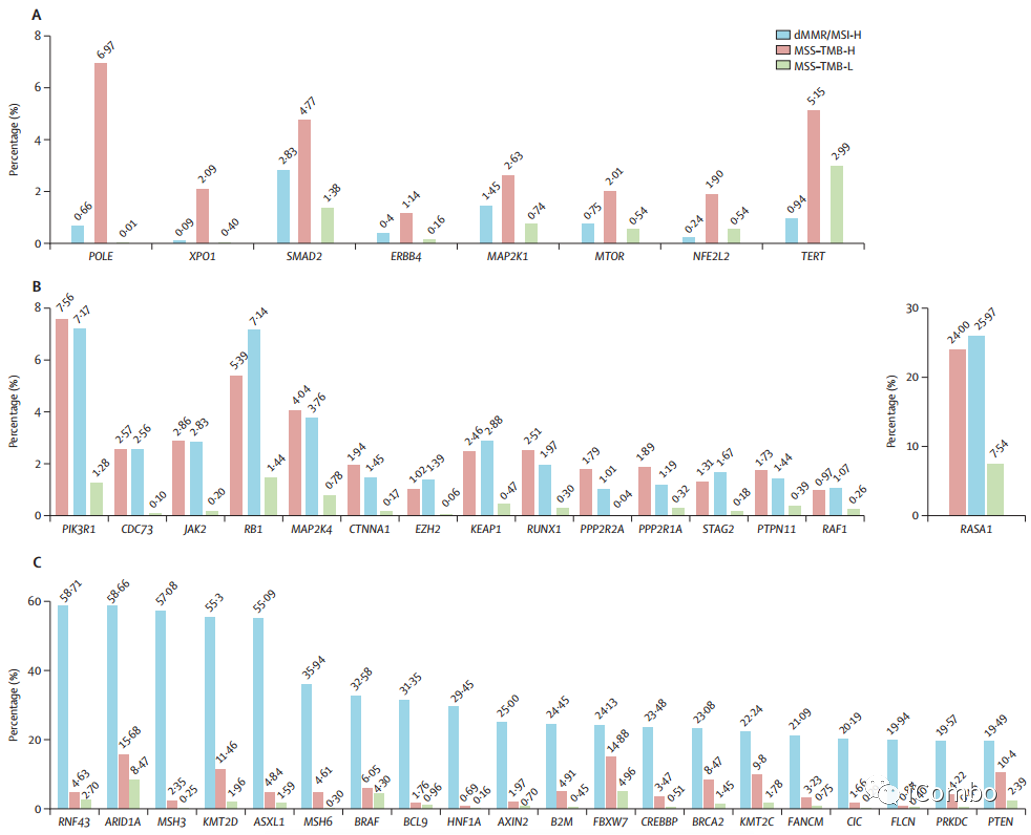
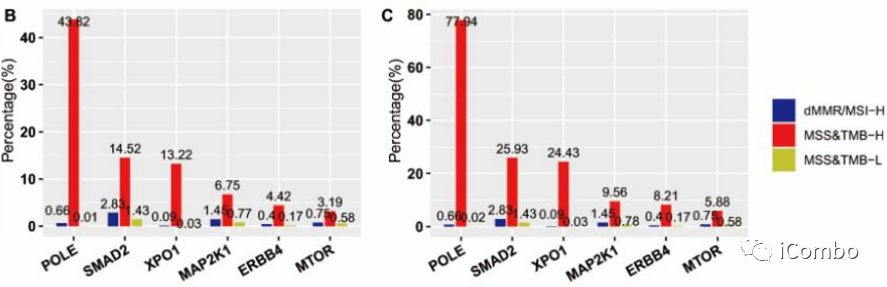
与其他亚组相比,MSS-TMB-H亚组中突变率显著升高的基因有POLE、XPO1、Smad2、ERBB4、MAP2K1、MTOR、NFE2L2、TERT,这8个基因被定义为基因组A;其中POLE在该亚组的突变率最高;且随着TMB截断点的增大,POLE在MSS-TMB-H中突变率升高;
PIK3R1、CDC73、JAK2、RB1、MAP2K4、CTNNA1、EZH2、Keap1、RUNX1、PPP2R2A、PPP2R1A、STAG2、PTPN11、RAF1和RASA1等15个基因突变频率在dMMR/MSI-H和MSS-TMB-H亚组之间相似,但在MSS-TMB-L亚组中显著降低,将这15个基因称为基因组B;
RNF43、ARID1A、MSH3、KMT2D和ASXL1基因在MSS-TMB-H亚组的突变率显著低于dMMR/MSI-H亚组,但显著高于MSS-TMB-L亚组。
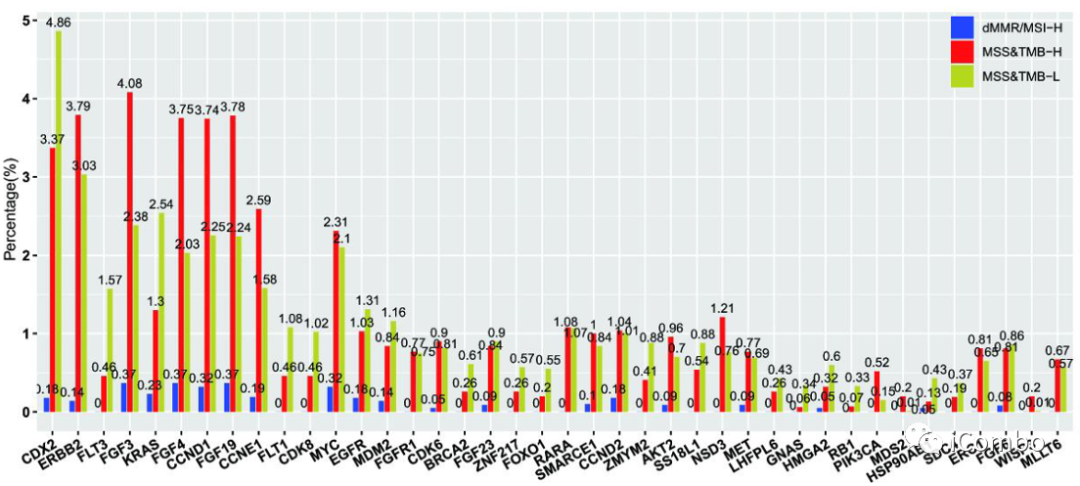
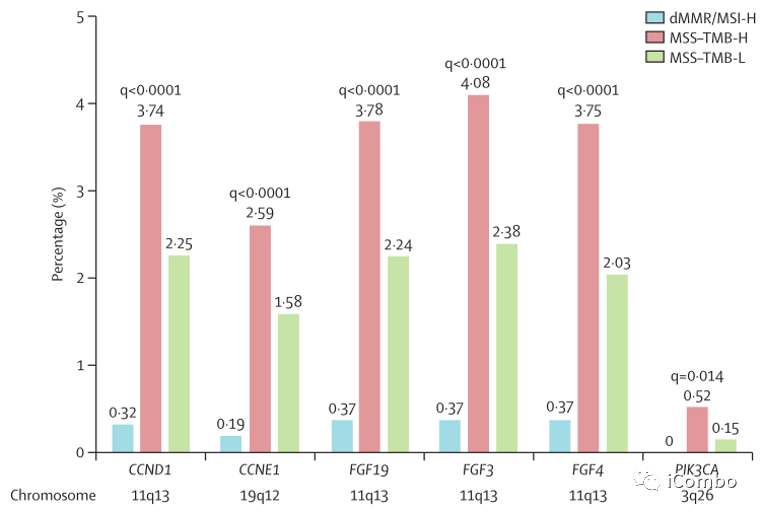
拷贝数扩增在两个MSS亚组中比在dMMR/MSI-H亚组中更常见;
CCND1、CCNE1、FGF19、FGF3、FGF4、PIK3CA在MSS-TMB-H亚组中的扩增率显著高于dMMR/MSI-H和MSS-TMB-L亚组,且这些基因大多位于染色体11q13上。
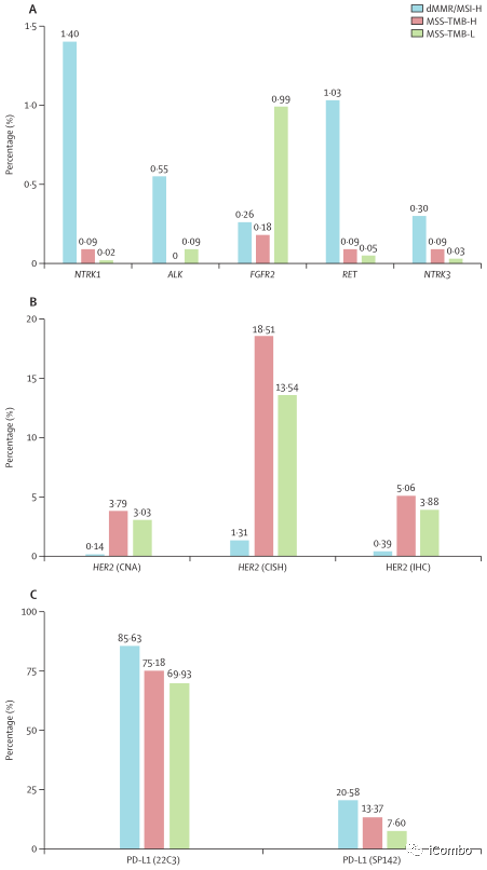
NTRK1、ALK、RET和NTRK3基因融合在MSS-TMB-H和MSS-TMB-L亚组中都很少见,在dMMR/MSI-H亚组中最高。然而,FGFR2融合在MSS-TMB-L亚组中比在dMMR/MSI-H和MSS-TMB-H亚组中更普遍;
HER2在MSS-TMB-H亚组中阳性率最高,其次是MSS-TMB-L亚组和dMMR/MSI-H亚组,这可能为ICIs联合抗HER2治疗能增强这部分患者的疗效提供了理论解释;
PD-L1在dMMR/MSI-H亚组中表达最高,其次是MSS-TMB-H和MSS-TMB-L亚组。
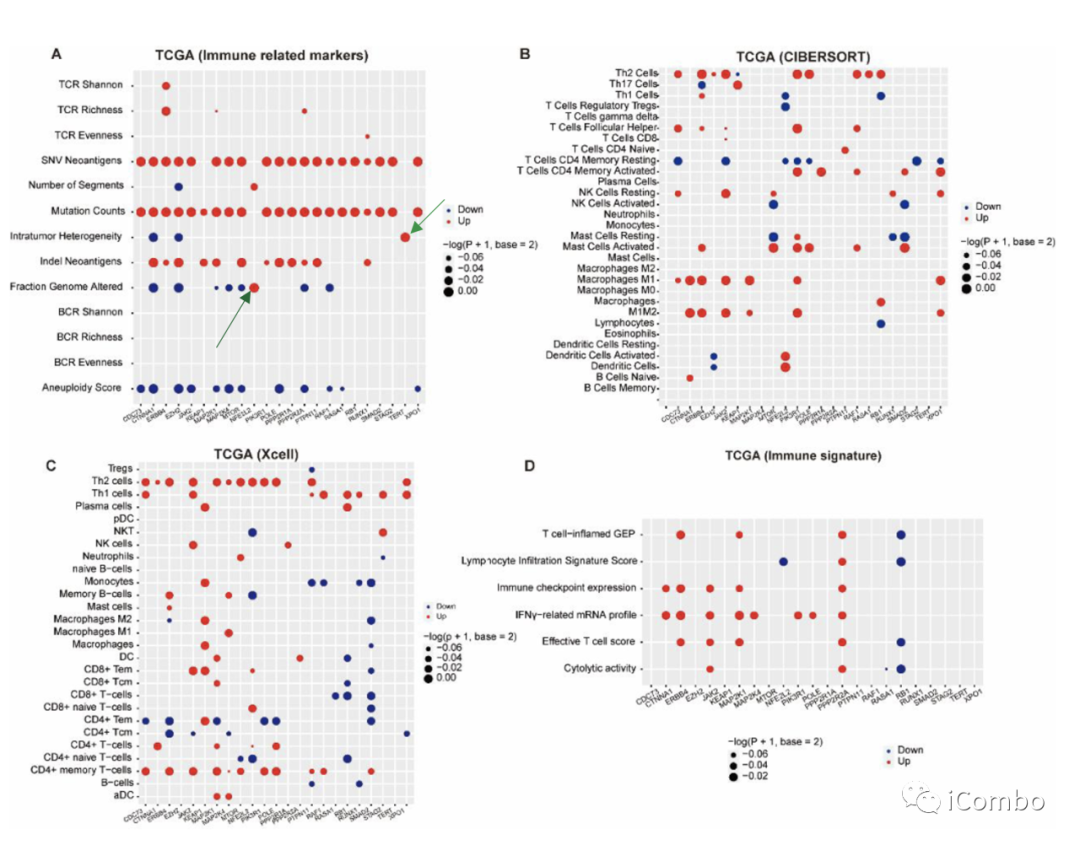
在MSS亚组中,NFE2L2和TERT突变分别显著增加了基因组改变和瘤内异质性的比例,这可能与免疫检查点抑制剂的抵抗有关;
免疫细胞浸润分析显示:MTOR、KeAP1、NFE2L2、RASA1、RB1和Smad2与抗肿瘤免疫反应(如NK细胞激活、CD8+T细胞等)呈负相关;
RB1和NFE2L2突变与免疫反应标签评分下调相关。
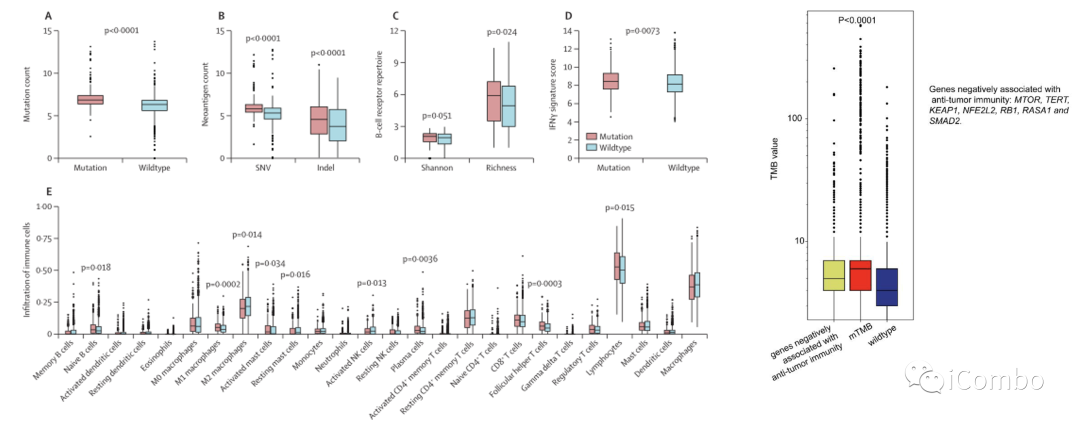
TCGA队列中,与mTMB野生型肿瘤相比,mTMB特征中任何基因突变的MSS胃肠道肿瘤的肿瘤抗原突变数、插入突变和单核苷酸变异以及B细胞受体丰度显著增加;
mTMB标志物中任何基因突变也与干扰素γ标签得分高、激活的NK细胞、M1样巨噬细胞和Th1细胞的高渗透、 M2样巨噬细胞低渗透相关;
在MTOR、TERT、Keap1、NFE2L2、RB1、RASA1或Smad2突变的MSS肿瘤中,TMB显著低于mTMB中有任何基因突变的亚组,但高于野生型mTMB的亚组。
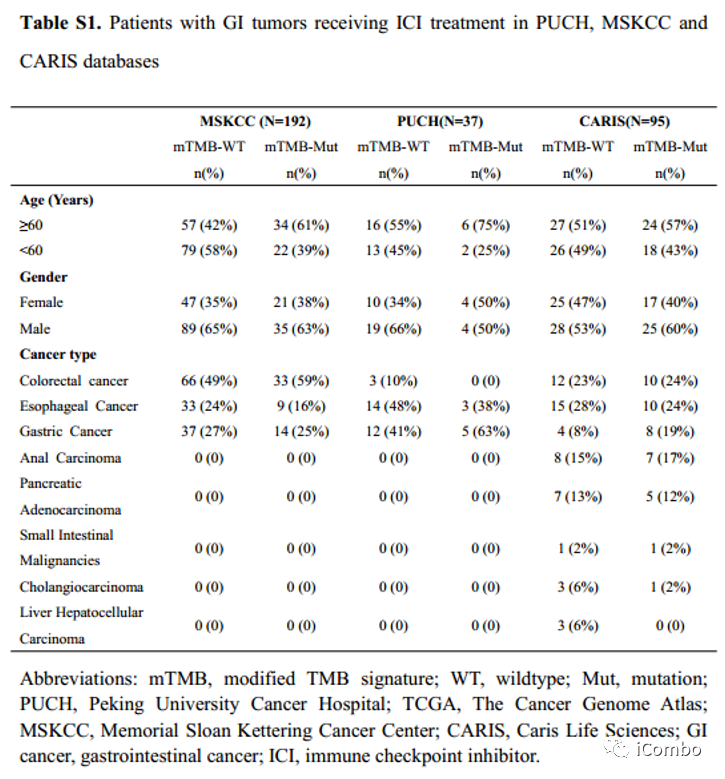
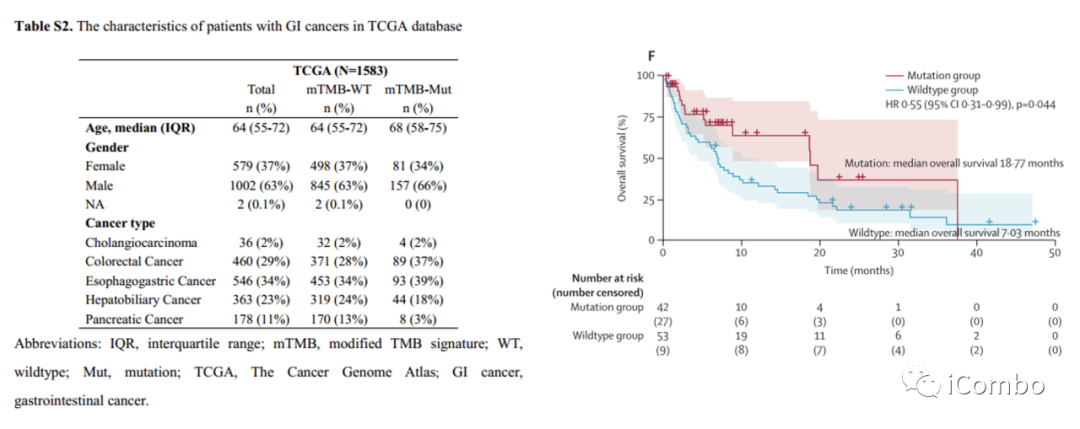
在CARIS队列中接受ICIs治疗的患者中,经过中位随访时间为22.10个月后,mTMB有任何突变的患者(n=42)的OS显著长于mTMB野生型肿瘤患者;
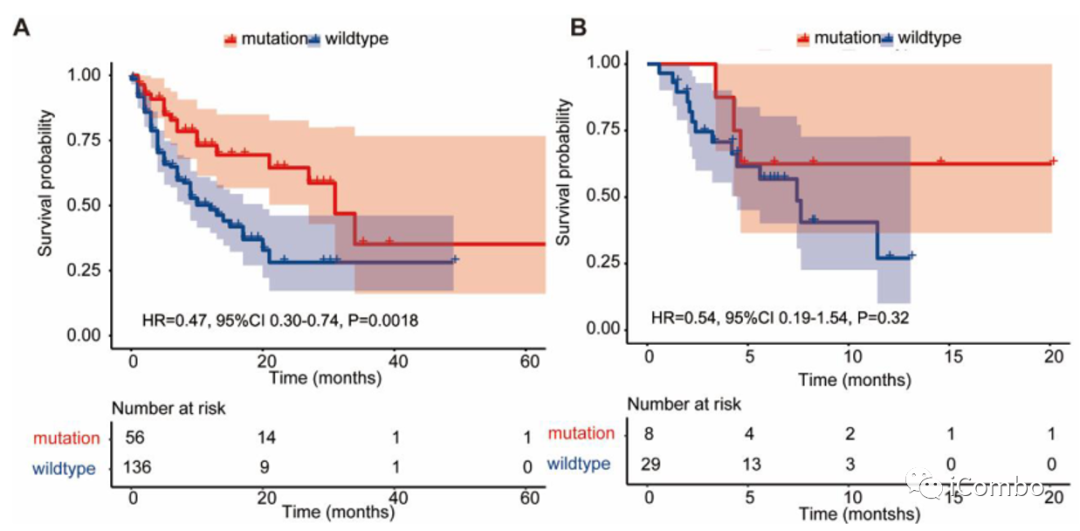
在MSKCC队列中也观察到类似的结果,但该队列无MSI-H状态结果,限制了分析;
在PUCH队列中,未观察到mTMB的任何突变与OS之间的显著关联,可能是由于样本量较小。
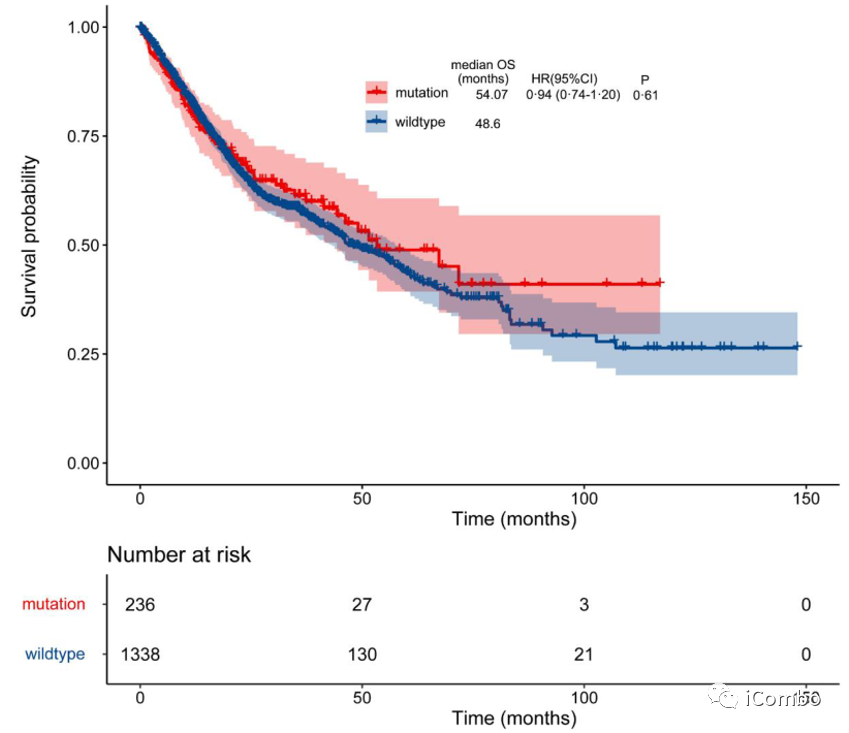
在中位随访时间为24.80个月的TCGA队列中,从未接受过ICIs治疗患者的mTMB特征基因突变与OS间无显著关联。
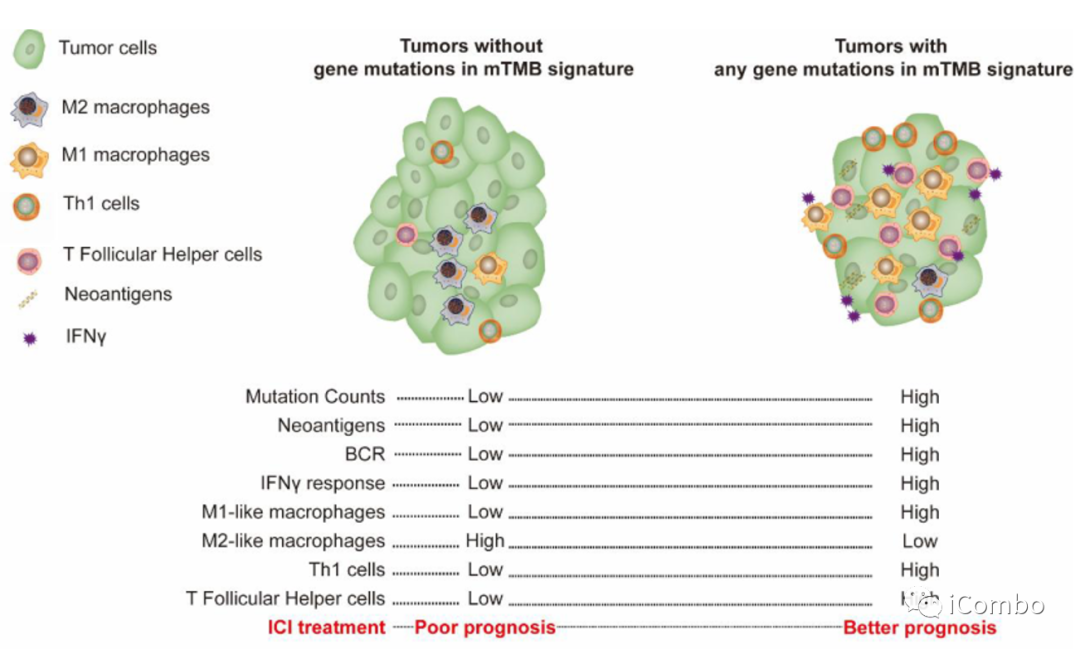
mTMB导致ICIs治疗疗效增加的潜在机制
讨论
创新性:
-
目前,这是探索MSS胃肠道肿瘤TMB-H分子特征的最大规模研究;
局限性:
-
回顾性研究;
-
不同队列中的肿瘤类型具有异质性,分别探讨每种肿瘤与TMB-H相关的基因组特征及其与ICIs疗效间的关系是需要的;
-
接受ICIs治疗的患者样本量较小,且缺乏某些类型的临床信息(如T细胞渗透密度、CPR值和抗生素治疗数据),这些可能会影响ICIs的疗效。
结论
综上所述,本研究显示,并不是所有与TMB-H相关的突变都能提高抗肿瘤免疫反应,还应考虑特定的基因突变,如Smad2、MTOR、Keap1、NFE2L2、RB1、TERT和RASA1;
TMB和正向调节抗肿瘤免疫的基因突变(如mTMB)的结合可能成为ICIs治疗患者选择的一种有前景的工具;
本研究也为靶向细胞周期蛋白D1或FGFs的药物与免疫检查点抑制剂治疗的结合提供了新的见解。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#胃肠道肿瘤# #高TMB#
19