JAMA Oncol | DA-EPOCH联合InO治疗难治/复发性B细胞ALL的疗效与免疫巩固治疗
2024-05-14 daikun MedSci原创 发表于上海
该研究旨在评估DA-EPOCH联合InO在成人B-ALL复发或难治患者中的安全性和疗效,DA-EPOCH联合InO疗法在成人B-ALL复发或难治患者中是可行的,且具有良好的安全性,毒性可控。
B-ALL(B细胞急性淋巴细胞白血病)复发或难治成人的治疗选择有限,因此需要探索新的治疗方法,InO(奥英妥珠单抗)是针对CD22阳性B细胞急性淋巴细胞白血病的单克隆抗体药物,已与低强度化疗联合使用,显示出一定的疗效,DA-EPOCH(依托泊苷、泼尼松、长春新碱、环磷酰胺和阿霉素)是一种较温和的化疗方案,用于治疗新诊断的急性淋巴细胞白血病,其疗效良好且毒性较低,该研究假设在DA-EPOCH基础上加用InO可能产生更佳的安全性和有效性,且比CAR-T等治疗更易于实施,因此,设计了一项临床研究旨在评估这一新组合疗法在成人B-ALL复发或难治患者中的安全性和疗效。

方法
该研究为一项单中心单臂的I期剂量爬坡试验,共入组24例成人B-ALL患者,使用3个剂量水平的InO联合DA-EPOCH治疗,纳入成人(≥18岁)CD22+ B-ALL复发或难治患者,要求至少有5%血或骨髓原始细胞或1个以上1.5cm或更大的髓外病变,使用3个剂量水平的InO(0.3mg/m2、0.6mg/m2、0.6mg/m2)联合DA-EPOCH方案(第1-5天给药),前5名患者使用0.3mg/m2的InO,之后采用贝叶斯最优区间设计指导剂量爬坡,主要观察指标是InO的最大耐受剂量,同时观察其他指标,包括缓解率、生存期、毒性反应等,根据特定标准确定剂量限制性毒性,包括4-5级非血液学毒性、肝窦阻塞综合征、无法完成一个周期治疗、治疗延迟>3周等。
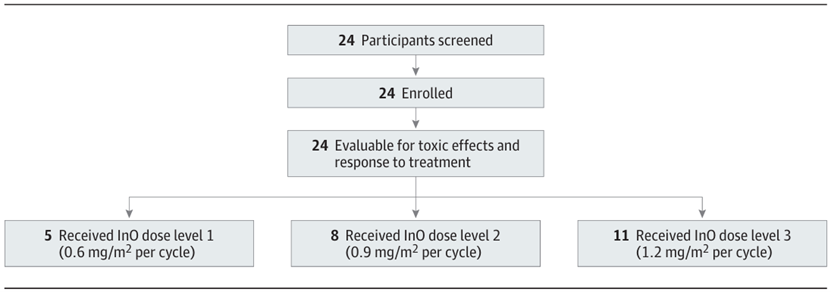
研究结果
InO的最大耐受剂量确定为0.6mg/m2,在11名患者中出现了3例剂量限制性毒性,包括1例低钠血症、1例延迟性全血细胞减少和1例肝窦阻塞综合征,整体毒性反应可控,无死亡病例,仅1例患者在移植后出现肝窦阻塞综合征,大部分肝功能异常为轻微且可逆,在19名基线有5%以上血或骨髓原始细胞的患者中,形态学完全缓解率为84%,MRD阴性率为88%,总体缓解率为83%,中位总生存期为17个月,中位缓解持续时间为15个月,中位无事件生存期为9.6个月,大多数患者接受后续巩固治疗,包括异基因造血干细胞移植、CAR-T疗法和博纳吐单抗,该组合疗法安全,毒性可控,整体疗效良好。
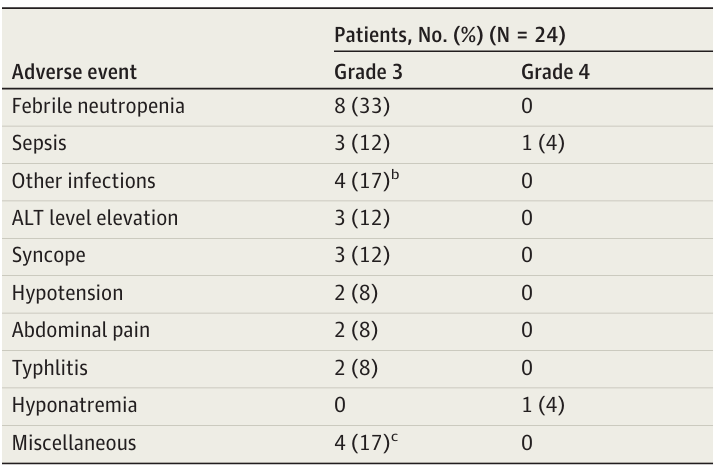
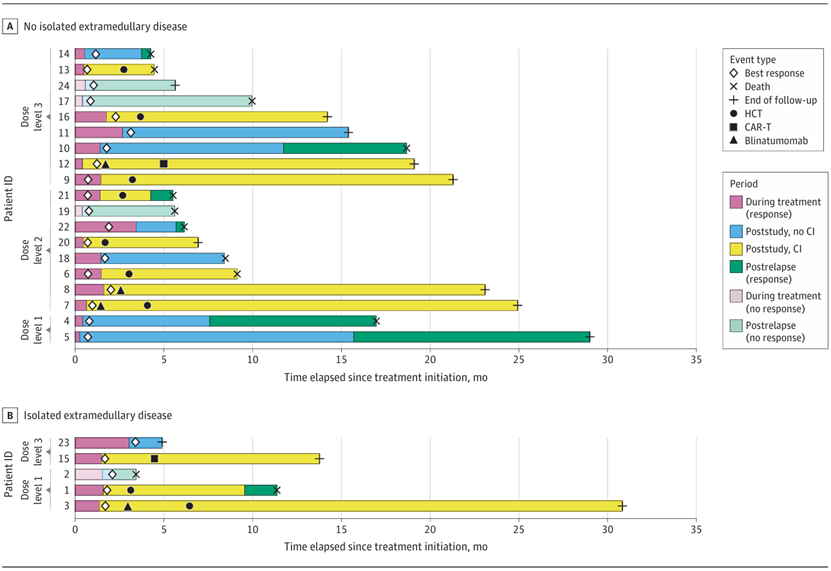
结论
DA-EPOCH联合InO疗法在成人B-ALL复发或难治患者中是可行的,显示出较高的缓解率,中位总生存期达到17个月,中位缓解持续时间为15个月且具有良好的安全性,毒性可控,整体疗效令人满意。该组合疗法是一种合理的治疗选择,易于在常规临床实践中应用,且无需在专科中心实施,鉴于该研究结果,值得进一步开展大规模的确认性临床试验,以验证该组合疗法的有效性和安全性,在等待大规模临床试验结果出炉之前,该组合疗法可以考虑在常规临床实践中作为B-ALL复发或难治患者的合理治疗选择。综上所述,该研究为B-ALL复发或难治患者提供了一种安全、有效且易于获取的治疗方案,值得进一步研究以确定其临床价值。
原始出处
Kopmar NE, Quach K, Gooley TA, Martino CH, Cherian S, Percival MM, Halpern AB, Ghiuzeli CM, Oehler VG, Abkowitz JL, Walter RB, Cassaday RD. Dose-Adjusted EPOCH Plus Inotuzumab Ozogamicin in Adults With Relapsed or Refractory B-Cell ALL: A Phase 1 Dose-Escalation Trial. JAMA Oncol. 2024 May 9:e240967. doi: 10.1001/jamaoncol.2024.0967. Epub ahead of print. PMID: 38722664; PMCID: PMC11082746.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#B-ALL# #奥英妥珠单抗# #DA-EPOCH#
10