Nature子刊:恶性周围神经鞘瘤最新分子亚群,及针对靶向药研发方向
2024-01-16 儿童肿瘤前沿 儿童肿瘤前沿 发表于陕西省
该研究对108种外周神经鞘瘤进行多平台综合分子分析,确定了两个MPNST 亚群,分别具有独特的可靶向致癌程序。
恶性外周神经鞘瘤(MPNST)是一种高侵袭性肉瘤,也是神经纤维瘤病1型(NF1)的相关恶性肿瘤,5年生存率低至20-50%。其标准治疗包括手术切除和辅助放疗,有效化疗很少,临床治疗效果进展有限。过去这一领域的研究集中在明确MPNST的转化驱动因素上,对MPNST的分子特征和亚型了解不足。
近日,加拿大多伦多大学神经外科系的 Gelareh Zadeh 教授在 Nature Communications 上发表题为 Multiplatform molecular profiling uncovers two subgroups of malignant peripheral nerve sheath tumors with distinct therapeutic vulnerabilities 的文章。该研究对108种外周神经鞘瘤进行多平台综合分子分析,确定了两个MPNST 亚群,分别具有独特的可靶向致癌程序。并在 MPNST的临床前模型中,证实了抑制亚群1中的 SHH 通路可阻止生长和恶性进展,为临床试验研究新疗法提供了临床前证据。

基于甲基组的特征分析确定了MPNST的两个不同亚群
研究人员首先对108种 PNSTs 的队列进行全基因组 DNA 甲基化模式分析,得到七个稳定而稳健的亚组(图1a)。高级别 MPNST形成两个不同的甲基组群(MPNSTG1,n = 8 和 MPNST-G2,n = 8)。MPNST-G1 患者的生存期明显差于 MPNST-G2(0.6 年 vs 1.4 年)。MPNST 存在两种截然不同的甲基化亚型,有可能成为 MPNST 的预后标志物。
在对 PNSTs 中 CpG 甲基化的程度研究时,观察到 MPNST-G1 和 MPNST-G2 的 DNA 甲基化程度总体降低(图 1c)。而MPNST-G1 肿瘤有更多的 CpG 岛甲基化(图 1)。启动子区域,MPNST-G1也 存在更多的甲基化 CpG 岛,和更多的相应基因转录沉默(图 1e、f)。通路分析发现SHH信号转导基因是 MPNST-G1中最显著富集的通路,而 MPNST-G2 中则没有(图 1g)。因此, MPNST-G1 肿瘤中,SHH 通路可能是通过表观遗传失调激活的。
研究发现甲基化亚群存在特定的染色体畸变。MPNST-G1表现出复杂的拷贝数改变(平均 17.5 条染色体受影响),基因不稳定。MPNST-G2 表现出较少的染色体改变(平均8.9 条染色体受影响)。MPNST-G1 的大多数样本中发现了 PTCH1 缺失(62.5%)和 SMO 增益(37.5%)。与 MPNST-G2 相比,MPNST-G1 中 SHH 通路基因的改变明显更高(75% vs 12.5%)。
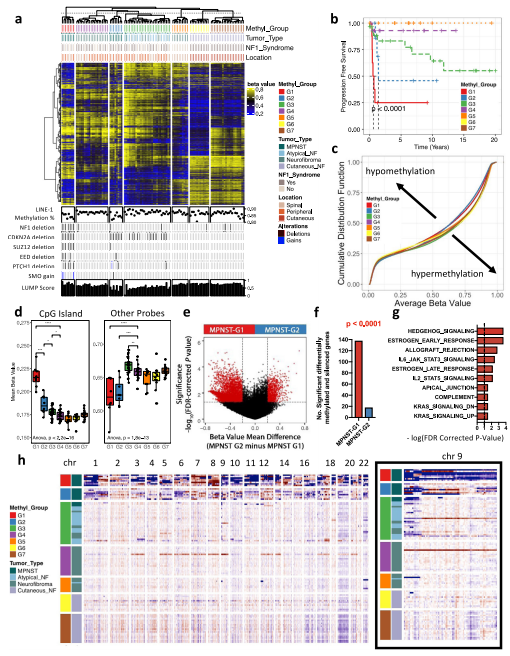
图 1. 基于甲基化和 CNV 的 PNST 分类
PRC2 成分的突变和非活化基因融合是 MPNST-G1 所特有
PNST 的突变谱检测发现,MPNSTs 的突变负荷显著高于良性和非典型神经纤维瘤。NF1 基因突变在 MPNST-G2 中的发生率明显更高,在 MPNST-G1 中观察到包含 NF1基因座的 17q 缺失率明显更高。PRC2 基因突变仅限于 MPNST-G1 肿瘤,在验证队列中证实了这一发现,进一步证明表观遗传失调在恶性肿瘤转化中的重要性。
检查所有 PNST 中基因融合的 RNA 序列数据,每个MPNST-G1样本中的融合事件明显增多。除了上述高拷贝数改变外,MPNSTG1 中基因融合的增加进一步证实该亚型的染色体不稳定性。
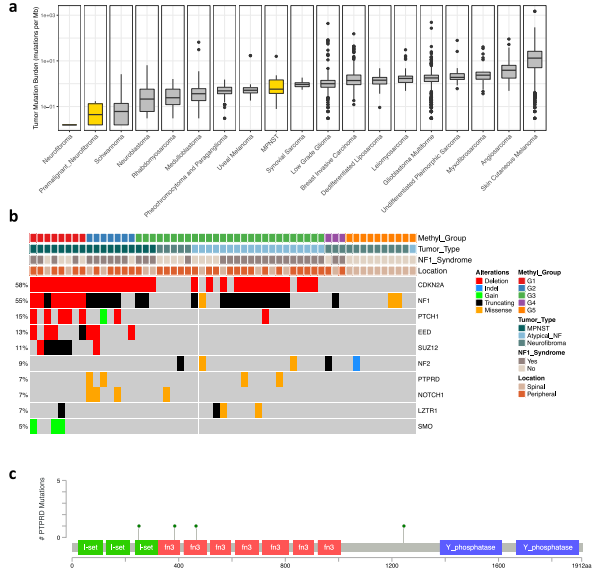
图2. PRC2突变是MPNST-G1所独有
转录谱分析发现两个 MPNST 亚群的激活通路分别为 SHH 通路和 WNT通路
分析基于甲基组的两个 MPNST亚群的转录谱观察到,MPNST-G1 富集了 PRC2 缺 失 模 块 和 SHH 通 路 激 活 , 而 MPNST-G2 则 富 集 了 WNT/ßcatenin/cyclinD1 通路激活(图 3d)。
MPNST-G1 中的肿瘤过度表达参与 SHH 信号转导的基因,如SMO、GLI2、GLI3、CCNE1 和 TGFB2(图 3e)。利用DrugBank数据库分析预测了可用于治疗的潜 在 药 物,发现平滑化抑制剂(vismodegib和sonidegib)是治疗MPNST-G1肿瘤的最有潜力的药物之一。
MPNST-G2 过表达了许多关键的 WNT 通路基因,包括 WNT10A、RAC2、AXIN1 和 FZD1(图 3f)。药物靶点分析发现,vorapaxar (一种PAR-1拮抗剂)有可能成为治疗MPNST-G2 的 候选药物。PAR-1 是 WNT 和 ß-catenin 通路的正向调节因子。
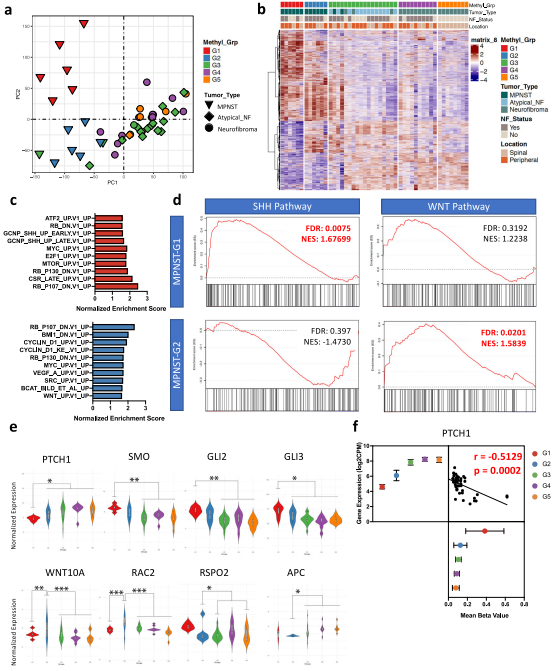
图 3. MPNST-G1 和 MPNST-G2 转录组特征不同。
单核 RNA 测序显示 MPNST-G1 中存在类似神经嵴细胞的特征
分析MPNST-G1 和 MPNSTG2 肿瘤细胞之间的差异,发现MPNST-G1 和 MPNST-G2 肿瘤细胞彼此不同。评估肿瘤细胞中许旺细胞系标志物的表达,发现神经纤维瘤与许旺细胞最为相似(图 4f),而大多数 MPNST 细胞失去了许旺细胞标记,向更原始的细胞状态分化。MPNST-G1 肿瘤细胞类似于神经嵴细胞,而MPNST-G2 肿瘤细胞更类似于许旺细胞前体细胞表型,缺乏许旺细胞标记。肿瘤细胞病理分析结果也显示,从非典型神经纤维瘤(许旺细胞)到MPNST-G2(许旺细胞前体细胞)再到MPNST-G1(神经嵴细 胞 )存在连续性,进一步证实这些肿瘤的神经嵴系发育轨迹。
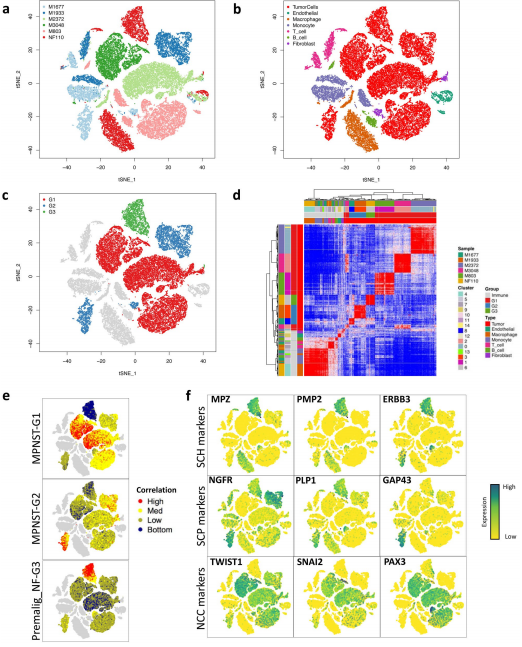
图 4. 单核 RNA 测序突显了进展外周神经鞘瘤复杂的肿瘤微环境和神经嵴谱系发育层次。
SHH 通路激活驱动MPNST恶性转化并提供有效的治疗靶点
甲基化、突变和转录组数据的积累都证明,有两个不同的 MPNST亚群是通过 SHH 和 WNT 这两条不同的途径形成的。在 MPNST-G1 中,多种生物学机制趋向于 SHH 通路在恶性进展中发挥核心作用。体外模型结果表明,敲除 PTCH1 会诱导SHH 通路的激活以及细胞增殖和迁移的显著增加(图 5)。体内模型结果表明,向免疫缺陷小鼠腹部注射 PTCH1 基因敲除细胞,75%的小鼠腹侧形成了肿瘤,而注射了未敲除PTCH1 基因的细胞的小鼠未形成肿瘤。这些结果验证了 SHH 通路可在体外和体内诱导恶性表型。
基因组数据确定 SHH 通路的上调是 MPNST-G1 肿瘤的驱动因素,而转录组网络分析确定 SMO 抑制剂是潜在的候选药物,因此假设sonidegib(SMO 抑制剂)可以为 SHH 通路激活的 MPNST 亚型提供治疗益处。体内模型和体外模型的实验结果均证实,抑制MPNST-G1中的SHH通路可以预防肿瘤生长和恶性进展(图5)。这些基因组/表观基因组的发现提供了临床前证据,支持在 MPNST-G1 亚群中使用 SMO 抑制剂进行临床试验。
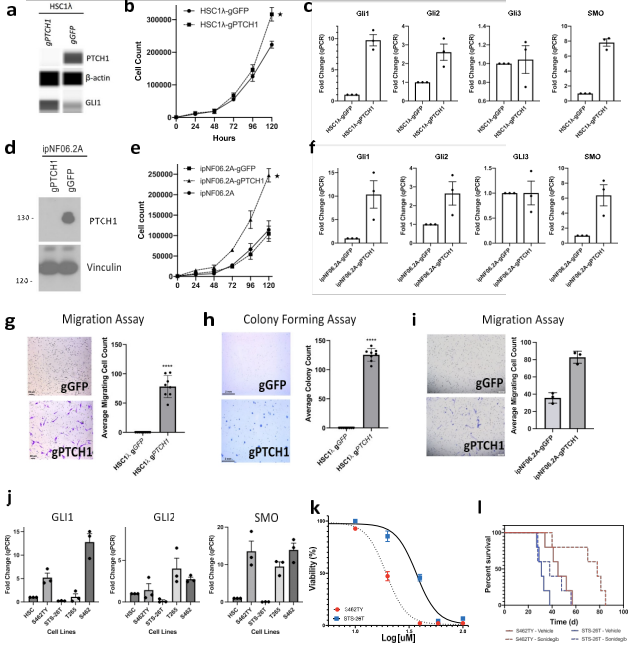
图 5. SHH 通路是 MPNSTs 亚群恶性转化的重要途径和治疗靶点。
本研究对两种MPNST亚型进行了全面的表征,为这一领域提供了宝贵信息。但是样本量较小(仅108例样本),两组之间的差异还需要在更大规模的研究中进行验证。此外,本研究没有深入探讨MPNST-G2全局低甲基化的机制。未来的研究可以针对性地检验更多样本,明确不同治疗方式对MPNST-G1和MPNST-G2的疗效,为开展临床试验提供依据。总之,本研究确立了MPNST分子分型的框架,为开发生物标志物和新的靶向疗法奠定了基础。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#靶向药# #恶性外周神经鞘瘤# #分子亚群#
27
认真学习了
0