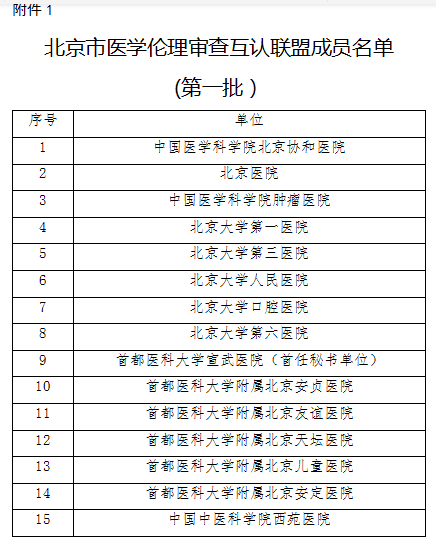
FDA授予Keytruda优先审查
协会还对该申请给予优先审查。该补充申请基于第3期KEYNOTE-189试验的总生存期(OS)和无进展生存期(PFS)数据。
MedSci原创 - Keytruda,FDA,优先审查 - 2018-05-02
GSK新任CEO审查其研发计划
制药公司葛兰素史克(GlaxoSmithKline)表示,为提高效率,将暂停30个临床和临床前项目,以审查其研究和开发渠道。总部位于伦敦的葛兰素史克公司表示,它还将对其罕见疾病部门进行战略审查,并"正在考虑未来对这些资产的所有权"。
MedSci原创 - GSK,研发计划 - 2017-07-26
欧盟审查MSD的Keytruda / chemo组合
欧洲的监管机构已经开始对MSD的Keytruda/pemetrexed组合进行审查,以治疗转移性非小细胞肺癌(NSCLC)患者的一线治疗。
MedSci原创 - Keytruda,/,chemo组合 - 2018-04-24
对Shire的HAE药物进行优先审查
美国监管机构正在对Shire的lanadelumab(SHP643)进行快速评估,该药用于预防12岁及以上患有遗传性血管性水肿(HAE)的患者发生血管性水肿。HAE是一种罕见的遗传疾病,会导致身体虚弱,疼痛,有时会危及生命。Shire对lanadelumab的申请得到了四项临床试验数据的支持,lanadelumab是一种特异性结合和抑制血浆激肽释放酶的研究性完全人单克隆抗体。来自关键III期HEL
MedSci原创 - Shire,HAE - 2018-02-23
美国优先审查Sanofi,Regeneron的cemiplimab。
美国监管机构正在对Sanofi和的cemiplimab进行优先审查,以治疗转移性皮肤鳞状细胞癌(CSCC)的患者,或者是那些不能手术的局部晚期CSCC患者。
MedSci原创 - cemiplimab,优先审查 - 2018-04-30
FDA审查沙格列汀心衰风险
;2月11日,美国食品与药物管理局(FDA)宣布称正在要求沙格列汀(saxagliptin)的厂商提交相关临床数据,以审查2型糖尿病患者应用该药治疗的可能心力衰竭风险。FDA相关人士希望在3月底能收到该药所有的临床数据并尽快完成审查将其结果公诸于众。
医学论坛网 - 沙格列汀,心衰风险,FDA - 2014-02-13
人体“基因剪刀”抗癌试验首次通过审查
该委员会负责对在美国进行的基因疗法临床试验进行安全及伦理审查。这项试验还需美国食品和药物管
新华社新华网 - 基因剪刀,CRISPR,基因编辑 - 2016-06-24
了解专利的官方审查流程
(一)发明专利的官方审查包括五阶段:受理阶段、初审阶段、公布阶段、实审阶段、授权阶段;1、发明专利的受理阶段时间:大约1个月左右;申请人获得专利受理通知书;如果通过电子提交方式申请专利,一般提交日的第二天即可获得申请日和申请号
MedSci原创 - 专利,审查流程 - 2015-04-22
Shire的lanadelumab获欧盟快速审查
欧洲监管机构将对Shire的遗传性血管瘤药物lanadelumab进行加速评估。该公司正在开发lanadelumab用于预防12岁及以上病症的患者发生血管性水肿。HAE是一种罕见的遗传性疾病,会导致身体虚弱,疼痛甚至威胁生命的肿胀,全球患病率约为1/10,p000到1/50,000。Lanadelumab是一种研究性完全人源单克隆抗体,其特异性结合并抑制血浆激肽释放酶,因此可能提供新的治疗方法。该
MedSci原创 - lanadelumab,欧盟快速审查 - 2018-03-01
FDA审查诺华新型血液肿瘤药物
FDA肿瘤药物咨询委员会在11月06日召开了会议并提前发布了文件,该机构官员没有给出多少评论,而是注重诺华公司768例3期临床试验的相关数据。在疗效方面,使用由诺华的帕比司他,武田的万珂和类固醇地塞米松组合的复方药物相对单独使用帕比司他能够延长无进展生存期(PFS)3.9个月,帮助患者延长近半年的寿命且没有严重症状。 诺华公司相信,其新的肿瘤治疗药物对于有严重多发性骨髓瘤和血癌的患者会有强烈
cphi - 血液肿瘤,药物 - 2014-11-11
Nature:科研资金申请审查中的隐性歧视
美国国立卫生研究院(NIH)科学审查中心负责人Richard Nakamura从未想过,自己在工作时潜意识地具有种族主义倾向。
生物360 - 科研资金申请,审查,隐性歧视 - 2014-08-25
美要求联邦实验室进行安全审查
白宫希望联邦政府资助的实验室加强生物安全审查。图片来源:GREG KNOBLOCH 在经历了几起今年早些时候发生的颇受关注的实验室事故后,美国白宫要求由联邦政府资助的实验室“立刻采取行动”——列出详细的样品清单,审查安全程序。
中国科学报 - 实验室,安全审查 - 2014-09-02
为您找到相关结果约500个