FDA批准首个夜间尿频治疗药物Noctiva
3月3日,FDA宣布批准Noctiva(醋酸去氨加压素)鼻腔喷雾用于治疗夜间多尿导致至少起夜2次的成人尿频患者。这是FDA批准的第一个治疗夜间尿频的药物。
医药魔方数据 - 夜间尿频,药物,治疗 - 2017-03-05
FDA批准遗传性肥胖药物Imcivree
FDA已批准Imcivree(setmelanotide)用于前阿片黑素细胞皮质激素(POMC)或瘦素受体(LEPR)遗传缺陷的肥胖人群的慢性体重管理。
MedSci原创 - 遗传性肥胖,Imcivree,瘦素受体(LEPR),前阿片黑素细胞皮质激素(POMC) - 2020-11-28
Vivus公司ED药物Avanafil获EMA批准
2012年3月26日,Vivus公司(Nasdaq:VVUS)今天宣布,欧洲药品管理局(EMA)已批准其研究性药物avanafi上市许可申请(Marketing Authorization ApplicationEMA对avanafi的批准,是基于VIVUS公司成功完成的一项广泛III期研究
生物谷 - 新药,FDA - 2012-04-16
吉利德HIV药物Vitekta获欧盟批准
吉利德(Gilead)11月18日宣布,整合酶抑制剂Vitekta(elvitegravir,85mg和100mg)已获欧盟委员会(EC)批准,用于无任何已知elvitegravir抗性相关突变的HIV
生物谷 - 新药,FDA - 2013-11-20
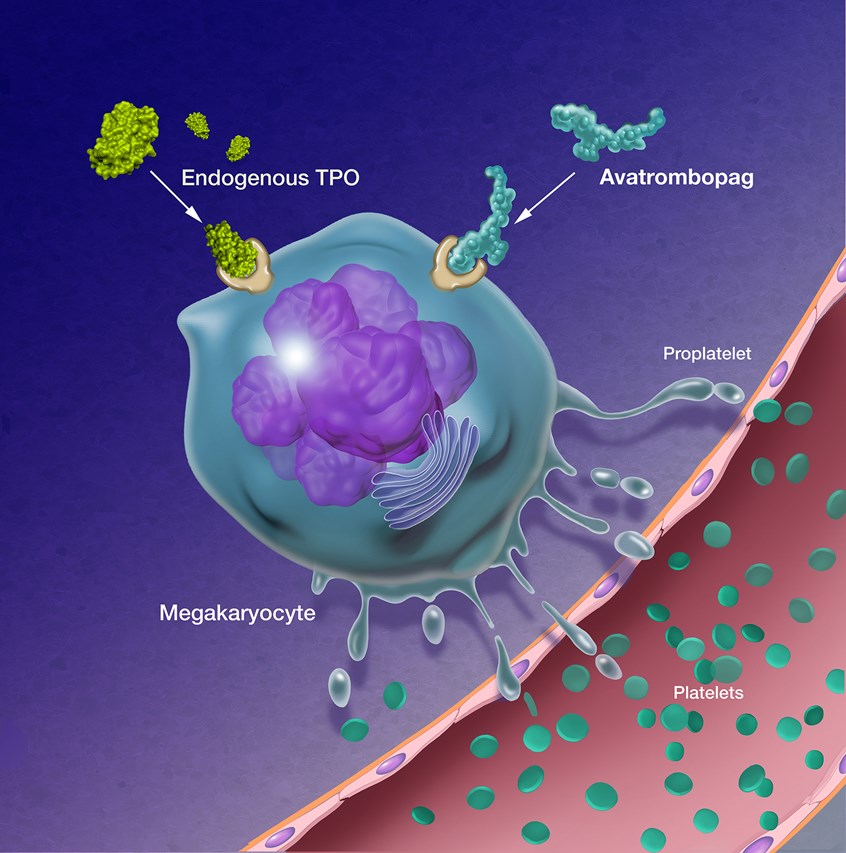
欧盟批准血小板减少症药物Doptelet
Doptelet通过模拟血小板生成素刺激巨核细胞发育和成熟,增加血小板数量。
MedSci原创 - 血小板减少症,血小板生成素受体激动剂,Doptelet(avatrombopag) - 2020-11-06
FDA批准首个治疗罕见皮肤癌药物
今日(3月24日),美国FDA宣布,加速批准由德国默克公司与辉瑞共同研发的PD-L1抗体Bavencio(Avelumab)上市,用于治疗罹患转移性默克尔细胞癌(metastatic Merkel cellcarcinoma,MCC)的成人与12岁以上儿童,包括那些先前未经化疗治疗的患者,Avelumab是FDA批准的首个治疗这一疾病的疗法,同时也是第二个获得美国FDA批准的PD-L1抗体药物。
医谷 - 皮肤癌 - 2017-03-24
强生淋巴瘤药物Imbruvia获FDA批准
强生(JNJ)和Pharmacyclics 11月13日宣布,FDA已批准血癌药物ibrutinib(拟用商品名为Imbruvica),用于既往已接受至少一种其他药物(如Celgene公司的Revlimid该药成为获得FDA突破疗法认定并获批的第2个药物,ibrutinib将成为上市的首个BTK靶向药物。
生物谷 - 新药,FDA - 2013-11-14
2014年FDA新批准的抗肿瘤药物
2014年,美国FDA药品评价和研究中心批准了41个新分子实体和生物制品许可申请。为过去18年之最。2014年美国FDA批准的41个新药中抗感染类药物有10个,而抗肿瘤领域也不示弱,仍达到了9个新药,而且获得美
新康界 - FDA,抗肿瘤药物 - 2015-02-10
2023上半年FDA批准肿瘤药物分析
2023上半年,FDA共批准了26款新分子实体药物,其中针对肿瘤的共有6款(包括诊断试剂flotufolastat F 18,表1),占据了23%的份额。
精准药物 - FDA,肿瘤药物 - 2023-07-08
FDA:首个脂肪肉瘤治疗药物Halaven批准上市
FDA批准Halaven治疗无法手术切除或转移性脂肪肉瘤。Halaven是第一个批准用于脂肪肉瘤治疗的药物,可改善改善患者的生存,可增加整体约7个月的生存期。通过对143名无法手术切除或转移性脂肪肉瘤的研究发现, Halaven治疗的患者整体生存期达15.6个月,其他化疗药物达卡巴嗪治疗的患者整体生
MedSci原创 - Halaven,软组织,肉瘤 - 2016-02-01
FDA委员会建议批准Chelsea药物Northera
Chelsea制药1月15日宣布,FDA心血管和肾脏药物顾问委员会(CRDAC)以16比1的投票结果,建议批准该公司的药物Northera(droxidopa,屈昔多巴),用于原发性自主神经衰弱(帕金森病
生物谷 - 新药,FDA - 2014-01-16
FDA批准减轻水痘症状药物Varizig上市
近日,美国食品与药物管理局(FDA)通过优先审查批准了“孤儿药”Varizig用于降低4天内接触水痘带状疱疹病毒而发生严重感染风险的高危患者。
医学论坛网 - 水痘,带状疱疹病毒,Varizig - 2012-12-25
GSK皮肤癌药物Mekinist获欧盟批准
葛兰素史克(GSK)的Mekinist近日赢得了欧洲药品管理局(EMA)的批准用于黑色素瘤的治疗,成为第一种在在欧洲批准授权的MEK抑制剂类药物。Mekinist(trametinib)已在欧盟批准作为单一治疗药物用于携带BRAFV600突变的不可切除或转移性黑色素瘤成人患者。这次批准通过对于葛兰素史克公司和诺华公司都是一个好消息,诺华曾与GSK达成了一项协议,以160亿美元从GSK收购M
不详 - 皮肤癌,药物 - 2014-07-14
为您找到相关结果约500个