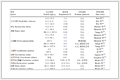
心血管治疗类医疗器械非劣效性试验特点及界值设置的系统评价
在迫切的临床需求下,心血管疾病领域的创新医疗器械发展迅速,在疾病的诊断、治疗以及康复随访等各个阶段均发挥了重要作用[2]。其中,经皮冠
中国循证医学杂志 - 心血管,非劣效性试验,界值标准 - 2024-03-17
国家药监局综合司公开征求《医疗器械临床试验检查要点及判定原则(征求意见稿)》意见
指导药品监督管理部门规范开展医疗器械临床试验监督检查工作,国家药监局组织制定了《医疗器械临床试验检查要点及判定原则(征求意见稿)》,现公开征求意见。
国家药品监督管理局 - 医疗器械临床试验 - 2023-11-29
工信部发布《医疗装备产业发展规划(2021— 2025年)》:2025年6-8家企业进入全球医疗器械行业50强
近日,工信部就《医疗装备产业发展规划(2021— 2025年)》(征求意见稿)公开征求意见,提出到2025年,关键零部件及材料取得重大突破,高端医疗装备安全可靠,产品性能和质量达到国际水平
医谷网 - 医疗装备,50强,协同联动 - 2021-03-07
直击新医改与监管新政下的中国医疗器械创新征途
2017年9月1日至3日,由苏州生物医药产业园(BioBAY)牵手中国医疗器械行业协会主办的第七届中国医疗器械高峰论坛(DeviceChina 2017)在苏州独墅湖畔拉开帷幕,直击新医改与监管新政下的中国医疗器械创新征途
生物探索 - 医疗器械,高端,高峰论坛 - 2017-09-02
国家药监局综合司公开征求《医疗器械网络销售质量管理规范(征求意见稿)》意见
为贯彻落实《中华人民共和国电子商务法》《医疗器械监督管理条例》《医疗器械网络销售监督管理办法》,国家药监局组织起草了《医疗器械网络销售质量管理规范(征求意见稿)》,现向社会公开征求意见。
国家药品监督管理局 - 医疗器械网络销售 - 2023-09-19
CFDA拟调整三类体外诊断试剂分类:730项归属三类,287项不属医疗器械
昨日(9月21日),食药监总局发布《关于征求过敏原等三类体外诊断试剂分类调整意见的函》(食药监械管便函〔2016〕63号),就过敏原类、流式细胞仪配套用和免疫组化类体外诊断试剂产品的分类调整意见公开征求意见,意见反馈截止时间为2016年10月31日,具体分类如下: 一、过敏原类体外诊断试剂 与变态反应(过敏原)相关的试剂,包括总IgE检测试剂、特异性IgE抗体检测试
CFDA - 体外诊断 - 2016-09-23
行业标准《人工智能医疗器械 质量要求和评价 第2部分:数据集通用要求》解析
本文对该部分标准的制订背景及要点内容进行解析,以期更好地指导行业应用。
协和医学杂志 - 医疗器械,人工智能 - 2023-12-02
国家药监局关于批准注册180个医疗器械产品的公告(2023年4月)(2023年第65号)
2023年4月,国家药监局共批准注册医疗器械产品180个。其中,境内第三类医疗器械产品125个,进口第三类医疗器械产品21个,进口第二类医疗器械产品33个,港澳台医疗器械产品1个(具体产品见附件)。
国家药品监督管理局官网 - 医疗器械 - 2023-06-02
医疗器械动物试验研究注册审查指导原则第二部分:试验设计、实施质量保证
本文为国家药品监督管理局医疗器械技术审评中心发布的《医疗器械动物试验研究注册审查指导原则第二部分:试验设计、实施质量保证》。
国家药品监督管理局医疗器械技术审评中心 - 动物试验 - 2024-04-23
医疗器械(含体外诊断试剂)监管信息基础数据元值域代码(注册和备案部分)(征求意见稿)
医疗器械(含体外诊断试剂)监管信息基础数据元值域代码(注册和备案部分)(征求意见稿)
CDE - 医疗器械,基础数据 - 2022-08-09
已获进口医疗器械注册证的产品转移中国境内企业生产有关事项公告(征求意见稿)
已获进口医疗器械注册证的产品转移中国境内企业生产有关事项公告(征求意见稿)
NMPA - 进口医疗器械 - 2022-08-09
以医疗器械作用为主的药械组合产品中药物定性定量及体外释放研究注册审查指导原则
为加强对药械组合产品注册工作的监督和指导,进一步鼓励具有临床价值的药械组合产品上市,构建适合我国国情的药械组合产品的管理模式,国家药品监督管理局将药械组合产品技术评价作为监管科学研究项目,组织制定了《
CDE - 医疗器械 - 2022-01-24
为您找到相关结果约500个