FDA授予切昆贡亚热疫苗快速通道资格
近日,PaxVax宣布,其在研疫苗已经收到美国食品和药物管理局(FDA)的快速通道资格认定(快速通道计划旨在促进并加速药物及疫苗的审查,以解决未满足的健康需求),用于预防由切昆贡亚热病毒引起的疾病。
MedSci原创 - 切昆贡亚热,疫苗,快速通道 - 2018-05-11
FDA:机器人已经可以给人做手术了
来自卡耐基梅隆大学的公司Medrobotics Corp.于2015年7月下旬发表声明,称其公司生产的Flex®机器人系统已经得到美国食品及药物管理局(FDA)的放行,可以在市场上销售了。
环球科学 - 机器人,手术 - 2015-08-10
FDA批准默沙东单抗新药,降低耐药菌复发风险
而近日,它的一款新药ZINPLAVA(bezlotoxumab)也获得了FDA的批准,用于降低艰难梭菌(Clostridium difficile)的复发风险。
生物谷 - 单抗新药 - 2016-11-01
Midatech收到FDA对MTD201临床计划的反馈
Midatech是一家专注于为患者提供创新的肿瘤学和罕见疾病产品的研发公司,近日宣布它已于2018年12月20日收到FDA对其主要产品MTD201(Q-奥曲肽)的临床研究的反馈意见。
MedSci原创 - MTD201,FDA,奥曲肽 - 2019-01-29
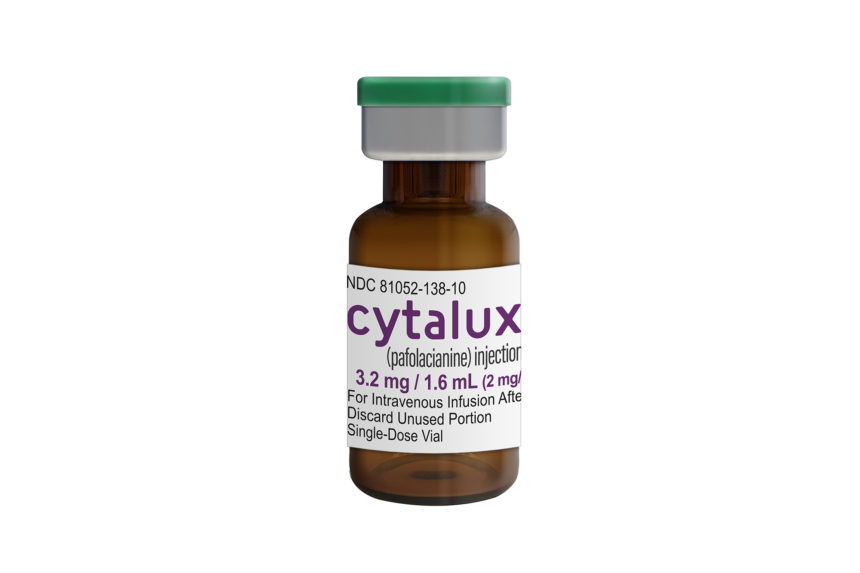
FDA批准Pafolacianine作为肺癌的术中分子成像剂
Pafolacianine(帕福拉西宁)是一种叶酸类似物/吲哚菁绿样结合物,靶向卵巢癌细胞显著表达的叶酸受体 (FR),是第一种经临床证实的靶向荧光成像剂,能在术中照亮卵巢肿瘤,为手术切除提供更准确的
MedSci原创 - 肺癌,Pafolacianine - 2022-12-20
FDA批准DANYELZA(naxitamab-gqgk)治疗神经母细胞瘤
DANYELZA(naxitamab-gqgk)与粒细胞巨噬细胞集落刺激因子(GM-CSF)联用用于治疗1岁及以上的骨复发或难治性高危神经母细胞瘤患者。
MedSci原创 - FDA,神经母细胞瘤,DANYELZA(naxitamab-gqgk) - 2020-11-26
FDA批准PaxVax公司口服单剂量霍乱疫苗研发申请
近日,PaxVax公司口服单剂量霍乱疫苗研发新药申请(IND)获得美国食品药监局(FDA)批准。PXVX-0200是一种对抗霍乱的活性疫苗,先前曾以商品名为Orochol在其他六个国家获得批准。
cyy123 - 新药,FDA - 2012-04-25
EpiCept神经痛药物AmiKet获FDA快速审定资格
近日,EpiCept公司的AmiKet获得美国食品药监局(FDA)授予的快速审定资格,这是一种含有4%的阿米替林和2%的氯胺酮的药物。根据FDA的规定,获得快速审定资格的药物会获得有限审定权,比标准的审定时间要缩短大概一半。 EpiCept公司总裁兼首席执行官Jack Talley说:“我们希望通过这次
cyy123 - 新药,FDA - 2012-04-25
美FDA新掌门人:要对移动健康应用大松绑
6月15日,FDA官网称即将实施一项计划,进一步明晰健康应用的监管层次,并且针对如何使用“上市”后数据对健康应用进行监管给出了一系列建议。
健康点 - FDA,健康应用 - 2017-06-19
FDA批准胆管癌FGFR靶向药pemigatinib获批
2020年4月18日,FDA肿瘤卓越中心主任Richard Pazdur宣布Pemazyre(pemigatinib)获批上市,该药对携带FGFR2基因融合或其他重排类型的晚期经治胆管癌患者具有良好的
燃石医学 - 胆管癌,pemigatinib,FGFR靶向药 - 2020-04-20
诺华治疗肢端肥大症长效药物获得FDA批准
美国FDA最近批准了诺华公司开发的用于治疗罕见疾病肢端肥大症的生长激素类药物Signifor登陆美国市场。这一药物也是继Sandostatin后,诺华公司在该领域开发的另一种主打产品。
生物谷 - 诺华,基因治疗 - 2014-12-18
FDA批准吡格列酮的首个仿制药上市
美国食品药品管理局(FDA)8月17日宣布,已批准2型糖尿病口服治疗药物吡格列酮的首个仿制药上市。
网络 - FDA,吡格列酮,仿制药,2型糖尿病 - 2012-08-21
为您找到相关结果约500个