单臂临床试验用于支持抗肿瘤药上市申请的适用性技术指导原则
在国家药品监督管理局的部署下,药审中心组织制定了《单臂临床试验用于支持抗肿瘤药上市申请的适用性技术指导原则》。
国家药品监督管理局官网 - 抗肿瘤药,单臂临床试验 - 2023-06-04
单臂临床试验设计用于支持抗肿瘤药上市申请的适用性技术指导原则
为阐明当前对单臂临床试验用于支持抗肿瘤药上市申请的适用性的科学认识,指导企业在完成早期研究后,更好地评估是否适合开展单臂临床试验作为关键临床研究,以支持后续的上市申请,在国家药品监督管理局的部署下,药
国家药品监督管理局药品审评中心 - 抗肿瘤药,单臂临床试验 - 2023-03-19
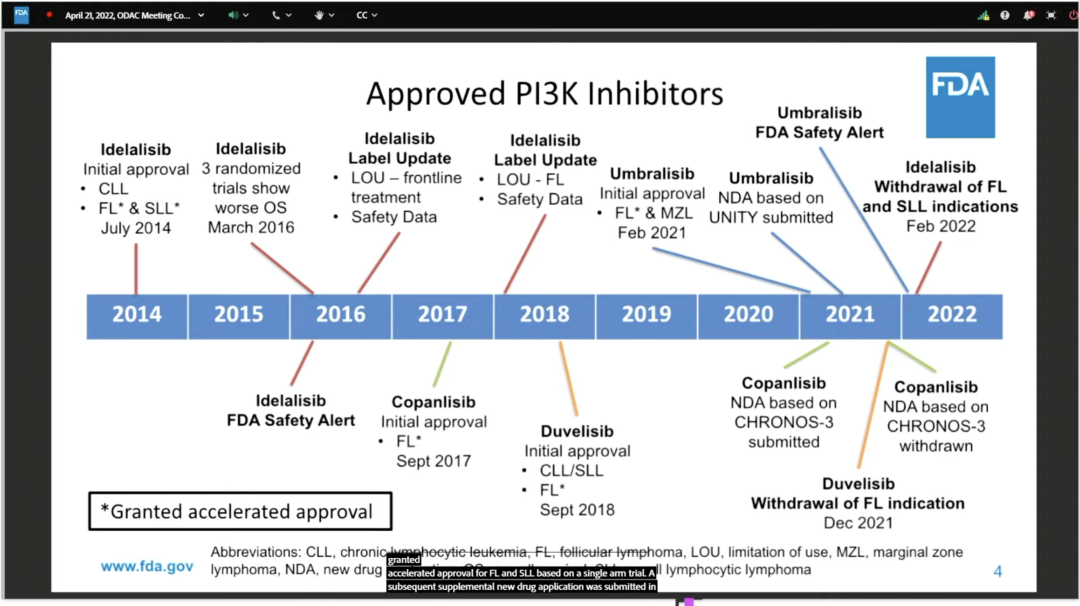
FDA 关闭 PI3K 抑制剂单臂试验的大门,会给中国新药研发带来哪些启示?
PI3K抑制剂可调节多个细胞过程,包括细胞生长、增值、分化和新陈代谢等。血癌中可见其信号通路的激活——失调的PI3K信号传导促进了恶性淋巴细胞的存活和增殖。目前,PI3K抑制剂
MedSci原创 - PI3K 抑制剂 - 2022-04-29
关于公开征求《单臂临床试验用于支持抗肿瘤药上市申请的适用性技术指导原则》意见的通知
单臂临床试验的研发策略显著地缩短了新药的上市时间;特别是近年来,许多新药在临床研究早期阶段就显现出非常突出的有效性数据,因此,越来越多的研发企业希望采用单臂临床试验支持抗肿瘤药物的上市申请。但与公认的
国家药品监督管理局药品审评中心 - 单臂临床试验 - 2022-06-23
(单臂Ⅱ期临床试验)
背景:临床前数据表明了表皮生长因子受体(epithelial growth factor receptor,EGFR)对皮肤鳞状细胞癌(cutaneous squamous cell carcinomas,CSCC)的发病起着关键性作用。EGFR本身具有酪氨酸激酶活性,一旦与表皮生长因子(EGF)组合可启动细胞核内的有关基因,从而促进细胞分裂增殖。胃癌、乳腺癌、膀胱癌和头颈部鳞癌的EGFR表达增高
MedSci原创 - 吉非替尼,皮肤鳞状细胞癌 - 2017-10-31
测血压只看单臂高、低压?千万别忽略这3个指标!
高血压是心脑血管疾病的重要危险因素,与心脑血管事件、靶器官损害密切相关。因此,血压达标并维持达标在日常生活中显得至关重要。
MedSci原创 - 高血压,测血压 - 2022-10-12
NAT COMMUN:达尔西利(Dalpiciclib)联合吡咯替尼(pyrotinib)治疗HER2阳性晚期乳腺癌的单臂II期临床试验
该研究旨在评估HER2阳性ABC患者中(无论HR状态如何)达尔西利联合吡咯替尼的疗效和安全性,该组合在HER2阳性ABC中具有抗肿瘤活性和可控的毒性。
MedSci原创 - 乳腺癌,吡咯替尼,达尔西利 - 2023-10-09
Lancet Rheumatolgoy:阿巴西普治疗 IgG4 相关疾病:一项前瞻性、开放标签、单臂、单中心、概念验证研究
IgG4相关疾病患者对选择性T细胞共刺激调节剂阿巴西普有不同的治疗反应。
MedSci原创 - IgG4相关性疾病,阿巴西普 - 2022-04-11
单臂试验支持上市的抗肿瘤药进入关键试验前临床方面沟通交流技术指导原则
为切实鼓励创新,保障抗肿瘤创新药以充分科学依据开展关键单臂试验,帮助申请人提高研发效率并更高效地沟通,在国家药品监督管理局的部署下,药审中心组织制定了《单臂试验支持上市的抗肿瘤创新药进入关键试验前临床
CDE - 单臂试验 - 2020-12-07
单臂试验支持注册的抗肿瘤创新药申请上市前临床方面沟通交流技术指导原则
根据药品注册管理办法(国家市场监督管理总局令第27号)第十六条,申请人在药品上市许可申请前等关键阶段,可以就重大问题与药品审评中心等专业技术机构进行沟通交流。
CDE - 指导原则 - 2020-10-03
单臂试验支持上市的抗肿瘤药上市许可申请前临床方面沟通交流技术指导原则(2020年)
为鼓励创新,帮助申请人提高与药审中心的沟通交流效率,保证药品审评的科学性和严谨性,在国家药品监督管理局的部署下,药审中心组织制定了《单臂试验支持上市的抗肿瘤药上市许可申请前临床方面沟通交流
NMPA - 单臂试验 - 2021-02-09
非比较研究及前后对照研究(单臂研究)结局变量Meta分析的效应量选择
关于成组设计类型比较研究的Meta分析或系统评价理论与方法学日趋成熟,但对单变量关系,又称非比较性研究或单组研究结局变量以及两变量关系研究,比如 前后比较研究变量进行综合分析的文献与方法则相对较少。目的:探讨针对单变量关系研究集中趋势描述的常用统计量比例或率及均数以及两变量关系研究中前后比 较研究的常用统计量均数得分法的Meta分析法。方法:应用计算机检索中文CNKI全文数据库、维普全文数据库
MedSci原创 - 单臂,Meta - 2013-11-30
多臂随机对照平行临床试验报告规范:CONSORT规范扩展
重要性:随机临床试验的报告质量欠佳。在当今时代,需要更高的研究透明度至关重要,报告不足会阻碍对试验结果的可靠性和有效性的评估。制定《 2010年合并试验标准报告》(CONSORT)的目的是改善随机临床
JAMA . 2019 Apr 23;321(16):1610-1620. doi: 10.1001/jama.2019.3087. - CONSORT规范,报告规范 - 2020-09-24
为您找到相关结果约500个