Nature/NCB:复旦大学多单位合作,鲁青团队揭示YAP融合诱导肿瘤的靶向治疗脆弱性,驱动室管膜瘤的发生的重要机制
2023-02-04 iNature iNature 发表于上海
突变和嵌合体分析表明,一个内在无序的区域促进YAP融合成核的、点状的、无膜的凝聚物的寡聚。YAP与转录激活因子GCN4的卷曲结构域融合诱导的寡聚和核凝聚也促进室管膜瘤的形成。
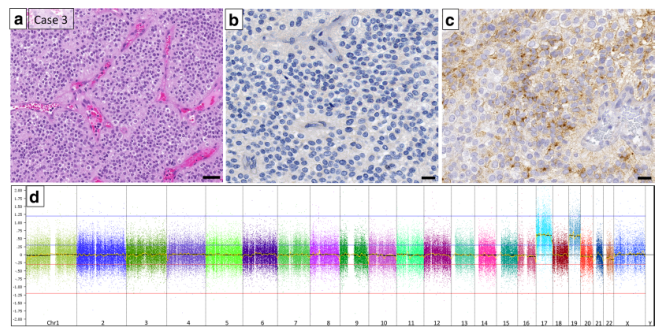
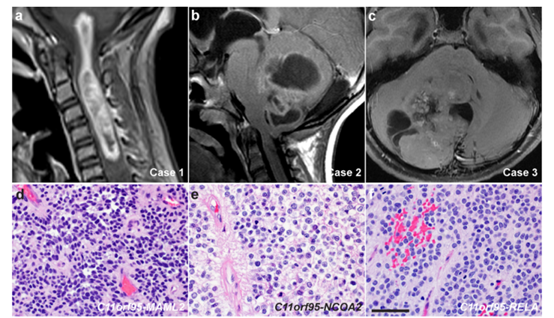
室管膜瘤(Ependymoma, EPN)是第三常见的儿科脑肿瘤。这些肿瘤发生在贯穿中枢神经系统的心室排列的室管膜层。尽管采用了多模式治疗,但EPN患者仍会出现身体残疾和神经发育障碍等慢性后遗症,大多数患者的肿瘤复发导致死亡。EPN起源于神经干/祖细胞(neural stem/progenitor cells, NSCs)。起源于中枢神经系统不同区域的EPN在组织学上相似,但表现出不同的分子特征和预后,并被分为至少9个不同的亚型。幕上半球室管膜瘤(Supratentorial hemispheric ependymomas, ST-EPNs)主要位于第三或第四脑室内或毗邻,该亚型占所有EPN的30%,与大量死亡率相关。ST-EPN起始的机制尚不完全清楚。HIPPO-YAP/TAZ (WWTR1)通路已成为器官生长和肿瘤发生的核心参与者。HIPPO-YAP融合蛋白的核定位与幕上室管膜瘤的发生有关。
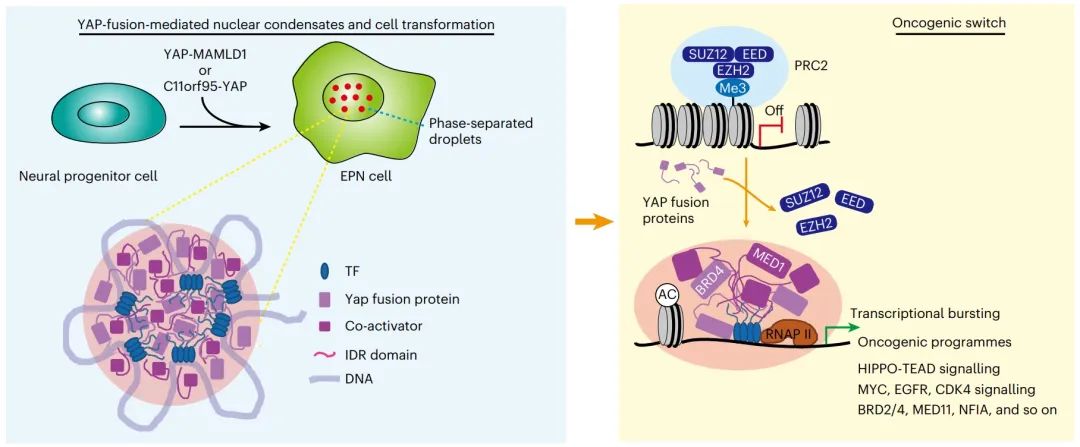
2023年2月2日,辛辛那提儿童医院医疗中心,复旦大学等多单位合作,鲁青(Q. Richard Lu)团队在Nature Cell Biology 杂志在线发表题为“Nuclear condensates of YAP fusion proteins alter transcription to drive ependymoma tumourigenesis”的研究论文,该研究发现复发患者来源的YAP融合,YAP-MAMLD1和C11ORF95-YAP的液-液相分离,而不是核定位,是神经祖细胞室管膜瘤发生的基础。突变和嵌合体分析表明,一个内在无序的区域促进YAP融合成核的、点状的、无膜的凝聚物的寡聚。YAP与转录激活因子GCN4的卷曲结构域融合诱导的寡聚和核凝聚也促进室管膜瘤的形成。
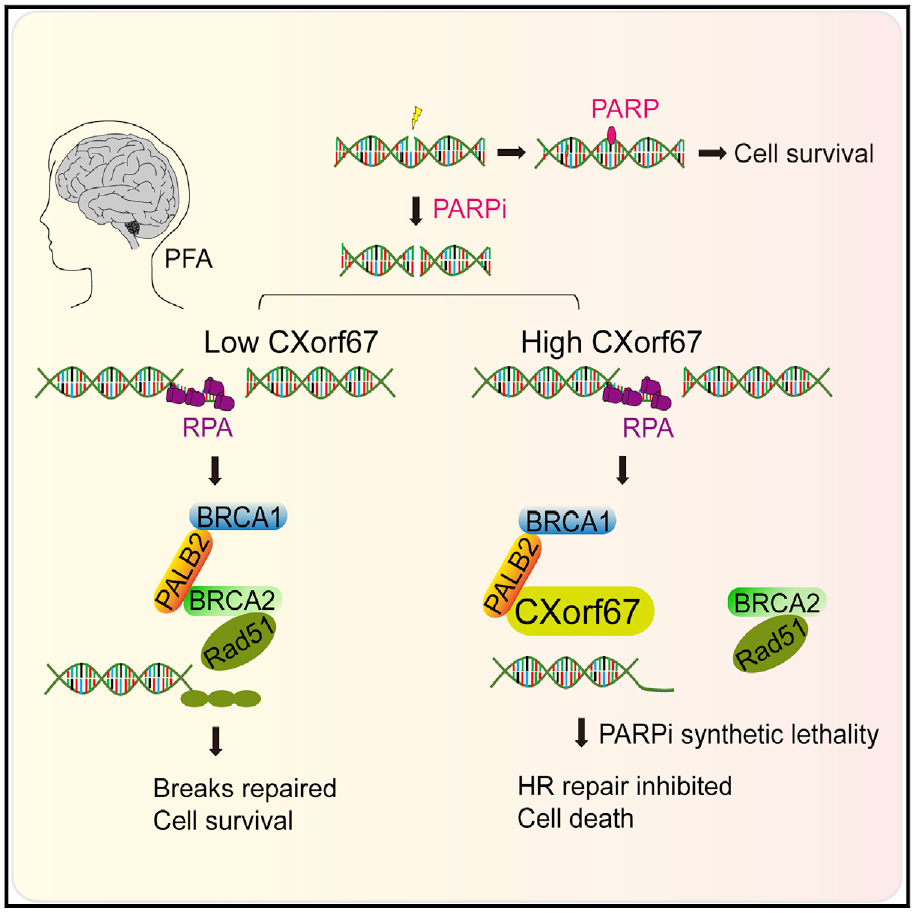
YAP-MAMLD1将转录因子和共激活因子(包括BRD4、MED1和TEAD)浓缩在凝析液中,同时排除转录抑制PRC2,并诱导远程增强子-启动子相互作用,促进转录和致癌程序。阻断凝结物介导的转录共激活因子活性抑制肿瘤发生,表明液相分离对室管膜瘤YAP融合致癌活性起关键作用。包含内在紊乱区域特征的YAP融合在人类肿瘤中很常见,这表明核凝聚物可以靶向治疗YAP融合诱导的癌症。总之,这项工作进一步揭示了YAP融合诱导肿瘤的靶向治疗脆弱性。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言