Metabolism 武汉大学鲁志兵/刘实教授团队揭示病毒性心肌损伤的新机制
2024-03-11 论道心血管 论道心血管 发表于上海
该研究揭示了糖代谢信号网络与IL-6介导的炎症反应之间的交互调控,并系统阐明了其在病毒性心肌损伤中的作用,从免疫代谢的角度深入剖析了IL-6对病毒性心肌炎的调控功能和分子机理。
病毒性心肌炎是指病毒感染所引起的心肌局限性或弥漫性炎症反应和心肌细胞损伤,重症可出现心源性休克和猝死。目前,对于病毒性心肌炎的发病机制了解有限,缺乏特异性治疗手段。既往研究报道,白细胞介素6 (IL-6)介导的炎症反应在病毒性心肌炎的发生发展中至关重要。
近年来,人们逐渐认识到,炎症反应和能量代谢密切相关。糖代谢作为细胞内能量代谢的最主要方式,其与IL-6信号通路之间的关系尚不清楚,其对病毒性心肌炎的调控作用和分子机制也未见报道。
2024年3月2日,武汉大学中南医院鲁志兵教授课题组与武汉大学病毒学国家重点实验室刘实教授课题组合作在Metabolism-Clinical and Experimental在线发表了题为“Interleukin-6 classic and trans-signaling utilize glucose metabolism reprogramming to achieve anti- or pro-inflammatory effects”的最新研究成果。该研究揭示了糖代谢信号网络与IL-6介导的炎症反应之间的交互调控,并系统阐明了其在病毒性心肌损伤中的作用,从免疫代谢的角度深入剖析了IL-6对病毒性心肌炎的调控功能和分子机理。

首先,研究者发现IL-6信号通路的活化能够驱动糖代谢的改变,引起相关中间产物的积累以及标志基因的表达,而应用IL-6受体的单克隆抗体Tocilizumab能够拮抗上述效应。
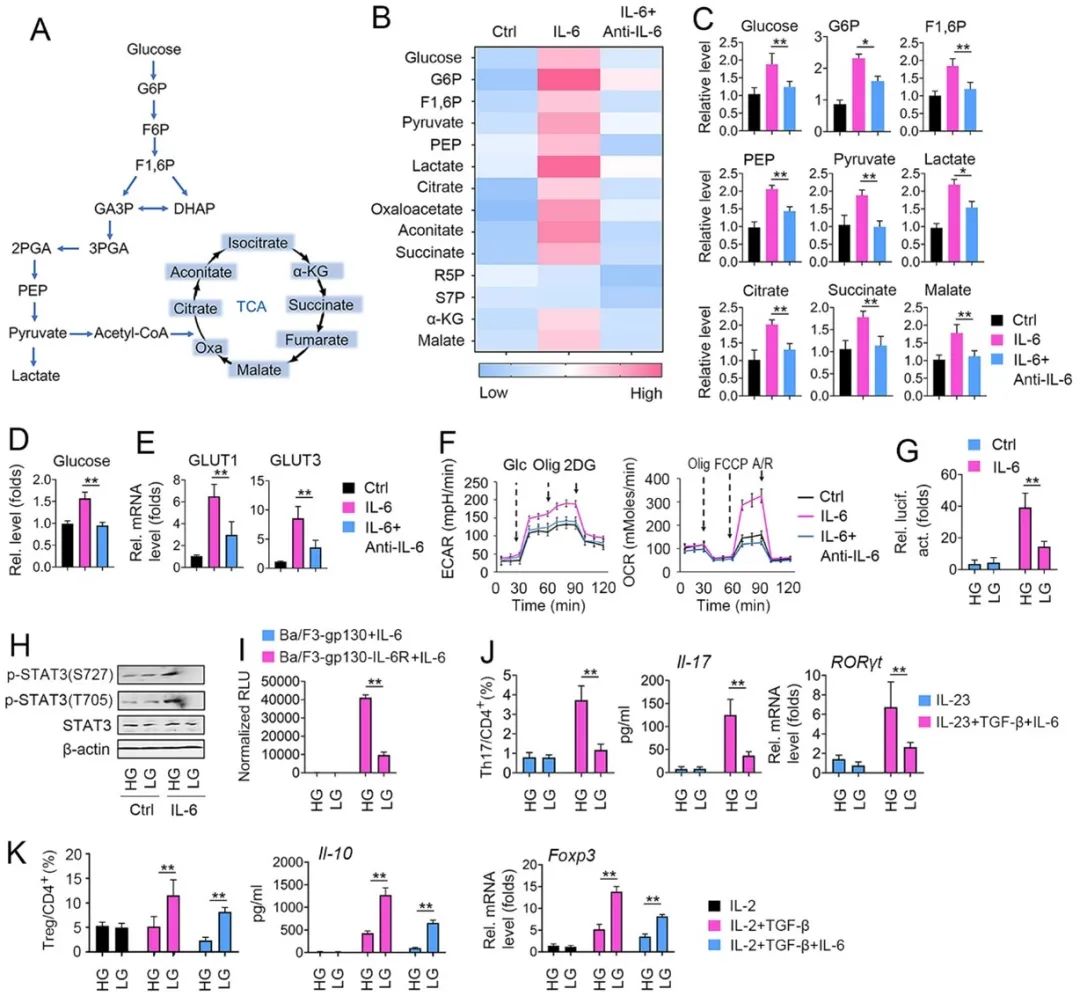
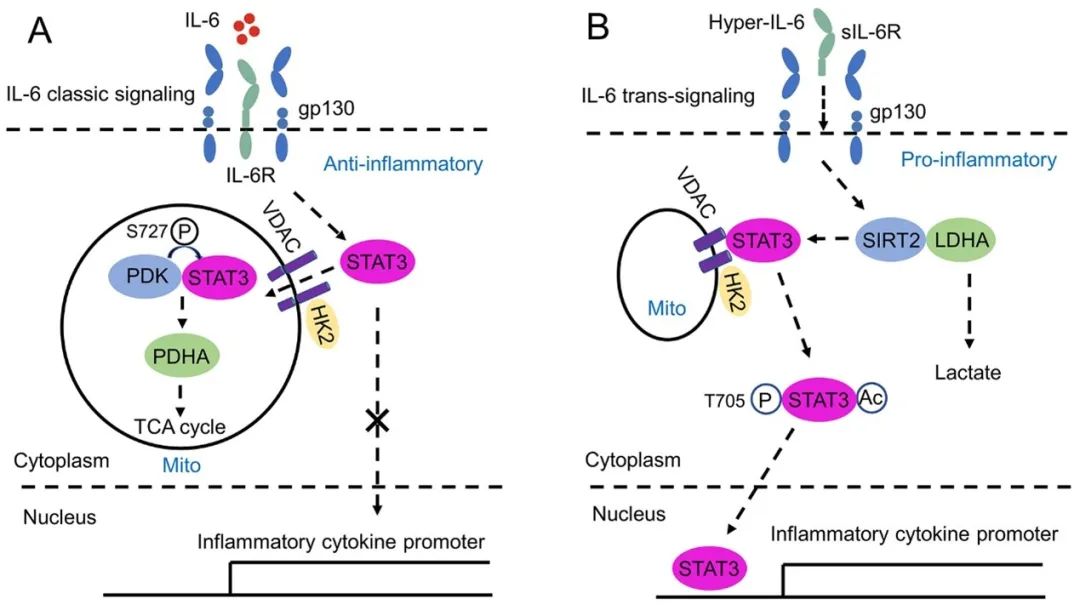
IL-6是一个具有促炎和抗炎双重特性的多功能细胞因子。IL-6与膜受体mIL-6R结合后,激活经典信号通路,发挥抗炎作用。IL-6还能够与可溶性sIL-6R受体结合,激活反式信号通路,发挥促炎作用。进一步的研究发现,IL-6经典信号通路和反式信号通路存在不同的糖代谢模式,前者能够驱动葡萄糖的氧化磷酸化,而后者诱导无氧糖酵解。

丙酮酸位于糖酵解和三羧酸循环的交叉点,其代谢命运主要受乳酸脱氢酶(LDHA)和丙酮酸脱氢酶(PDHA)的调控。前者通过将丙酮酸转化为乳酸来促进糖酵解,而后者通过将丙酮酸催化为乙酰辅酶A来维持三羧酸循环。研究者进一步探讨了IL-6诱导糖代谢重编程的分子机理。实验结果表明,IL-6经典信号通路能够促进PDK1和STAT3的相互作用,诱导PKD1与PDHA的解离,进而导致PDHA去磷酸激活,驱动葡萄糖氧化磷酸化。

而IL-6反式信号通路能够促进STAT3与SIRT2的解离,增强SIRT2和LDHA的相互作用,进而诱导LDHA的去乙酰化,增加其酶活性,最终促进葡萄糖的无氧糖酵解途径。

最后,研究者在小鼠疾病模型中探讨了IL-6信号驱动免疫代谢,调控Treg/Th17平衡和炎症反应,参与病毒性心肌炎进程的发病机理。
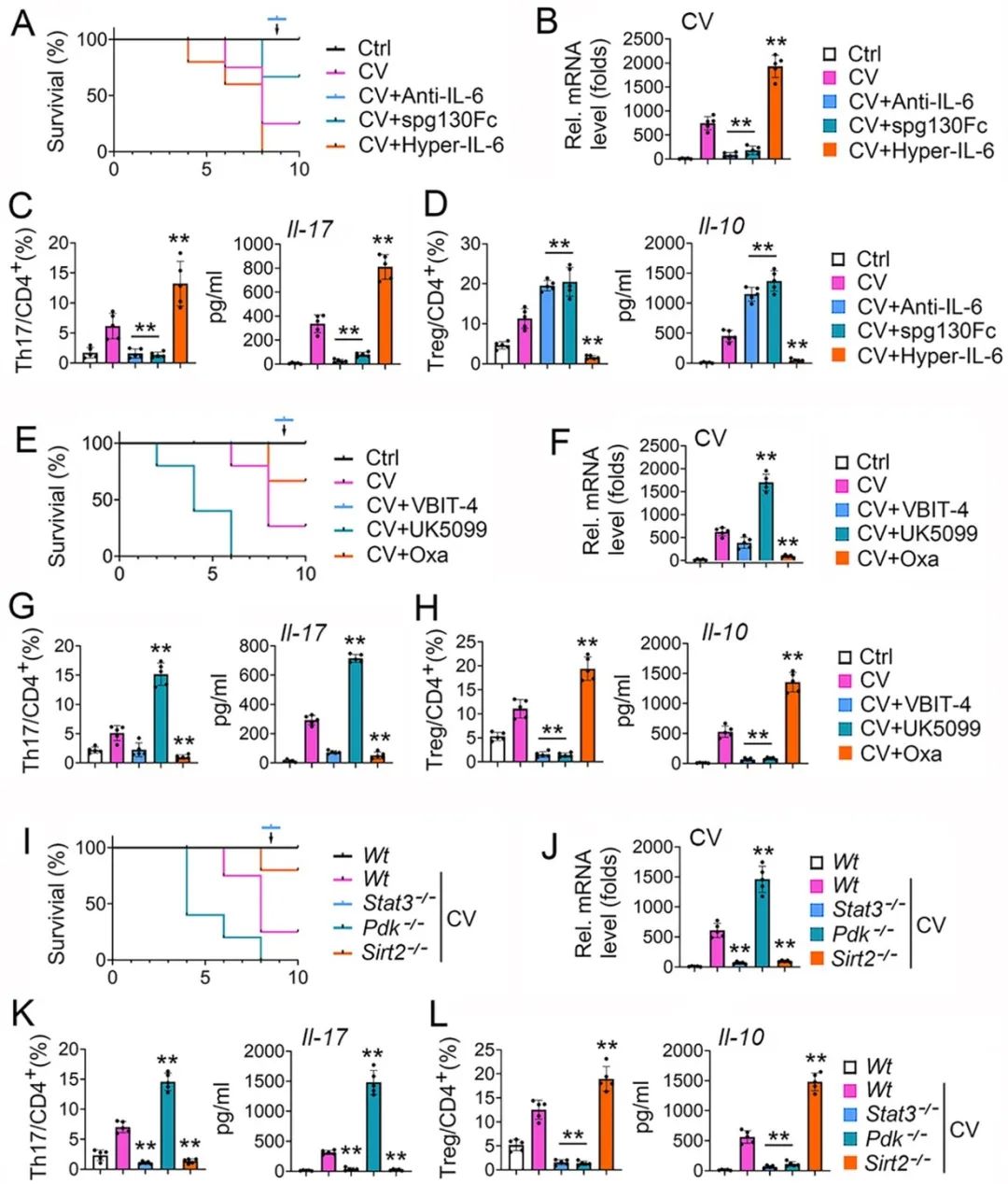
综上所述,该研究阐明了IL-6信号通路和糖代谢重编程的交互作用。IL-6经典信号通路通过STAT3/PDK1/PDHA轴驱动葡萄糖氧化磷酸化,调控抗炎反应;IL-6反式信号通路通过STAT3/LDHA/SIRT2轴诱导葡萄糖无氧糖酵解途径,调控促炎反应。
武汉大学中南医院鲁志兵教授、武汉大学病毒学国家重点实验室刘实教授为本文的共同通讯作用。该项工作得到了国家重点研发计划(2021YFC2701800, 2021YFC2701804)、国家自然科学基金(U22A20335,81872262)、湖北省杰出青年科学基金(2021CFA054)等项目的资助。
刘实教授课题组长期从事病毒调控免疫和炎症信号网络研究,围绕能量代谢与炎症信号通路的交互调控机制,通过系列研究工作,揭示了乳酸/MAVS复合物、LGALS3BP/TRAF复合物、OGT/IRF5复合物等多种免疫网络与糖脂代谢网络之间的关键蛋白质机器/代谢物动态组装与交互调控。靶向免疫与炎症网络的相关细胞器鉴定,阐明了穹窿体细胞器在病毒诱导免疫和炎症信号网络中的作用及机理。
鲁志兵教授团队长期从事心血管疾病的基础和临床研究,近年来,整合团队资源,建立创新研究团队,创立武汉大学心肌损伤与修复研究所,针对病毒性、缺血性、药物性等临床常见病理因素所致的心肌损伤开展了系列研究。团队从临床实践出发,于2019年疫情期间,对早期新冠肺炎患者的临床数据分析,在全球范围内率先揭示了新冠病毒感染与心肌损伤之间的关系,为合并基础心脏疾病的新冠肺炎患者的整体治疗策略提供了科学依据(JAMA Cardiol. 2020)。团队进一步与武汉大学病毒学国家重点实验室积极交叉合作,围绕病毒性心肌损伤的分子机制,开展深入研究。该研究系统阐明了IL-6介导葡萄糖代谢重编程和免疫炎症反应对病毒性心肌炎的调控作用和分子机制,为相关疾病的治疗开辟了新的策略和思路。
原文链接:
https://linkinghub.elsevier.com/retrieve/pii/S0026-0495(24)00058-1
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#病毒性心肌损伤# #病毒性心肌炎#
14